Xây dựng quy trình realtime Rt - Pcr phát hiện Sars - Cov - 2 trong mẫu bệnh phẩm lâm sàng
SARS-CoV-2 (COVID-19) là bệnh truyền nhiễm cấp tính lây truyền theo
đường hô hấp, gây đại dịch trên toàn cầu [1]. Tất cả các đối tượng đều có thể nhiễm
và mắc bệnh, 80% các trường hợp nhiễm bệnh có triệu chứng ở mức nhẹ, 15% bệnh
nhân có triệu chứng nặng và 5% là các ca bệnh nguy kịch, nguy cơ tử vong chủ yếu
là người lớn tuổi có bệnh lý nền, người suy giảm miễn dịch Các triệu chứng của
bệnh khi khởi phát khác nhau nhưng hầu hết những người bị nhiễm COVID-19 sẽ có
những biểu hiện như: sốt, ho, khó thở, mệt mỏi Thời gian ủ bệnh trung bình là 4
ngày (có thể từ 2 đến 7 ngày) [2, 3, 4]. Hiện nay chưa có vắc xin phòng bệnh, vì vậy
việc phát hiện sớm và chính xác tác nhân SARS-CoV-2 là chiến lược quan trọng của
quốc gia trong công tác phòng chống dịch.
Các kỹ thuật để phát hiện SARS-CoV-2 trên thế giới bao gồm test nhanh phát
hiện kháng thể, miễn dịch huỳnh quang, tuy nhiên phương pháp sinh học phân tử
realtime RT-PCR được đánh giá hiệu quả, có độ nhạy, độ đặc hiệu, độ chính xác
cao, được sử dụng trong các xét nghiệm khẳng định. Các quy trình xét nghiệm
SARS-CoV-2 bằng phương pháp realtime RT-PCR trên các vùng gen orf1ab
(RdRp), gen E, gen N, được công bố bởi các Viện nghiên cứu và CDC của Trung
Quốc, Đức, Hồng Kông, Nhật Bản, Thái Lan, Hoa Kỳ và Pháp đã được thông qua
WHO [6-11]. Một trong số đó là quy trình của Victor Corman và cs. (Đức) khuếch
đại đoạn gen trên vùng gen E để phát hiện bat-CoV, phát hiện đồng thời SARS-CoV
và SARS-CoV-2 trên gen RdRp. So với trình tự hệ gen SARS-CoV-2 đầu tiên
Wuhan-Hu-1 được công bố trên GenBank [5], đã xuất hiện nhiều đột biến gen, tuy
nhiên hiện tại quy trình của Victor Corman vẫn đặc hiệu

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5
Trang 6

Trang 7

Trang 8

Trang 9
Tóm tắt nội dung tài liệu: Xây dựng quy trình realtime Rt - Pcr phát hiện Sars - Cov - 2 trong mẫu bệnh phẩm lâm sàng

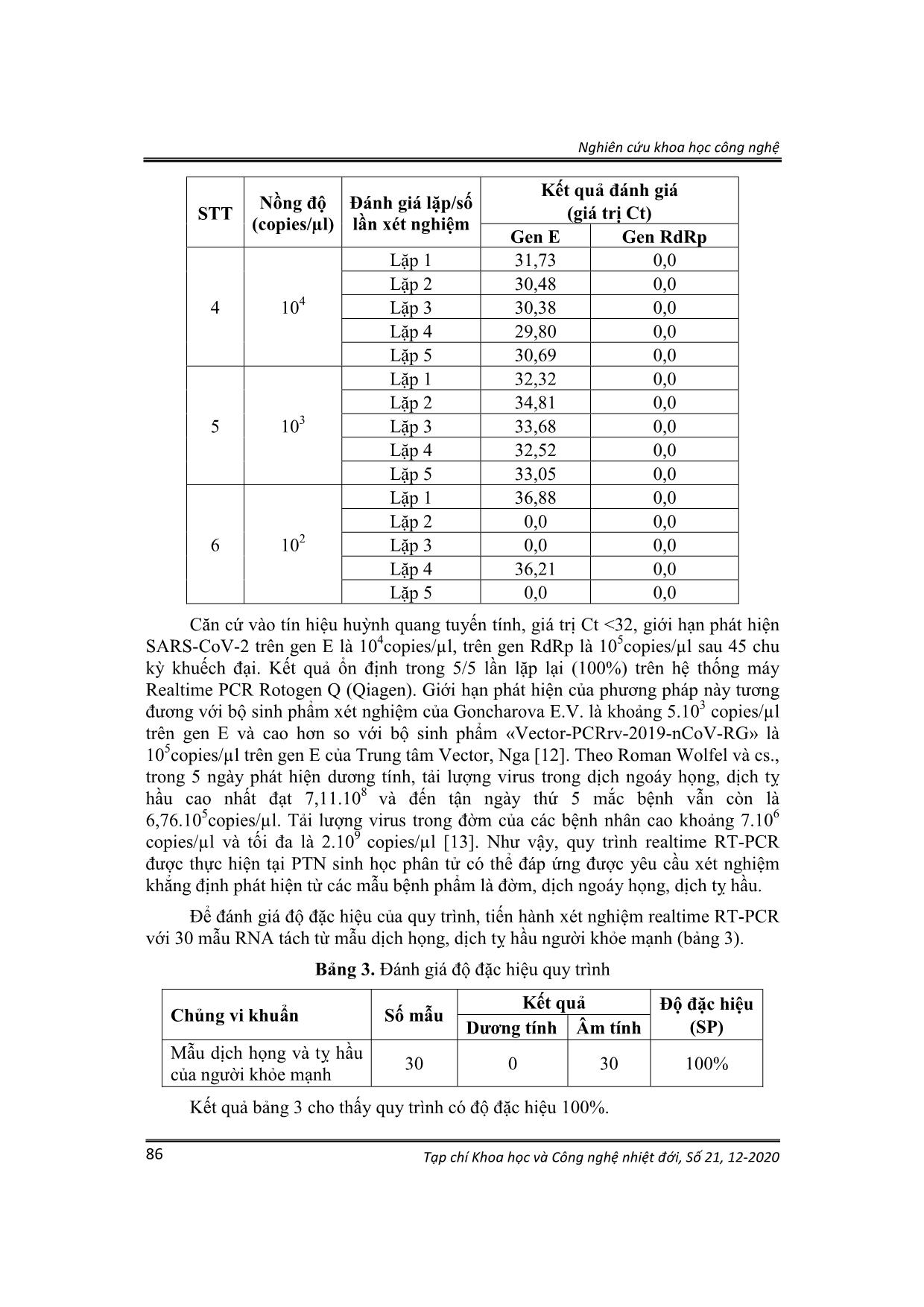
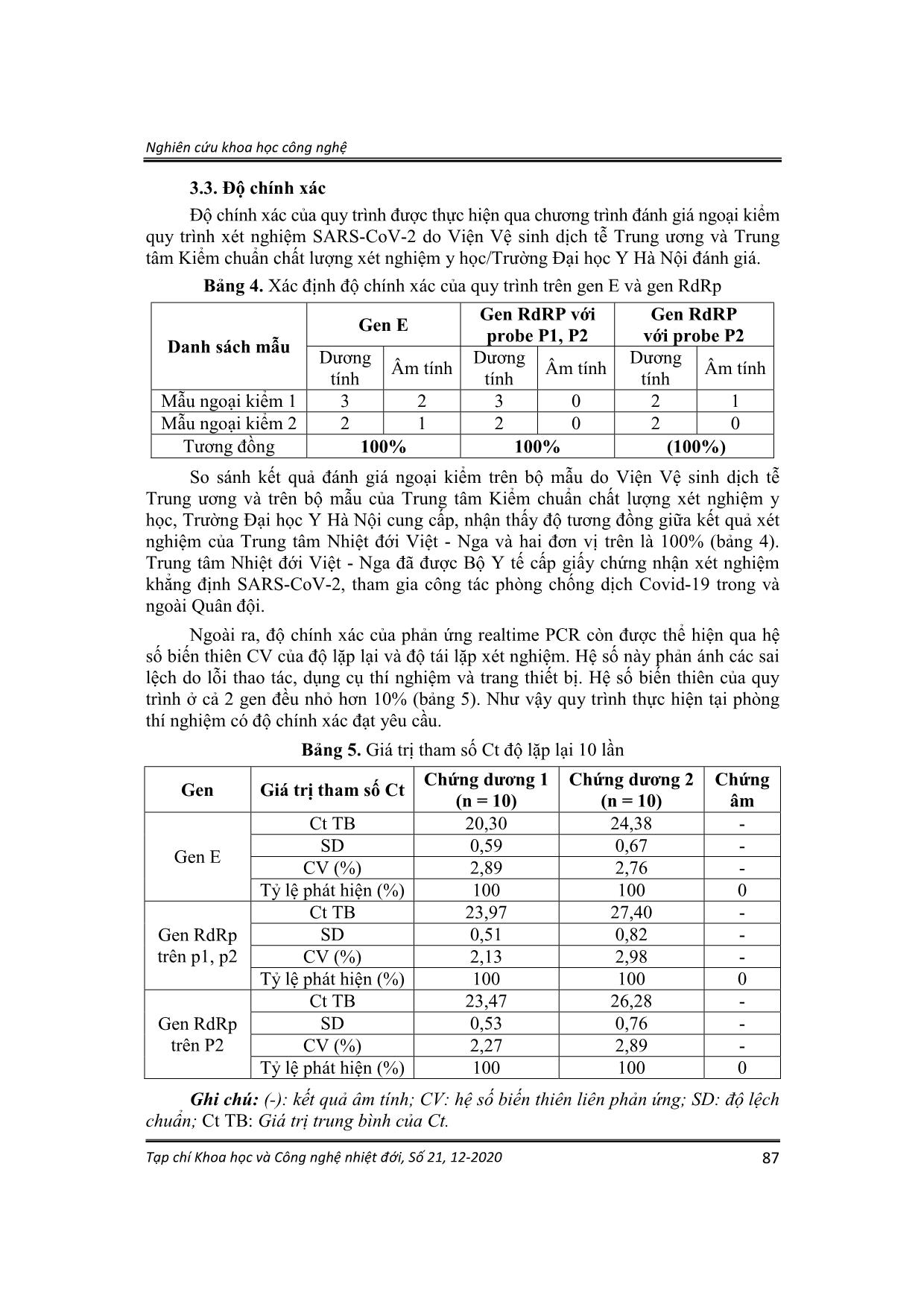
Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 82 XÂY DỰNG QUY TRÌNH REALTIME RT-PCR PHÁT HIỆN SARS-CoV-2 TRONG MẪU BỆNH PHẨM LÂM SÀNG BÙI THỊ THANH NGA (1), PHẠM THỊ HÀ GIANG (1), TRỊNH VĂN TOÀN (1), ĐẶNG THỊ VIỆT HƯƠNG (1), DƯƠNG VĂN NGHĨA (1), BÙI THỊ LAN ANH (1) 1. ĐẶT VẤN ĐỀ SARS-CoV-2 (COVID-19) là bệnh truyền nhiễm cấp tính lây truyền theo đường hô hấp, gây đại dịch trên toàn cầu [1]. Tất cả các đối tượng đều có thể nhiễm và mắc bệnh, 80% các trường hợp nhiễm bệnh có triệu chứng ở mức nhẹ, 15% bệnh nhân có triệu chứng nặng và 5% là các ca bệnh nguy kịch, nguy cơ tử vong chủ yếu là người lớn tuổi có bệnh lý nền, người suy giảm miễn dịch Các triệu chứng của bệnh khi khởi phát khác nhau nhưng hầu hết những người bị nhiễm COVID-19 sẽ có những biểu hiện như: sốt, ho, khó thở, mệt mỏiThời gian ủ bệnh trung bình là 4 ngày (có thể từ 2 đến 7 ngày) [2, 3, 4]. Hiện nay chưa có vắc xin phòng bệnh, vì vậy việc phát hiện sớm và chính xác tác nhân SARS-CoV-2 là chiến lược quan trọng của quốc gia trong công tác phòng chống dịch. Các kỹ thuật để phát hiện SARS-CoV-2 trên thế giới bao gồm test nhanh phát hiện kháng thể, miễn dịch huỳnh quang, tuy nhiên phương pháp sinh học phân tử realtime RT-PCR được đánh giá hiệu quả, có độ nhạy, độ đặc hiệu, độ chính xác cao, được sử dụng trong các xét nghiệm khẳng định. Các quy trình xét nghiệm SARS-CoV-2 bằng phương pháp realtime RT-PCR trên các vùng gen orf1ab (RdRp), gen E, gen N, được công bố bởi các Viện nghiên cứu và CDC của Trung Quốc, Đức, Hồng Kông, Nhật Bản, Thái Lan, Hoa Kỳ và Pháp đã được thông qua WHO [6-11]. Một trong số đó là quy trình của Victor Corman và cs. (Đức) khuếch đại đoạn gen trên vùng gen E để phát hiện bat-CoV, phát hiện đồng thời SARS-CoV và SARS-CoV-2 trên gen RdRp. So với trình tự hệ gen SARS-CoV-2 đầu tiên Wuhan-Hu-1 được công bố trên GenBank [5], đã xuất hiện nhiều đột biến gen, tuy nhiên hiện tại quy trình của Victor Corman vẫn đặc hiệu. Theo khuyến cáo của Bộ Y tế, Viện Y sinh nhiệt đới đã xây dựng quy trình xét nghiệm SARS-CoV-2 bằng kỹ thuật realtime RT-PCR theo khuyến cáo của WHO phù hợp điều kiện trong phòng thí nghiệm (PTN) lưu động, sẵn sàng tham gia nhiệm vụ phòng chống dịch viêm đường hô hấp cấp Covid-19 khi Bộ Quốc phòng yêu cầu. 2. ĐỐI TƯỢNGVÀ PHƯƠNG PHÁP NGHIÊN CỨU 2.1. Đối tượng nghiên cứu - 10453 mẫu lâm sàng: mẫu dịch họng, tỵ hầu của các đối tượng được Ban chỉ đạo phòng, chống dịch Trung tâm và Quân khu 5 chỉ định xét nghiệm trong thời gian từ 10/3-17/8/2020. - Tiêu chuẩn chọn: Mẫu dịch họng, dịch tỵ hầu của những người có triệu chứng sốt, ho, khó thở hoặc những người có tiền sử tiếp xúc với những người nhiễm, nghi nhiễm hoặc nhiễm COVID-19 trong vòng 14 ngày. - Tiêu chuẩn loại trừ: Mẫu dịch họng của những người sốt, ho do nguyên nhân khác, không có tiền sử tiếp xúc với người nhiễm COVID-19 và không tình nguyện tham gia nghiên cứu. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 83 - Chứng dương: Mẫu RNA virus SARS-CoV-2 tách từ dịch tế bào nuôi cấy do Viện Vệ sinh dịch tễ Trung ương cung cấp. - Bộ mẫu RNA ngoại kiểm (02 mẫu âm tính; 01 mẫu dương tính SARS; 02 mẫu dương tính SARS-CoV-2) do Viện Vệ sinh dịch tễ Trung ương cung cấp. Bộ mẫu RNA ngoại kiểm (02 mẫu dương tính với SARS-CoV-2; 01 mẫu âm tính) do Trung tâm Kiểm chuẩn chất lượng xét nghiệm y học - Trường Đại học Y Hà Nội cung cấp. - Mẫu âm: 30 mẫu dịch họng, dịch tỵ hầu người khoẻ mạnh, tình nguyện, không có biểu hiện của bệnh đường hô hấp và yếu tố dịch tễ từ vùng dịch hay tiếp xúc với người mắc COVID-19 trong vòng 14 ngày. 2.2. Phương pháp nghiên cứu 2.2.1. Phương pháp thu thập mẫu theo hướng dẫn số 343/QĐ-BYT Lấy đồng thời dịch ngoáy họng và dịch tỵ hầu của bệnh nhân. Đưa tăm bông vô trùng (6100, Aptaca, Ý) vào vùng hầu họng, miết và xoay tròn nhẹ 3-4 lần tại khu vực 2 bên vùng amidan và thành họng sau để lấy được dịch và tế bào vùng họng. Sử dụng que bông mềm vô trùng (WS1010, Vincen, Trung Quốc) lấy dịch tỵ hầu. Khi đưa que bông mềm vào mũi, vừa đẩy vừa xoay vào sâu một khoảng bằng ½ độ dài từ cánh mũi đến dái tai cùng phía. Giữ que bông mềm tại chỗ lấy mẫu trong vòng 5 giây để đảm bảo dịch thấm tối đa. Sau khi lấy dịch ty hầu và dịch ngoáy họng, các que lấy mẫu được bảo quản chung trong ống môi trường DMEM (code 11995065, Gibco, Mỹ). Ghi tên bệnh nhân, mã code lên trên ống lấy mẫu. Các mẫu được chuyển tới PTN từ 2-8 tiếng trong thùng lạnh và bảo quản ở -80oC. 2.2.2. Các cặp mồi sử dụng trong nghiên cứu Mồi và đầu dò theo công bố của Victor Corman và cs. được tổng hợp bởi Công ty Integrated DNA Technologies [6]. 02 cặp mồi và 3 probe đặc hiệu trên gen E (gen vỏ- Envelope) và gen RdRp (RNA polymerase phụ thuộc RNA - RNA dependent RNA polymerase). Bảng 1. Trình tự mồi và probe của gen E và gen RdRp Gen đích Mồi, probe Trình tự (5’-3’) Vị trí Gen E E - F1 ACAGGTACGTTAATAGTTAATAGCGT 26.269 - 26.294 E - R2 ATATTGCAGCAGTACGCACACA 26.360 - 26.381 P - E FAM-ACACTAGCCATCCTTACTGCGCTTCG-BBQ Gen RdRp RdRp - F2 GTGARATGGTCATGTGTGGCGG 15.431 - 15.452 RdRp -R1 CARATGTTAAASACACTATTAGCATA 15.505 - 15.530 RdRp - P1 FAM-CCAGGTGGWACRTCATCMGGTGATGC-BBQ RdRp- P2 FAM-CAGGTGGAACCTCATCAGGAGATGC-BBQ Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 84 2.2.3. Phương pháp tách chiết RNA Các mẫu bệnh phẩm được tiến hành tách chiết RNA bằng bộ kít QIAamp RNA mini kit (Qiagen, Đức). Quy trình tách chiết RNA được tiến hành theo hướng dẫn của nhà sản xuất. 2.2.4. Tạo panel chứng dương Để xác định giới hạn phát hiện, mẫu RNA của virus SARS-CoV-2 (có nồng độ ban đầu là 107copies/µl) được sử dụng để pha loãng theo cơ số 10. Tiến hành thực hiện phản ứng realtime RT-PCR trên dải mẫu từ 107 đến 102 copies/µl trên gen E và gen RdRp. 2.2.5. Phương pháp Realtime RT- PCR Quy trình xét nghiệm phát hiện SARS-CoV-2 được tiến hành theo 3 bước: Realtime RT-PCR 1: sàng lọc phát hiện Beta-coronavirus trên đoạn gen E với hỗn hợp phản ứng được tối ưu hóa với tổng thể tích là 25 μl bằng cách sử dụng kit SuperScript III Platinum One-Step qRT-PCR (Invitrogen, Thermo) chứa 5 μl khuôn mẫu RNA; 1 μl mỗi mồi E-F1 và E-R2; 0,5 μl probe R-P; 1 μl enzyme RT; 3,6 μl nước cất khử ion; 12,5 μl hỗn hợp 2X; 0,4 μl Mg+2. Phản ứng realtime RT-PCR 2 phát hiện virus SARS-CoV và SARS-CoV-2 trên đoạn gen RdRp với 02 probe P1 và P2 gồm: 5 μl khuôn mẫu RNA; 1,5 μl mồi RdRp-F2 và 2 μl mồi RdRp-R1; 0,5 μl probe RdRp-P1 và RdRp-P2; 1 μl enzyme RT; 1,6 μl nước cất khử ion; 12,5 μl hỗn hợp 2X; 0,4 μl Mg+2. Phản ứng Realtime RT-PCR 3: khẳng định virus SARS-CoV-2 trên đoạn gen RdRp với probe P2 gồm: 5 μl khuôn mẫu RNA; 1,5 μl mồi RdRp-F2 và 2 μl mồi RdRp-R1; 0,5 μl probe RdRp-P2; 1 μl enzyme RT; 2,1 μl nước cất khử ion; 12,5 μl hỗn hợp 2X; 0,4 μl Mg+2. Chương trình nhiệt của cả 3 phản ứng realtime RT-PCR gồm: 55oC/10 phút, 94oC/3 phút, (94oC/15 giây, 58oC/30 giây) 45 chu kỳ. Phản ứng khuếch đại RNA SARS-CoV-2 được thực hiện trên máy RotorGen Q phát hiện tại kênh phát huỳnh quang FAM. 2.2.6. Phương pháp xác định giới hạn phát hiện, đánh giá độ nhạy, tính chính xác - Giới hạn phát hiện: Nồng độ RNA tương đương 107copies/µl, tách từ tế bào nuôi cấy do Viện Vệ sinh Dịch tễ Trung ương cung cấp được pha loãng 10 lần để đạt dải pha loãng từ 107 đến102 copies/µl. Thí nghiệm được lặp lại 5 lần. - Độ nhạy phát hiện: Là nồng độ thấp nhất cho 100% số lần lặp lại có kết quả đánh giá dương tính SARS-CoV-2; - Tính chính xác: Khả năng cho kết quả đúng với các mẫu đã được đánh giá ngoại kiểm. Đối với quy trình realtime PCR, tiến hành đánh giá hệ số biến thiên liên phản ứng (CV) và độ lệch chuẩn (SD); Ct trung bình (Ct TB). CV ≤ 10%. 2.2.7. Đạo đức trong nghiên cứu Nghiên cứu đã được Hội đồng Đạo đức trong nghiên cứu y sinh học của Trung tâm Nhiệt đới Việt - Nga thông qua. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 85 3. KẾT QUẢ VÀ BÀN LUẬN 3.1. Kết quả khuếch đại trên gen E, gen RdRp Thực hiện quy trình xét nghiệm SARS-CoV-2 tại PTN sinh học phân tử Viện Y sinh nhiệt đới với mẫu chứng âm và chứng dương RNA tách từ dịch tế bào nuôi cấy, thí nghiệm lặp lại 3 lần. Kết quả hình 1 cho thấy chứng dương chạy trên gen E, gen RdRp có tín hiệu huỳnh quang rõ nét. Như vậy, thành phần bộ kit và kết quả ổn định như kết quả của Corman Victor M và cs. [6]. Hình 1. Mẫu chứng dương kênh FAM trên gen E, trên gen RdRp 3.2. Xác định giới hạn phát hiện, độ đặc hiệu của quy trình Để xác định giới hạn phát hiện của quy trình, tiến hành thí nghiệm trên các mẫu RNA SARS-CoV-2 do Viện VSDTTƯ cung cấp. Thực hiện phản ứng realtime RT-PCR trên gen E và gen RdRp. Bảng 2. Đánh giá độ nhạy phát hiện của quy trình trên gen E và gen RdRp STT Nồng độ (copies/µl) Đánh giá lặp/số lần xét nghiệm Kết quả đánh giá (giá trị Ct) Gen E Gen RdRp 1 107 Lặp 1 19,55 23,61 Lặp 2 20,36 23,09 Lặp 3 20,94 24,13 Lặp 4 19,69 23,85 Lặp 5 20,86 23,28 2 106 Lặp 1 23,9 25,90 Lặp 2 23,64 26,01 Lặp 3 24,69 26,55 Lặp 4 25,05 26,42 Lặp 5 24,49 26,58 3 105 Lặp 1 27,18 32,43 Lặp 2 27,11 31,14 Lặp 3 27,94 30,25 Lặp 4 28,06 30,70 Lặp 5 27,57 31,24 Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 86 STT Nồng độ (copies/µl) Đánh giá lặp/số lần xét nghiệm Kết quả đánh giá (giá trị Ct) Gen E Gen RdRp 4 104 Lặp 1 31,73 0,0 Lặp 2 30,48 0,0 Lặp 3 30,38 0,0 Lặp 4 29,80 0,0 Lặp 5 30,69 0,0 5 103 Lặp 1 32,32 0,0 Lặp 2 34,81 0,0 Lặp 3 33,68 0,0 Lặp 4 32,52 0,0 Lặp 5 33,05 0,0 6 102 Lặp 1 36,88 0,0 Lặp 2 0,0 0,0 Lặp 3 0,0 0,0 Lặp 4 36,21 0,0 Lặp 5 0,0 0,0 Căn cứ vào tín hiệu huỳnh quang tuyến tính, giá trị Ct <32, giới hạn phát hiện SARS-CoV-2 trên gen E là 104copies/µl, trên gen RdRp là 105copies/µl sau 45 chu kỳ khuếch đại. Kết quả ổn định trong 5/5 lần lặp lại (100%) trên hệ thống máy Realtime PCR Rotogen Q (Qiagen). Giới hạn phát hiện của phương pháp này tương đương với bộ sinh phẩm xét nghiệm của Goncharova E.V. là khoảng 5.103 copies/µl trên gen E và cao hơn so với bộ sinh phẩm «Vector-PCRrv-2019-nCoV-RG» là 105copies/µl trên gen E của Trung tâm Vector, Nga [12]. Theo Roman Wolfel và cs., trong 5 ngày phát hiện dương tính, tải lượng virus trong dịch ngoáy họng, dịch tỵ hầu cao nhất đạt 7,11.108 và đến tận ngày thứ 5 mắc bệnh vẫn còn là 6,76.105copies/µl. Tải lượng virus trong đờm của các bệnh nhân cao khoảng 7.106 copies/µl và tối đa là 2.109 copies/µl [13]. Như vậy, quy trình realtime RT-PCR được thực hiện tại PTN sinh học phân tử có thể đáp ứng được yêu cầu xét nghiệm khẳng định phát hiện từ các mẫu bệnh phẩm là đờm, dịch ngoáy họng, dịch tỵ hầu. Để đánh giá độ đặc hiệu của quy trình, tiến hành xét nghiệm realtime RT-PCR với 30 mẫu RNA tách từ mẫu dịch họng, dịch tỵ hầu người khỏe mạnh (bảng 3). Bảng 3. Đánh giá độ đặc hiệu quy trình Chủng vi khuẩn Số mẫu Kết quả Độ đặc hiệu (SP) Dương tính Âm tính Mẫu dịch họng và tỵ hầu của người khỏe mạnh 30 0 30 100% Kết quả bảng 3 cho thấy quy trình có độ đặc hiệu 100%. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 87 3.3. Độ chính xác Độ chính xác của quy trình được thực hiện qua chương trình đánh giá ngoại kiểm quy trình xét nghiệm SARS-CoV-2 do Viện Vệ sinh dịch tễ Trung ương và Trung tâm Kiểm chuẩn chất lượng xét nghiệm y học/Trường Đại học Y Hà Nội đánh giá. Bảng 4. Xác định độ chính xác của quy trình trên gen E và gen RdRp Danh sách mẫu Gen E Gen RdRP với probe P1, P2 Gen RdRP với probe P2 Dương tính Âm tính Dương tính Âm tính Dương tính Âm tính Mẫu ngoại kiểm 1 3 2 3 0 2 1 Mẫu ngoại kiểm 2 2 1 2 0 2 0 Tương đồng 100% 100% (100%) So sánh kết quả đánh giá ngoại kiểm trên bộ mẫu do Viện Vệ sinh dịch tễ Trung ương và trên bộ mẫu của Trung tâm Kiểm chuẩn chất lượng xét nghiệm y học, Trường Đại học Y Hà Nội cung cấp, nhận thấy độ tương đồng giữa kết quả xét nghiệm của Trung tâm Nhiệt đới Việt - Nga và hai đơn vị trên là 100% (bảng 4). Trung tâm Nhiệt đới Việt - Nga đã được Bộ Y tế cấp giấy chứng nhận xét nghiệm khẳng định SARS-CoV-2, tham gia công tác phòng chống dịch Covid-19 trong và ngoài Quân đội. Ngoài ra, độ chính xác của phản ứng realtime PCR còn được thể hiện qua hệ số biến thiên CV của độ lặp lại và độ tái lặp xét nghiệm. Hệ số này phản ánh các sai lệch do lỗi thao tác, dụng cụ thí nghiệm và trang thiết bị. Hệ số biến thiên của quy trình ở cả 2 gen đều nhỏ hơn 10% (bảng 5). Như vậy quy trình thực hiện tại phòng thí nghiệm có độ chính xác đạt yêu cầu. Bảng 5. Giá trị tham số Ct độ lặp lại 10 lần Gen Giá trị tham số Ct Chứng dương 1 (n = 10) Chứng dương 2 (n = 10) Chứng âm Gen E Ct TB 20,30 24,38 - SD 0,59 0,67 - CV (%) 2,89 2,76 - Tỷ lệ phát hiện (%) 100 100 0 Gen RdRp trên p1, p2 Ct TB 23,97 27,40 - SD 0,51 0,82 - CV (%) 2,13 2,98 - Tỷ lệ phát hiện (%) 100 100 0 Gen RdRp trên P2 Ct TB 23,47 26,28 - SD 0,53 0,76 - CV (%) 2,27 2,89 - Tỷ lệ phát hiện (%) 100 100 0 Ghi chú: (-): kết quả âm tính; CV: hệ số biến thiên liên phản ứng; SD: độ lệch chuẩn; Ct TB: Giá trị trung bình của Ct. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 88 Có thể nói, kết quả xét nghiệm chịu ảnh hưởng của nhiều yếu tố như tính chất mẫu, phòng xét nghiệm, trang thiết bị sử dụng và các điều kiện môi trường tại thời điểm xét nghiệm. Vì vậy việc xây dựng, đánh giá phương pháp xét nghiệm tại PTN cần được tiến hành trước khi đưa xét nghiệm mới vào phục vụ bệnh nhân, đặc biệt đối với xét nghiệm phát hiện SARS-CoV-2, đây là bước quan trọng, đảm bảo chất lượng xét nghiệm của PTN. Từ ngày 10/3/2020 đến 17/8/2020 thực hiện theo yêu cầu của ban chỉ đạo Phòng chống dịch COVID-19 Bộ Quốc phòng và Trung tâm, nhóm nghiên cứu đã tiến hành xét nghiệm virus SARS-CoV-2 tại PTN lưu động trên 10453 mẫu, trong đó có 115 mẫu của các cán bộ, chiến sĩ của Trường Quân sự Quân đoàn 1 - Ninh Bình, 403 từ các cán bộ, chiến sĩ thuộc 7 đồn của Bộ đội Biên phòng tỉnh Quảng Bình (Cửa khẩu quốc tế Cha Lo, Cà Xèng, Ra Mai, Cà Roòng, Cồn Roàng, Làng Mô, Làng Ho) và mẫu được gửi từ Y học dự phòng - Quân khu 5 là 3233 mẫu, Bệnh viện Quân y 17 là 973 mẫu, CDC Đà Nẵng là 929 mẫu và CDC Quảng Nam là 4480 mẫu. Hình 2. Mẫu dương phát hiện kênh FAM trên gen E và gen RdRp Kết quả realtime RT-PCR phát hiện 06 mẫu dương tính trên cả gen E (giá trị Ct từ 12,05 đến 29,47 và gen RdRp (giá trị Ct từ 14,47 đến 31,06) (hình 2). Trong đó 03/6 mẫu dương có tải lượng virus cao với giá trị Ct trên gen E lần lượt là 12,05; 15,01; 18,80 và trên gen RdRp là 14,47; 16,97 và 20,27. 4. KẾT LUẬN Quy trình xét nghiệm SARS-CoV-2 có giới hạn phát hiện là 103 copies/µl trên gen E và 105 copies/µl trên gen RdRp với độ nhạy, độ đặc hiệu và độ chính xác là 100%. Phòng thí nghiệm đã được Viện Vệ sinh dịch tễ Trung ương cấp giấy chứng nhận đủ năng lực xét nghiệm khẳng định SARS-CoV-2 bằng kỹ thuật realtime RT- PCR, tham gia công tác xét nghiệm SARS-CoV-2 trên 10.453 mẫu lâm sàng thu thập từ ngày 10/3/2020 đến ngày 17/8/2020 bằng kỹ thuật realtime RT-PCR, đã phát hiện 06 mẫu dương tính trên cả gen E và gen RdRp. Các kết quả phát hiện SARS- CoV-2 có độ tin cậy cao, đáp ứng kịp thời công tác phòng chống đại dịch hiện nay. Lời cảm ơn: Nhóm thực hiện đề tài xin gửi lời cảm ơn tới Viện Vệ sinh dịch tễ Trung ương và Trường Đại học Y Hà Nội đã hỗ trợ đề tài trong việc đánh giá ngoại kiểm và hỗ trợ chứng dương RNA virus SARS-CoV-2. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 89 TÀI LIỆU THAM KHẢO 1. World Health Organization (WHO), Coronavirus, Geneva: WHO; 2020 [Accessed 21 Jan 2020], Available from: https://www.who.int/health- topics/coronavirus. 2. Guan W.J., et al., Clinical characteristics of 2019 novel coronavirus infection in China. 2020. DOI: https://doi.org/10.1101/2020.02.06.20020974. 3. Huang C., et al., Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet, 2020, 395(10223):497-506. 4. To K.K., Tsang O.T., Leung W.S., et al., Temporal profiles of viral load in posterior oropharyngeal saliva samples and serum antibody responses during infection by SARS-CoV-2: an observational cohort study, Lancet Infect Dis 2020. 5. Zhang Y.Z., Novel 2019 coronavirus genome, Virological, [Accessed 21 Jan 2020], Available from: genome/319. 6. Victor Corman et al., Detection of 2019-nCoV by real-time RT-PCR, Euro Surveill., 2020, 25(3). 7. China_CDC, Specific primers and probes for detection 2019 novel coronavirus, 2020, DOI: 211337.html. 8. Nao N., et al., Detection of second case of 2019-nCoV infection in Japan, 2020, DOI: https://www.who.int/docs/default-source/coronaviruse/method- niid-20200123-2.pdf?sfvrsn=fbf75320_7. 9. HKU Med, Detection of 2019 Novel Coronavirus (2019-nCoV) in suspected human cases by RT-PCR, Available online: https://www.who.int/docs/ default- source /coronaviruse/peiris-protocol-16-1- 20.pdf?sfvrsn=af1aac73_4. 10. Centers for Disease Control and Prevention, A CDC 2019-Novel Coronavirus (2019-nCoV) Real-time RT-PCR diagnostic panel, Available online: https://www.fda.gov/media/134922/download 11. Institut Pasteur, Paris, Protocol: Real-Time RT-PCR Assays for the Detection of SARS-CoV-2, Available online: https://www.who.int/docs/default- source/coronaviruse/real-time-rt-pcr-assays-for-the-detectionof-sars-cov-2- institut-pasteur-paris.pdf?sfvrsn=3662fcb6_2. 12. Goncharova E.V, Donnikov A.E, Kadochnikova V.V, Morozova S.A, Boldyreva M.N, Galkina I.S, Blinov D.V, Real-time RT-PCR diagnostics of virus causing COVID-19, Фармакоэкономика, Современная Фармакоэкономика и Фармакоэпидемиология, 2020, Том 13, №1. 13. Roman Wolfel, Victor M. Corman, Virological assessment of hospitalized patients with COVID-2019, Nature 581, 2020, tr.465-469. Nghiên cứu khoa học công nghệ Tạp chí Khoa học và Công nghệ nhiệt đới, Số 21, 12-2020 90 SUMMARY VERIFICATION OF SARS-CoV-2 VIRUS DETECTION PROCEDURE The verification of SARS-CoV-2 virus detection procedure has been executed in the Laboratory of Molecular Biology- Bio-Medicine Institute. The results showed that the sensitivity, specificity and accuracy of procedure were 100% by using selected samples. Using the external control samples provided by the Center for Medical Testing Quality Control - Hanoi Medical University and the National Institute of Hygiene and Epidemiology Institute provided accurate results. It can be said that process validation improves test quality, thereby contributing to ensuring the quality of laboratory tests. The detection results of SARS-CoV-2 are highly reliable, timely respond to the current epidemic prevention. Keywords: COVID-19, SARS-CoV-2, E gene, RdRp gene. Nhận bài ngày 01 tháng 9 năm 2020 Phản biện xong ngày 07 tháng 10 năm 2020 Hoàn thiện ngày 04 tháng 11 năm 2020 (1) Viện Y sinh nhiệt đới, Trung tâm Nhiệt đới Việt - Nga
File đính kèm:
 xay_dung_quy_trinh_realtime_rt_pcr_phat_hien_sars_cov_2_tron.pdf
xay_dung_quy_trinh_realtime_rt_pcr_phat_hien_sars_cov_2_tron.pdf

