Đảm bảo chất lượng kế hoạch xạ trị vmat sử dụng phương pháp 1D, 2D và tái tạo liều 3D cho bệnh nhân ung thư vùng đầu cổ tại bệnh viện ung bướu Tp. HCM
Đặt vấn đề: Đảm bảo chất lượng cho kế hoạch trước khi xạ là một bước quan trọng không thể thiếu
trong một quy trình xạ vị nó ảnh hưởng trực tiếp tới kết quả điều trị cho bệnh nhân.
Mục đích nghiên cứu: Nghiên cứu này trình bày quy trình và kết quả đảm bảo chất lượng (QA,
quality assurance) cho kế hoạch xạ trị điều biến liều thể tích cung tròn (Volumetric Modulated Arc
Therapy, VMAT) tại Bệnh viện Ung bướu TP.HCM cho bệnh nhân ung thư vùng đầu cổ.
Đối tượng và phương pháp: Có 30 kế hoạch VMAT của bệnh nhân ung thư vùng đầu cổ được thực
hiện trong nghiên cứu này. Mỗi kế hoạch VMAT được lập trên phần mềm lập kế hoạch Eclipse 13.6 với
năng lượng 6 MV phát ra từ máy TrueBeam (Varian Medical Systems, Palo Alto, CA). Các kế hoạch này
đều được tiến hành kiểm tra độ chính xác về liều lượng giữa lập kế hoạch và thực tế trước khi điều trị.
Thiết bị sử dụng trong QA bao gồm buồng ion hóa (1D QA), EPID, ArcCHECK của hãng Sunnuclear (2D
QA) và phần mềm 3DVH (3D QA). Chỉ số Gamma tính bởi bằng phần mềm SNC và phần mềm 3DVH
được sử dụng để so sánh, đánh giá liều sai khác giữa tính toán và thực nghiệm.
Kết quả: Sai khác trung bình giữa liều đo đạc bằng buồng ion hóa và tính toán trên TPS là 0,88%
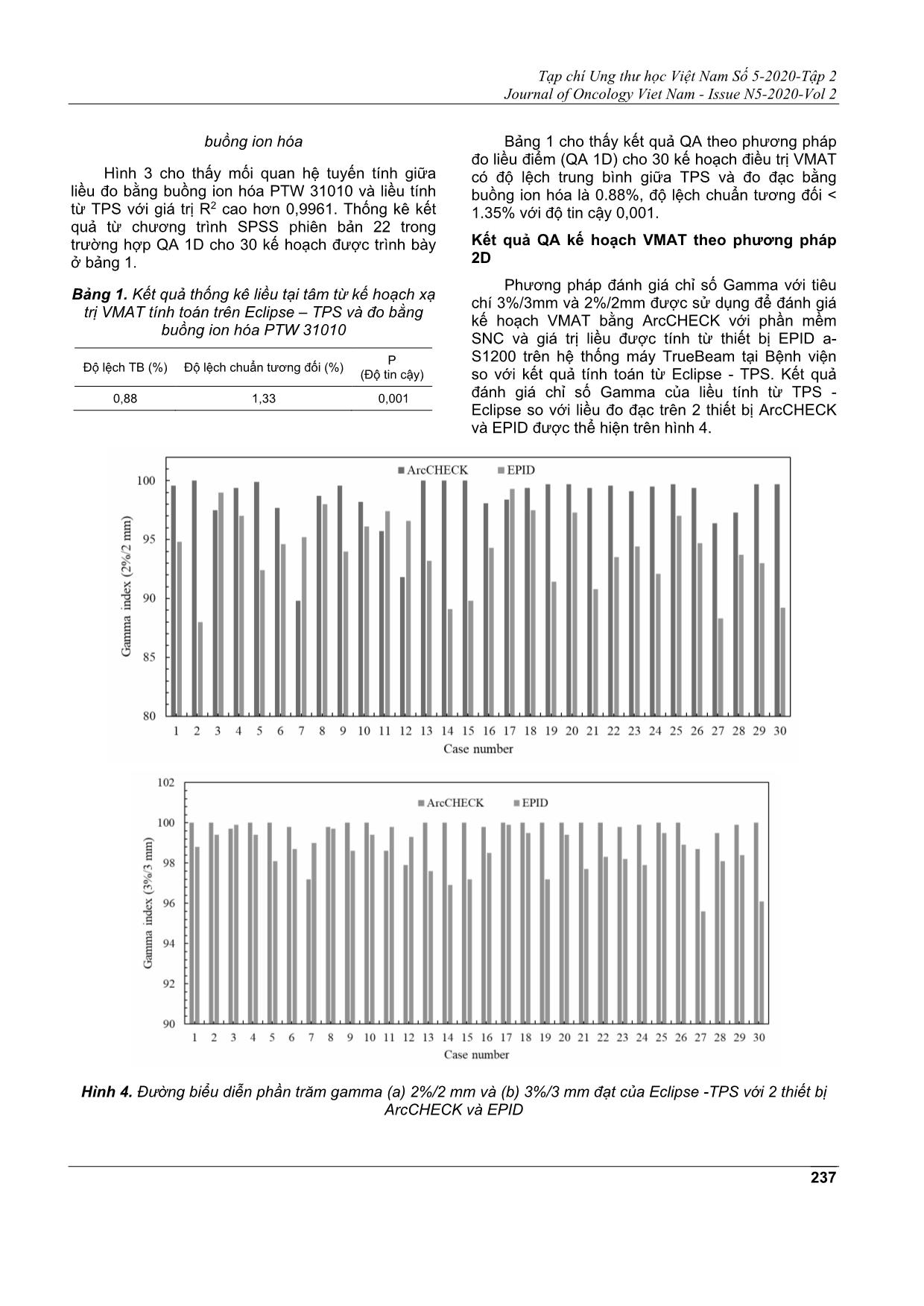
(1D). tỉ lệ phần trăm gamma (3%/3 mm) cho tất cả 30 bệnh nhân sử dụng 2 thiết bị EPID và ArcCHECK
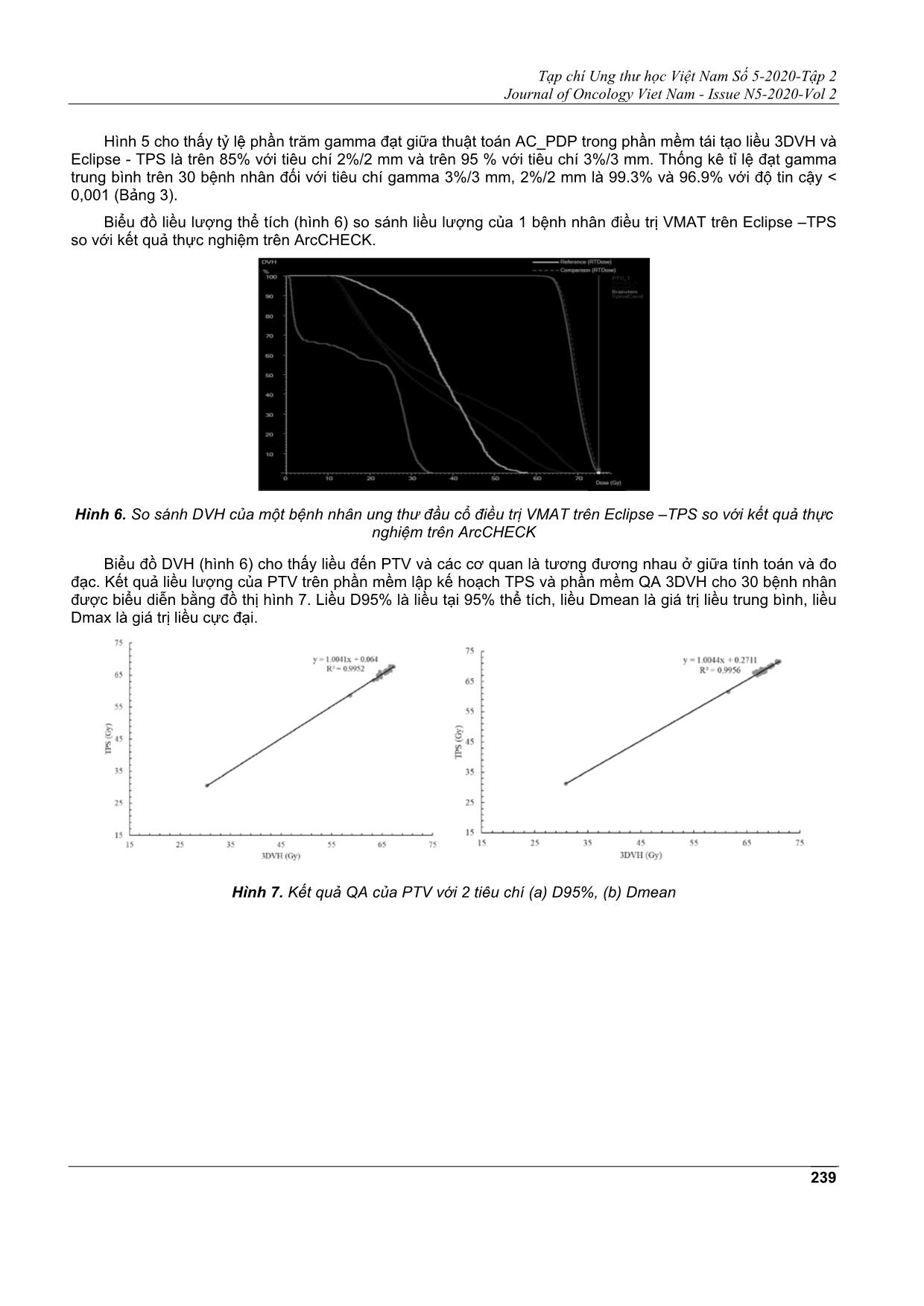
đều đạt trên 95% (2D). Chỉ số Gamma 3D bằng phương pháp tái tạo liều trên phần mềm 3DVH đối với
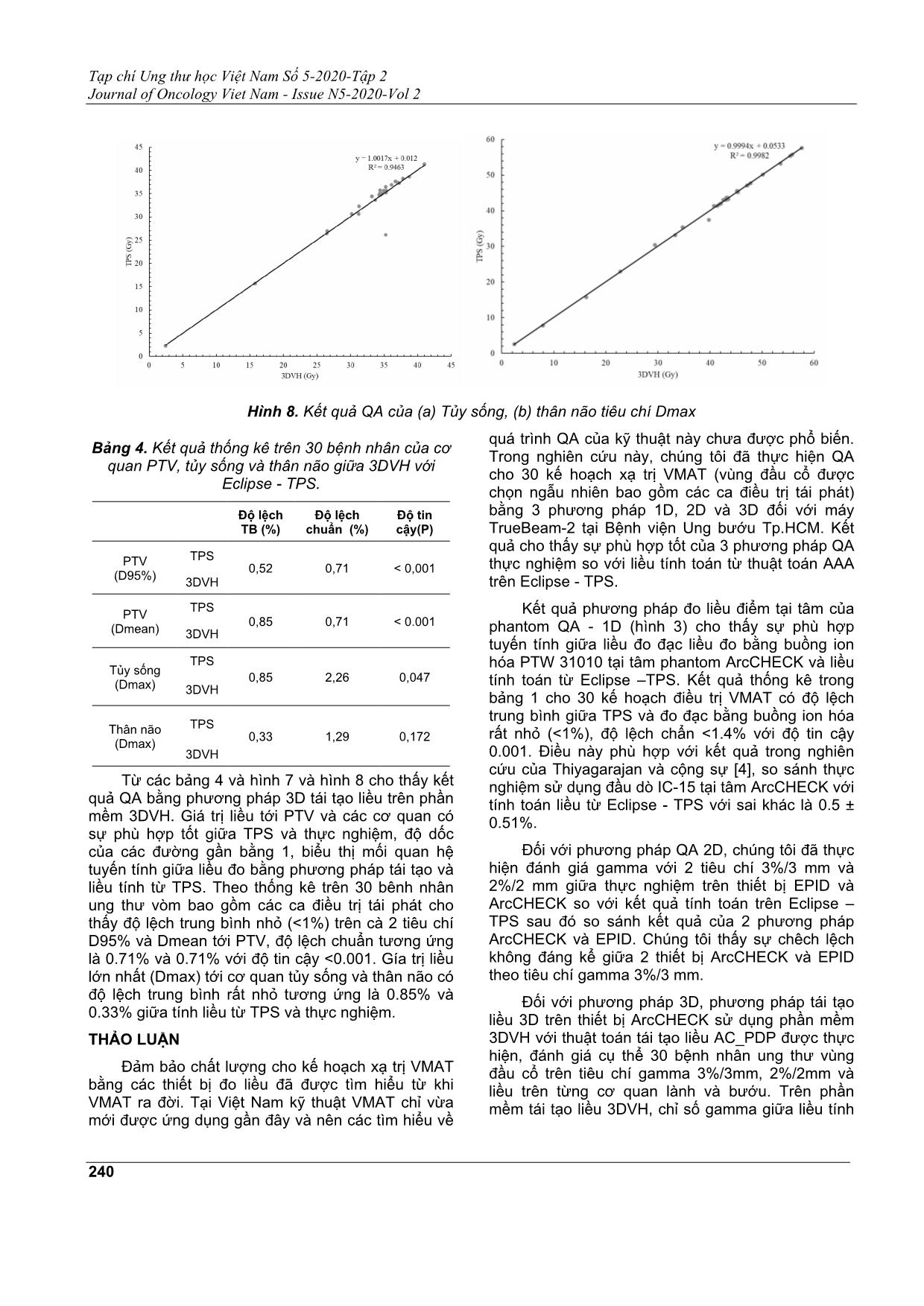
PTV (cả 2 tiêu chí D95% và Dmean) và cơ quan lành đều lớn hơn 95% cho tất cả 30 bệnh nhân.
Kết luận: Các kết quả của việc kiểm tra trước khi xạ trị buồng ion hóa, EPID, ArcCHECK và phần
mềm 3DVH đã khẳng định rằng kế hoạch VMAT cho ung thư vùng đầu cổ tại Bệnh viện ung bướu HCM
đảm bảo chất lượng, an toàn trước khi điều trị cho bệnh nhân vì các sai khác liều điểm đều nhỏ hơn 5%
và chỉ số gamma đều lớn hơn 90%.

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5

Trang 6
Trang 7
Trang 8

Trang 9
Trang 10
Tải về để xem bản đầy đủ
Tóm tắt nội dung tài liệu: Đảm bảo chất lượng kế hoạch xạ trị vmat sử dụng phương pháp 1D, 2D và tái tạo liều 3D cho bệnh nhân ung thư vùng đầu cổ tại bệnh viện ung bướu Tp. HCM

Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 233 XẠ TRỊ - KỸ THUẬT PHÓNG XẠ ĐẢM BẢO CHẤT LƯỢNG KẾ HOẠCH XẠ TRỊ VMAT SỬ DỤNG PHƯƠNG PHÁP 1D, 2D VÀ TÁI TẠO LIỀU 3D CHO BỆNH NHÂN UNG THƯ VÙNG ĐẦU CỔ TẠI BỆNH VIỆN UNG BƯỚU TP.HCM PHAN QUỐC UY1, NGUYỄN TRUNG HIẾU2, ĐẶNG THỊ MINH TÂM3, VÕ TẤN LINH3,TRƯƠNG HỮU THANH3 Địa chỉ liên hệ: Phan Quốc Uy Email: phanquocuy_real@yahoo.com Ngày nhận bài: 12/10/2020 Ngày phản biện: 03/11/2020 Ngày chấp nhận đăng: 05/11/2020 1 KS. Phó Trưởng Khoa Kỹ thuật Phóng xạ - Bệnh viện Ung Bướu TP. HCM 2 KS. Trưởng Khoa Kỹ thuật Phóng xạ - Bệnh viện Ung Bướu TP. HCM 3 KS Khoa Kỹ thuật Phóng xạ - Bệnh viện Ung Bướu TP. HCM GIỚI THIỆU Kỹ thuật xạ trị điều biến liều thể tích cung tròn (VMAT) hay còn gọi là RapidArc là kỹ thuật tiên tiến phát triển từ kỹ thuật xạ trị (IMRT) cho phép giảm đáng kể thời gian trong quá trình điều trị do sự thay đổi đồng thời tốc độ quay đầu máy gia tốc. Do những hạn chế về thiết bị và thuật toán sử dụng TÓM TẮT Đặt vấn đề: Đảm bảo chất lượng cho kế hoạch trước khi xạ là một bước quan trọng không thể thiếu trong một quy trình xạ vị nó ảnh hưởng trực tiếp tới kết quả điều trị cho bệnh nhân. Mục đích nghiên cứu: Nghiên cứu này trình bày quy trình và kết quả đảm bảo chất lượng (QA, quality assurance) cho kế hoạch xạ trị điều biến liều thể tích cung tròn (Volumetric Modulated Arc Therapy, VMAT) tại Bệnh viện Ung bướu TP.HCM cho bệnh nhân ung thư vùng đầu cổ. Đối tượng và phương pháp: Có 30 kế hoạch VMAT của bệnh nhân ung thư vùng đầu cổ được thực hiện trong nghiên cứu này. Mỗi kế hoạch VMAT được lập trên phần mềm lập kế hoạch Eclipse 13.6 với năng lượng 6 MV phát ra từ máy TrueBeam (Varian Medical Systems, Palo Alto, CA). Các kế hoạch này đều được tiến hành kiểm tra độ chính xác về liều lượng giữa lập kế hoạch và thực tế trước khi điều trị. Thiết bị sử dụng trong QA bao gồm buồng ion hóa (1D QA), EPID, ArcCHECK của hãng Sunnuclear (2D QA) và phần mềm 3DVH (3D QA). Chỉ số Gamma tính bởi bằng phần mềm SNC và phần mềm 3DVH được sử dụng để so sánh, đánh giá liều sai khác giữa tính toán và thực nghiệm. Kết quả: Sai khác trung bình giữa liều đo đạc bằng buồng ion hóa và tính toán trên TPS là 0,88% (1D). tỉ lệ phần trăm gamma (3%/3 mm) cho tất cả 30 bệnh nhân sử dụng 2 thiết bị EPID và ArcCHECK đều đạt trên 95% (2D). Chỉ số Gamma 3D bằng phương pháp tái tạo liều trên phần mềm 3DVH đối với PTV (cả 2 tiêu chí D95% và Dmean) và cơ quan lành đều lớn hơn 95% cho tất cả 30 bệnh nhân. Kết luận: Các kết quả của việc kiểm tra trước khi xạ trị buồng ion hóa, EPID, ArcCHECK và phần mềm 3DVH đã khẳng định rằng kế hoạch VMAT cho ung thư vùng đầu cổ tại Bệnh viện ung bướu HCM đảm bảo chất lượng, an toàn trước khi điều trị cho bệnh nhân vì các sai khác liều điểm đều nhỏ hơn 5% và chỉ số gamma đều lớn hơn 90%. Từ khóa: VMAT, ArcCHECK, QA 1D, QA 2D, QA 3D. Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 234 trong tính toán liều nên mặc dù VMAT đã được phát triển từ rất sớm - năm 1995[1], nhưng mãi cho đến năm 2007 VMAT được giới thiệu lần đầu trong lâm sàng[2]. VMAT cho phép thay đổi đồng thời 3 thông số trong quá trình phát tia là: tốc độ quay đầu máy gia tốc, hình dạng chùm tia tạo ra nhờ MLC và suất liều. Trong khi đó, kỹ thuật IMRT chỉ cho phép thay đổi 2 thông số đó là hình dạng chùm và suất liều. Kỹ thuật VMAT không những tạo ra phân bố liều tốt hơn với IMRT mà còn có thời gian phát tia ngắn hơn. Chính vì lý do đó mà kỹ thuật VMAT ngày càng được sử dụng rộng rãi tại nhiều nước trên thế giới như Hoa Kỳ, Pháp, Anh, Nhật, Hàn Quốc,[3]. Tại Việt Nam, kỹ thuật VMAT vẫn chưa được sử dụng thường quy, rộng rãi tại trên toàn quốc mà chỉ được áp dụng tại một số cơ sở xạ trị lớn như Bệnh viện Ung bướu Tp.HCM, Bệnh viện 108, Bệnh viện Chợ Rẫy,... Kỹ thuật VMAT rất phức tạp vì có nhiều thông số thay đổi trong quá trình phát tia nên thực nghiệm tiến hành kiểm tra độ chính xác về liều lượng giữa lập kế hoạch và thực tế trước khi điều trị cho kế hoạch xạ trị VMAT được bắt buộc phải tiến hành tại các cơ sở xạ trị. Do đó, việc đảm bảo chất lượng kế hoạch xạ trị VMAT thu hút được quan tâm chú ý bởi các nhà vật lý y khoa trong nước và quốc tế. Có nhiều phương pháp và thiết bị khác nhau để đảm bảo chất lượng kế hoạch xạ trị VMAT. Nhìn chung, có ba phương pháp chính được áp dụng phổ biến đó là phương pháp đo liều một chiều (1D) sử dụng đầu dò, nhiệt kế phát quang (TLD); phương pháp đo liều phân bố hai chiều (2D) sử dụng mảng đầu dò 2 chiều hoặc dùng film; và phương pháp phân bố ba chiều (3D) sử dụng các mảng đầu dò 3 chiều hoặc tái tạo lại phân bố liệu bằng các phần mềm chuyên dụng. Thiyagarajan và cộng sự [4] đánh giá kế hoạch VMAT của họ bằng buồng ion hóa (IC-15) và ArcCHECK. Kết quả chỉ ra rằng, sai khác giữa TPS và thực nghiệm sử dụng buồng ion hóa là 0,5% và chỉ số gamma trung bình với tiêu chí 3%/ 3mm là 98.53%. Nghiên cứu của Li và công sự[5] sử dụng ArcCHECK để QA cho 10 kế hoạch IMRT và VMAT. Chỉ số gamma trung bình (3%/3 mm) cho 10 kế hoạch IMRT và VMAT lần lượt là 95% và 93%. Tại Việt Nam, kỹ thuật VMAT chỉ vừa mới được ứng dụng trong một vài năm gần đây. Trong đó, Bệnh viện Ung bướu TP.HCM đã từng bước áp dụng kỹ thuật VMAT trong lâm sàng và đã trang bị được các thiết bị như ArcCHECK, phần mềm 3DVH để QA cho kỹ thuật VMAT. Do đó, mục tiêu của nghiên cứu này là đánh giá kỹ thuật VMAT cho bệnh nhân ung thư vùng đầu cổ tại Bệnh viện Ung bướu TP.HCM (Bệnh viện) bằng các thiết bị trên. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU Kế hoạch xạ trị VMAT Ba mươi bệnh nhân ung thư đầu cổ được lựa chọn ngẫu nhiên được lập kế hoạch xạ trị VMAT bằng thuật toán tính liều AAA trên phần mềm lập kế hoạch điều trị (TPS) Eclipse phiên bản 13.6 với năng lượng 6 MV và suất liều 600 MU/phút p ... ế hoạch xạ trị (ảnh CT, cấu trúc cơ quan, kế hoạch xạ trị) và file tính liều từ phần mềm SNC trên thiết bị QA ArcCHECK được đưa vào phần mềm 3DVH thực hiện tái tạo liều bằng giải thuật AC_PDP. Kết quả được đánh giá chỉ số Gamma và sự chênh lệch liều của các cơ quan và PTV giữa tính toán trên TPS và đo đạc. Phương pháp đánh giá Độ lệch tương đối Độ lệch tương đối của liều giữa thực nghiệm và tính toán từ TPS được tính [3]: Meas TPS Meas D D%DD 100D (2.1) Trong đó: DMeas là giá trị liều từ đo đạc thực nghiệm và DTPS là giá trị liều được tính bởi TPS. Tính chỉ số Gamma Sai khác liều điểm được sử dụng để đánh giá kết quả độ lệch giữa thực nghiệm và tính toán có thể gây ra các sai số ở các vùng liều thấp và khu vực có độ biên thiên liều cao [7]. Do đó, chỉ số Gamma là một phương pháp được dùng để đánh kết hợp giữa sai số liều lượng ∆D trong phạm vi khoảng cách cho phép DTA (thông thường ∆D/DTA = 3%/3 mm hoặc ∆D/DTA = 2%/2 mm). Chỉ số Gamma được tính theo công thức [7]: 2 2m c m cm c 2 2 M M r r ,r δ r ,rΓ r ,r = +Δd ΔD (2.2) Trong đó: + ∆D = m c c c m mδ r ,r = D (r ) -D (r ) là sai khác liều tính toán với liều đo. + ∆d = 2 m c m cr r ,r = r - r là sai khác về vị trí đối với cùng một giá trị liều. + rm là vị trí của điểm đo, rc là vị trí không gian của phân bố tính toán ứng với điểm đo. KẾT QUẢ Kết quả QA kế hoạch VMAT theo phương pháp 1D Tiến hành QA theo phương pháp đo liều điểm (QA 1D) sử dụng ArcCHECK kết nối buồng ion hóa PTW 31010. Kết quả so sánh liều đo đạc tại tâm ArcCHECK bằng buồng ion hóa PTW 31010 với điểm liều tương ứng được tính từ Eclipse - TPS cho 30 kế hoạch điều trị VMAT của bệnh nhân ung thư vòm được thể hiện trong hình 3. Hình 3. Kết quả liều lượng giữa TPS và đo đạc bằng Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 237 buồng ion hóa Hình 3 cho thấy mối quan hệ tuyến tính giữa liều đo bằng buồng ion hóa PTW 31010 và liều tính từ TPS với giá trị R2 cao hơn 0,9961. Thống kê kết quả từ chương trình SPSS phiên bản 22 trong trường hợp QA 1D cho 30 kế hoạch được trình bày ở bảng 1. Bảng 1. Kết quả thống kê liều tại tâm từ kế hoạch xạ trị VMAT tính toán trên Eclipse – TPS và đo bằng buồng ion hóa PTW 31010 Độ lệch TB (%) Độ lệch chuẩn tương đối (%) P (Độ tin cậy) 0,88 1,33 0,001 Bảng 1 cho thấy kết quả QA theo phương pháp đo liều điểm (QA 1D) cho 30 kế hoạch điều trị VMAT có độ lệch trung bình giữa TPS và đo đạc bằng buồng ion hóa là 0.88%, độ lệch chuẩn tương đối < 1.35% với độ tin cậy 0,001. Kết quả QA kế hoạch VMAT theo phương pháp 2D Phương pháp đánh giá chỉ số Gamma với tiêu chí 3%/3mm và 2%/2mm được sử dụng để đánh giá kế hoạch VMAT bằng ArcCHECK với phần mềm SNC và giá trị liều được tính từ thiết bị EPID a- S1200 trên hệ thống máy TrueBeam tại Bệnh viện so với kết quả tính toán từ Eclipse - TPS. Kết quả đánh giá chỉ số Gamma của liều tính từ TPS - Eclipse so với liều đo đạc trên 2 thiết bị ArcCHECK và EPID được thể hiện trên hình 4. Hình 4. Đường biểu diễn phần trăm gamma (a) 2%/2 mm và (b) 3%/3 mm đạt của Eclipse -TPS với 2 thiết bị ArcCHECK và EPID Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 238 Hình 4 cho thấy tỉ lệ gamma đạt với tiêu chí 3%/3 mm đạt trên 95% và 2%/2 mm trên 87% của 2 thiết bị EPID và ArcCHECK so với liều tính toán từ Eclipse - TPS. ArcCHECK cho thấy sự phù hợp với TPS tốt hơn so với kết quả đánh giá chỉ số gamma giữa EPID và TPS. Kết quả thống kê bằng SPSS cho tỉ lệ gamma đạt của 30 kế hoạch VMAT giữa 2 thiết bị EPID và ArcCHECK được trình bày trong bảng 2. Bảng 2. Kết quả thống kê về so sánh chỉ số phù hợp gamma giữa 2 thiết bị EPID, ArcCHECK và Eclipse - TPS với tiêu chí 3%/3 mm và 2%/2 mm. Tiêu chí gamma Thiết bị Gamma TB (%) Độ lệch chuẩn (%) Độ tin cậy (P) 3%/3 mm ArcCHECK 99,7 0,68 < 0,001 EPID 98,5 1,11 < 0,001 2%/2 mm ArcCHECK 98,4 2,37 < 0,001 EPID 94,1 3,18 < 0,001 Bảng 2 cho thấy có sự chêch lệch nhỏ giữa đánh giá chỉ số gamma bằng 2 thiết bị ArcCHECK và EPID với tiêu chí 3%/3mm và 2%/2mm. Với tiêu chí 3%/3mm tỉ lệ gamma đạt trung bình cho 30 kế hoạch trên EPID và ArcCHECK là 98,5% và 99,7%, tương ứng với độ lệch chuẩn lần lượt là 1,11% và 0,68% với độ tin cậy <0.001. Với tiêu chí 2%/2mm tỉ lệ gamma đạt trung bình cho 30 kế hoạch trên EPID và ArcCHECK lần lượt là 94,1% và 98,4% với độ tin cậy < 0.001. Kết quả QA kế hoạch VMAT theo phương pháp 3D Hình 5 đánh sự sai khác về liều lượng và khoảng cách qua so sánh chỉ số Gamma giữa liều ghi nhận từ phần mềm tái tạo từ phần mềm 3DVH và liều tính toán từ Eclipse – TPS. Kết quả sự khác nhau về liều lượng của PTV và các cơ quan lành với 30 kế hoạch xạ trị VMAT vùng đầu cổ được tái tạo liều trên phần mềm 3DVH và tính toán từ thuật toán AAA trên Eclipse -TPS được thể hiện trong các hinh 7, 8. Hình 5. Kết quả đánh giá chỉ số phù hợp Gamma giữa 3DVH và Eclipse – TPS với tiêu chí (a) 3%/3 mm và (b) 2%/2 mm. Bảng 3. Kết quả thống kê về so sánh chỉ số gamma giữa phần mềm tái tạo liều 3DVH của ArcCHECK và liều tính toán từ Eclipse - TPS với tiêu chí 3%/3 mm và 2%/2mm Tiêu chí Gamma TB (%) Độ lệch chuẩn (%) Độ tin cậy (P) 3%/3 mm 99,3 1,19 < 0,001 2%/2 mm 96,9 3,18 < 0,001 Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 239 Hình 5 cho thấy tỷ lệ phần trăm gamma đạt giữa thuật toán AC_PDP trong phần mềm tái tạo liều 3DVH và Eclipse - TPS là trên 85% với tiêu chí 2%/2 mm và trên 95 % với tiêu chí 3%/3 mm. Thống kê tỉ lệ đạt gamma trung bình trên 30 bệnh nhân đối với tiêu chí gamma 3%/3 mm, 2%/2 mm là 99.3% và 96.9% với độ tin cậy < 0,001 (Bảng 3). Biểu đồ liều lượng thể tích (hình 6) so sánh liều lượng của 1 bệnh nhân điều trị VMAT trên Eclipse –TPS so với kết quả thực nghiệm trên ArcCHECK. Hình 6. So sánh DVH của một bệnh nhân ung thư đầu cổ điều trị VMAT trên Eclipse –TPS so với kết quả thực nghiệm trên ArcCHECK Biểu đồ DVH (hình 6) cho thấy liều đến PTV và các cơ quan là tương đương nhau ở giữa tính toán và đo đạc. Kết quả liều lượng của PTV trên phần mềm lập kế hoạch TPS và phần mềm QA 3DVH cho 30 bệnh nhân được biểu diễn bằng đồ thị hình 7. Liều D95% là liều tại 95% thể tích, liều Dmean là giá trị liều trung bình, liều Dmax là giá trị liều cực đại. Hình 7. Kết quả QA của PTV với 2 tiêu chí (a) D95%, (b) Dmean Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 240 Hình 8. Kết quả QA của (a) Tủy sống, (b) thân não tiêu chí Dmax Bảng 4. Kết quả thống kê trên 30 bệnh nhân của cơ quan PTV, tủy sống và thân não giữa 3DVH với Eclipse - TPS. Độ lệch TB (%) Độ lệch chuẩn (%) Độ tin cậy(P) PTV (D95%) TPS 0,52 0,71 < 0,001 3DVH PTV (Dmean) TPS 0,85 0,71 < 0.001 3DVH Tủy sống (Dmax) TPS 0,85 2,26 0,047 3DVH Thân não (Dmax) TPS 0,33 1,29 0,172 3DVH Từ các bảng 4 và hình 7 và hình 8 cho thấy kết quả QA bằng phương pháp 3D tái tạo liều trên phần mềm 3DVH. Giá trị liều tới PTV và các cơ quan có sự phù hợp tốt giữa TPS và thực nghiệm, độ dốc của các đường gần bằng 1, biểu thị mối quan hệ tuyến tính giữa liều đo bằng phương pháp tái tạo và liều tính từ TPS. Theo thống kê trên 30 bênh nhân ung thư vòm bao gồm các ca điều trị tái phát cho thấy độ lệch trung bình nhỏ (<1%) trên cà 2 tiêu chí D95% và Dmean tới PTV, độ lệch chuẩn tương ứng là 0.71% và 0.71% với độ tin cậy <0.001. Gía trị liều lớn nhất (Dmax) tới cơ quan tủy sống và thân não có độ lệch trung bình rất nhỏ tương ứng là 0.85% và 0.33% giữa tính liều từ TPS và thực nghiệm. THẢO LUẬN Đảm bảo chất lượng cho kế hoạch xạ trị VMAT bằng các thiết bị đo liều đã được tìm hiểu từ khi VMAT ra đời. Tại Việt Nam kỹ thuật VMAT chỉ vừa mới được ứng dụng gần đây và nên các tìm hiểu về quá trình QA của kỹ thuật này chưa được phổ biến. Trong nghiên cứu này, chúng tôi đã thực hiện QA cho 30 kế hoạch xạ trị VMAT (vùng đầu cổ được chọn ngẫu nhiên bao gồm các ca điều trị tái phát) bằng 3 phương pháp 1D, 2D và 3D đối với máy TrueBeam-2 tại Bệnh viện Ung bướu Tp.HCM. Kết quả cho thấy sự phù hợp tốt của 3 phương pháp QA thực nghiệm so với liều tính toán từ thuật toán AAA trên Eclipse - TPS. Kết quả phương pháp đo liều điểm tại tâm của phantom QA - 1D (hình 3) cho thấy sự phù hợp tuyến tính giữa liều đo đạc liều đo bằng buồng ion hóa PTW 31010 tại tâm phantom ArcCHECK và liều tính toán từ Eclipse –TPS. Kết quả thống kê trong bảng 1 cho 30 kế hoạch điều trị VMAT có độ lệch trung bình giữa TPS và đo đạc bằng buồng ion hóa rất nhỏ (<1%), độ lệch chẩn <1.4% với độ tin cậy 0.001. Điều này phù hợp với kết quả trong nghiên cứu của Thiyagarajan và cộng sự [4], so sánh thực nghiệm sử dụng đầu dò IC-15 tại tâm ArcCHECK với tính toán liều từ Eclipse - TPS với sai khác là 0.5 ± 0.51%. Đối với phương pháp QA 2D, chúng tôi đã thực hiện đánh giá gamma với 2 tiêu chí 3%/3 mm và 2%/2 mm giữa thực nghiệm trên thiết bị EPID và ArcCHECK so với kết quả tính toán trên Eclipse – TPS sau đó so sánh kết quả của 2 phương pháp ArcCHECK và EPID. Chúng tôi thấy sự chêch lệch không đáng kể giữa 2 thiết bị ArcCHECK và EPID theo tiêu chí gamma 3%/3 mm. Đối với phương pháp 3D, phương pháp tái tạo liều 3D trên thiết bị ArcCHECK sử dụng phần mềm 3DVH với thuật toán tái tạo liều AC_PDP được thực hiện, đánh giá cụ thể 30 bệnh nhân ung thư vùng đầu cổ trên tiêu chí gamma 3%/3mm, 2%/2mm và liều trên từng cơ quan lành và bướu. Trên phần mềm tái tạo liều 3DVH, chỉ số gamma giữa liều tính Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 241 toán bằng thuật toán AAA trên Eclipse - TPS và tái tạo từ phần mềm 3DVH. Ngoài ra, các cơ quan như tủy sống, thân não và PTV từ hệ thống TPS được tác giả QA bằng phương pháp tái tạo liều trên phần mềm 3DVH có kết quả rất tốt, được biểu diễn bằng các đồ thị hình 7 và hình 8 với độ dốc gần bằng 1, cho thấy mối quan hệ tuyến tính giữa liều đo bằng phương pháp tái tạo và liều tính từ TPS là phù hợp. Kết quả QA bằng phương pháp 3D sử dụng phần mềm 3DVH trên thiết bị ArcCHECK là phù hợp với nghiên cứu Masahide Saito năm 2017[8]. KẾT LUẬN Kết quả của nghiên cứu này khẳng định kế hoạch VMAT cho ung thư vùng đầu cổ tại Bệnh viện ung bướu HCM đảm bảo chất lượng, an toàn trước khi điều trị cho bệnh nhân vì các sai khác liều điểm đều nhỏ hơn 5% và chỉ số gamma đều lớn hơn 90%. TÀI LIỆU THAM KHẢO 1. C X Yu, Physics in Medicine and Biology (1995), "Intensity-modulated arc therapy with dynamic multileaf collimation: an alternative to tomotherapy" 40(9), 1435 - 1449. 2. K Otto, Medical Physics (2007), “Volumetric modulated arc therapy: IMRT in a single gantry arc” 35(1), 310 - 317. 3. Website của tập đoàn ARC về các trung tâm xạ trị kỹ thuật cao VMAT tại Mỹ, https://advancedradiationcenters.com 4. R Thiyagarajan, A Nambiraj, S N Sinha, G Yadav, A Kumar, S Vikraman, and Kothandaraman, Reports of Practical Oncology and Radiotherapy (2016), "Analyzing the performance of ArcCHECK diode array detector for VMAT plan" 21(1), 50 - 56. 5. G Li, Y Zhang, X Jiang, S Bai, G Peng, K Wu, J Qingfeng, Physica medica (2013), "Evaluation of the ArcCHECK QA system for IMRT and VMAT verification" 29(3), 295 - 303. 6. Website của hãng Sun Nuclear, https://sunnuclear.com 7. D A Low, W B Harms, S Mutic, and J A Purdy, Medical Physics (1998), “A technique for the quantitative evaluation of dose distributions” 25 (5), 656 - 661. 8. M Saito, N Kadoya, K Sato, K Ito, S Dobashi, K Takeda, H Onishi, and K Jingu, Journal of Applied Clinical Medical Physics (2017), “Comparison of DVH-based plan verification methods for VMAT: ArcCHECK-3DVH system and dynalog-based dose reconstruction” 18(4), 206 - 214. Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 242 Tạp chí Ung thư học Việt Nam Số 5-2020-Tập 2 Journal of Oncology Viet Nam - Issue N5-2020-Vol 2 243 ABSTRACT Background: Quality assurance (QA) for VMAT are important and should be done before treatment that directly affects the the outcome of treatment for the patients. Aim: The purpose of this study is to presents t the quality assurance QA procedures and results for the Volumetric Modulated Arc Therapy (VMAT) plans at Ho Chi Minh City Oncology Hospital in VietNam for head and neck patients cancer. Materials and methods: 30 VMAT plans of head and neck cancer patients was seleted in this study. Each VMAT plan was planned on Eclipse 13.6 with 6 MV photon from the TrueBeam LINAC (Varian Medical Systems, Palo Alto, CA). QA were performed for all patients' VMAT plans using an ionization chamber (1D QA), EPID, ArcCHECK of Sunnuclear (2D QA) and 3DVH software (3D QA). Gamma index calculated by SNC software and 3DVH software was used to compare and evaluate dose difference between calculation and measurment. Results: The mean relative difference dose between the measured by the ionization chamber and calculated on the TPS was 0.88% (1D). The gamma percentage (3% / 3 mm) for all 30 patients using EPID and ArcCHECK were higher than 95% (2D). Gamma 3D index by dose reconstruction method on 3DVH software for PTV (both D95% and Dmean criteria) and organ were greater than 95% for all 30 patients. Conclusion: The results form the ionization chamber, EPID, ArcCHECK measurement and 3DVH calculation confirmed that the VMAT plan for head and neck cancer at HCM Oncology Hospital is good for treatmenting because the relative differences dose are smaller than 5% and the gamma index greater than 90%. Keywords: VMAT, ArcCHECK, QA 1D, QA 2D, QA 3D.
File đính kèm:
 dam_bao_chat_luong_ke_hoach_xa_tri_vmat_su_dung_phuong_phap.pdf
dam_bao_chat_luong_ke_hoach_xa_tri_vmat_su_dung_phuong_phap.pdf

