Thử nghiệm tạo biofloc từ nguồn vi sinh tự nhiên cho ương giống tôm thẻ chân trắng (litopenaeus vanamei boone, 1931) tại tỉnh Thừa Thiên Huế
Nghiên cứu này được thực hiện nhằm tìm hiểu khả năng hình thành biofloc để duy trì sự ổn
định của môi trường nước trong hệ thống ương giống tôm thẻ chân trắng. Một tổ hợp vi sinh phát triển
từ nguồn nước tự nhiên được sử dụng để so sánh với đối chứng có bổ sung chế phẩm vi sinh công
nghiệp. Thí nghiệm được tiến hành trong điều kiện hạn chế ánh sáng mặt trời trong 24 ngày, không có
sự trao đổi nước và có bổ sung rỉ mật hàng ngày để làm nguồn carbon (tỷ lệ C/N ở mức 15:1). Tổ hợp
biofloc hình thành đã kiểm soát lượng NH4+ và NO2– bằng quá trình đồng hóa dị dưỡng và nitrat hóa.
Trong suốt quá trình thí nghiệm, hàm lượng N–NH4 và N–NO2 của hệ thống biofloc được duy trì ở mức
an toàn đối với tôm con, lần lượt là 0,99 ± 0,02 mg·L–1 và 0,49 ± 0,08 mg·L–1. Ở mật độ nuôi 400 con·m–3,
khối lượng tôm tăng từ 0,01 đến 0,59 g·con–1 sau 24 ngày nuôi ở tất cả các bể với tỷ lệ sống đạt 82,5%

Trang 1

Trang 2

Trang 3
Trang 4
Trang 5

Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Thử nghiệm tạo biofloc từ nguồn vi sinh tự nhiên cho ương giống tôm thẻ chân trắng (litopenaeus vanamei boone, 1931) tại tỉnh Thừa Thiên Huế

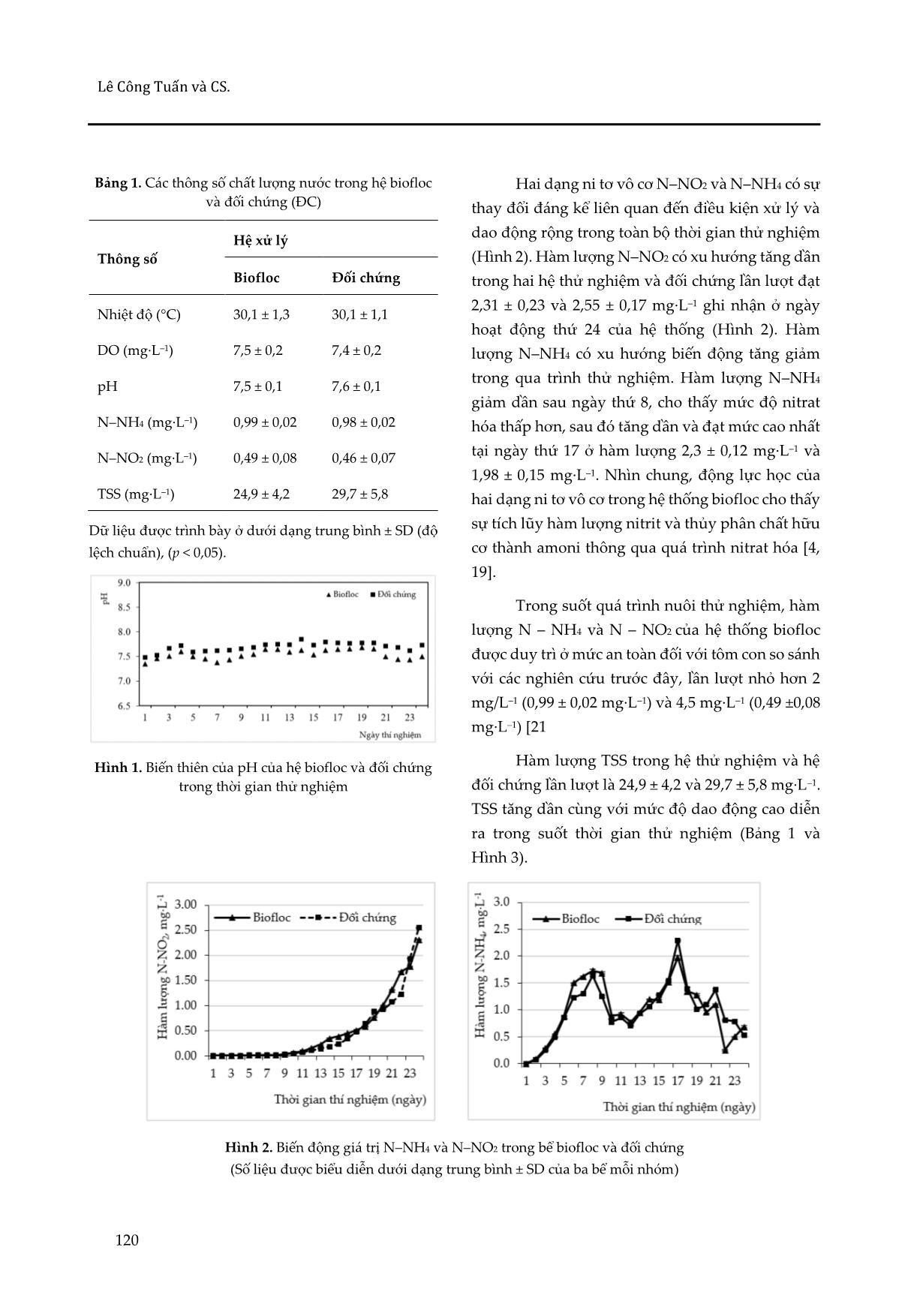
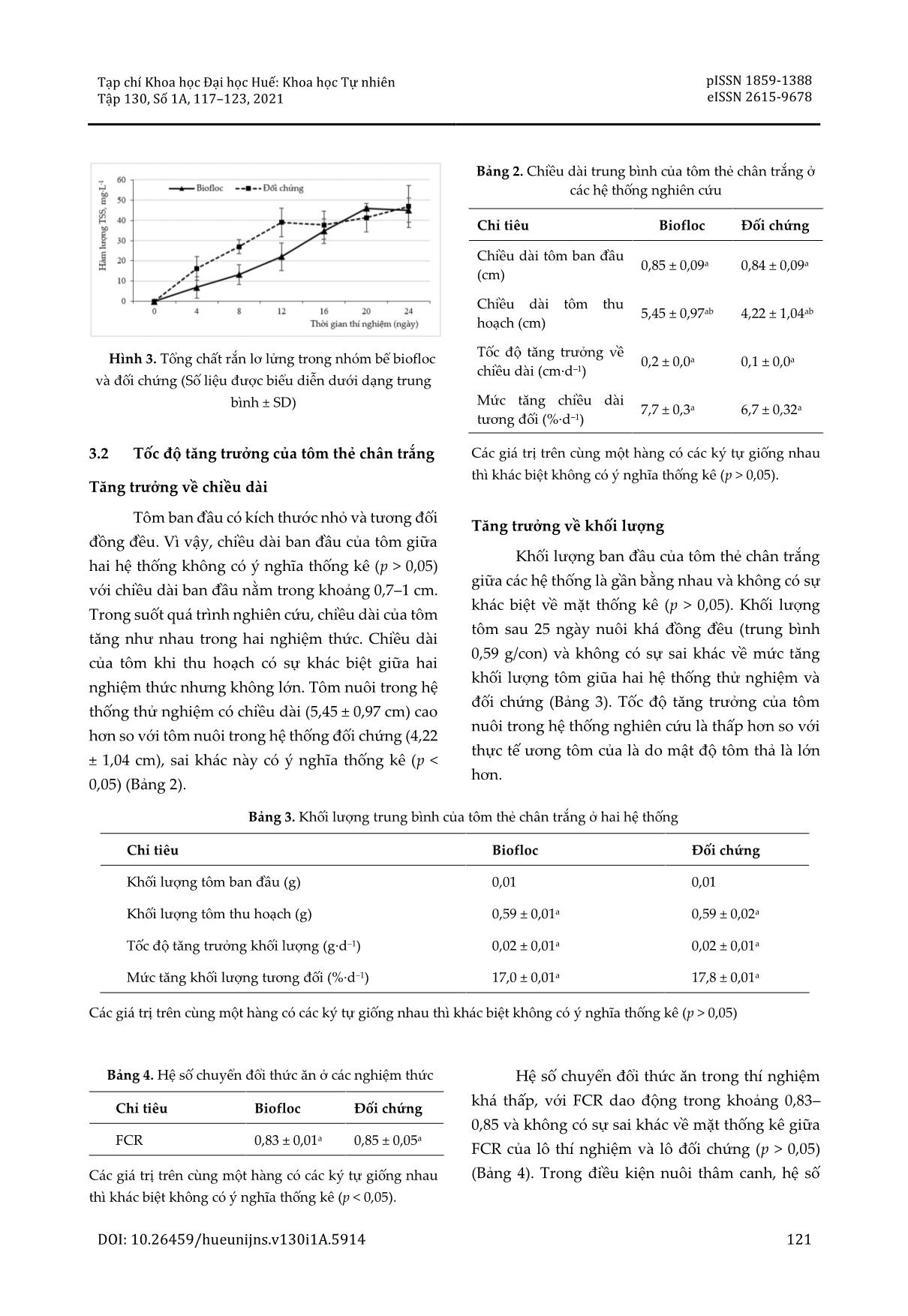
Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên Tập 130, Số 1A, 117–123, 2021 pISSN 1859-1388 eISSN 2615-9678 DOI: 10.26459/hueunijns.v130i1A.5914 117 THỬ NGHIỆM TẠO BIOFLOC TỪ NGUỒN VI SINH TỰ NHIÊN CHO ƯƠNG GIỐNG TÔM THẺ CHÂN TRẮNG (Litopenaeus vanamei Boone, 1931) TẠI TỈNH THỪA THIÊN HUẾ Lê Công Tuấn1, Tề Minh Sơn1, Đoàn Thị Mỹ Lành1, Nguyễn Hoàng Lộc2*, Nguyễn Đức Huy3 1 Khoa Môi trường, Trường Đại học Khoa học, Đại học Huế, 77 Nguyễn Huệ, Huế, Việt Nam 2 Khoa Sinh học, Trường Đại học Khoa học, Đại học Huế, 77 Nguyễn Huệ, Huế, Việt Nam 3 Viện Công nghệ sinh học, Đại học Huế, Quốc lộ 10, Phú Vang, Thừa Thiên Huế, Việt Nam * Tác giả liên hệ Nguyễn Hoàng Lộc (Ngày nhận bài: 13-07-2020; Ngày chấp nhận đăng: 02-10-2020) Tóm tắt. Nghiên cứu này được thực hiện nhằm tìm hiểu khả năng hình thành biofloc để duy trì sự ổn định của môi trường nước trong hệ thống ương giống tôm thẻ chân trắng. Một tổ hợp vi sinh phát triển từ nguồn nước tự nhiên được sử dụng để so sánh với đối chứng có bổ sung chế phẩm vi sinh công nghiệp. Thí nghiệm được tiến hành trong điều kiện hạn chế ánh sáng mặt trời trong 24 ngày, không có sự trao đổi nước và có bổ sung rỉ mật hàng ngày để làm nguồn carbon (tỷ lệ C/N ở mức 15:1). Tổ hợp biofloc hình thành đã kiểm soát lượng NH4+ và NO2– bằng quá trình đồng hóa dị dưỡng và nitrat hóa. Trong suốt quá trình thí nghiệm, hàm lượng N–NH4 và N–NO2 của hệ thống biofloc được duy trì ở mức an toàn đối với tôm con, lần lượt là 0,99 ± 0,02 mg·L–1 và 0,49 ± 0,08 mg·L–1. Ở mật độ nuôi 400 con·m–3, khối lượng tôm tăng từ 0,01 đến 0,59 g·con–1 sau 24 ngày nuôi ở tất cả các bể với tỷ lệ sống đạt 82,5%. Từ khóa: biofloc, tôm thẻ chân trắng, ương giống, vi sinh tự nhiên Evaluation of biofloc from saltwater bacteria community for white-leg shrimp (Litopenaeus vanamei Boone, 1931) culture in Thua Thien Hue Le Cong Tuan1, Te Minh Son1, Doan Thi My Lanh1, Nguyen Hoang Loc2*, Nguyen Duc Huy3 1 Department of Environmental Science, University of Sciences, Hue University, 77 Nguyen Hue St., Hue Vietnam 2 Department of Biology, University of Sciences, Hue University, 77 Nguyen Hue St., Hue, Vietnam 3I nstitute of Biotechnology, Hue University, Rd. 10, Phu Vang, Thua Thien Hue, Vietnam * Correspondence to Nguyen Hoang Loc (Received: 13 July 2020; Accepted: 02 October 2020) Abstract. This study was conducted to investigate the formation of biofloc in maintaining the stability of the water quality in the white-leg shrimp nursery system. A treatment unit using microorganisms from natural water was conducted to compare with a control supplemented with commercial probiotics. The experiment was conducted under the conditions of limited sunlight for 24 days without water exchange and with daily molasses addition as a carbon source (the C/N ratio is 15:1). The resulting biofloc complex could control the increase of NH4+ and NO2– via heterotrophic assimilation and nitrification. During the experiments, the N–NH4 and N–NO2 concentrations of the biofloc system maintain a safe range for the juveniles at 0.99 ± 0,02 and 0.49 ± 0.08 mg·L–1, respectively. At the culture density of 400 Lê Công Tuấn và CS. 118 shrimp·m–3, the shrimp weight increases from 0.01 g to 0.59 g per shrimp on the 24th day of culture for all culture tanks with a survival rate of 82.5%. Keywords: biofloc, shrimp nursery, saltwater bacteria, white-leg shrimp 1 Giới thiệu Một trong những công nghệ có tiềm năng tạo ra sản lượng cao từ nuôi trồng thủy hải sản, đồng thời đảm bảo sự bền vững về mặt môi trường, kinh tế và xã hội là công nghệ biofloc [1, 2]. Biofloc là kỹ thuật huyền phù và được phát triển trong những năm 80 của thế kỷ XX. Công nghệ này dựa trên việc duy trì các nhóm vi khuẩn trong huyền phù ở mật độ cao bằng cách cung cấp không khí liên tục [3]. Quá trình cung cấp không khí liên tục cho quá trình phân hủy hiếu khí các chất hữu cơ, thức ăn thừa, phân tôm, v.v. trong ao nuôi đi kèm sự phát triển của quần thể vi sinh vật dị dưỡng đa dạng và lơ lửng [4]. Quần thể vi sinh vật dị dưỡng giúp kiểm soát chất lượng nước, đồng thời là nguồn thức ăn giàu protein cho tôm và có thể đóng vai trò như một biện pháp thay thế để kiểm soát mầm bệnh [5, 6]. Về mặt lý thuyết, hệ thống vận hành thông qua việc bổ sung nguồn carbon để tăng tỷ lệ C/N, từ đó, tăng cường chuyển đổi ni tơ vô cơ thành sinh khối của vi sinh vật [4]. Các vi sinh vật sử dụng carbohydrate làm nguồn năng lượng để tạo ra các tế bào mới và ni tơ được sử dụng để tổng hợp protein, đây cũng là yếu tố chính trong sự hình thành các tế bào mới [4]. Do đó, bản chất của công nghệ biofloc là một quá trình vi sinh vật cơ bản, sử dụng carbohydrate đi kèm với việc cố định ni tơ vô cơ [4]. Tỷ lệ C/N cao (10–20) được khuyến nghị sử dụng để phát triển biofloc và loại bỏ ammoni hiệu quả [5, 6]. Điều này có thể đạt được bằng cách thêm các nguồn carbon khác nhau có sẵn tại địa phương (rỉ mật, đường mía, v.v.) và sử dụng thức ăn có hàm lượng ni tơ thấp [4, 5]. Lợi ích của công nghệ biofloc so với các phương thức truyền thống về mặt hiệu quả sử dụng và chất lượng nước cho nuôi đã được chứng minh thành công trong nuôi tôm [4, 7-9] và ở một mức độ nào đó trong nuôi cá [10, 11]. Tuy nhiên, hiện nay việc ứng dụng công nghệ biofloc vào nuôi tôm thẻ chân trắng ở Việt Nam đang gặp khó khăn từ nhiều nguyên nhân khác nhau, trong đó nguyên nhân về chất lượng chế phẩm vi sinh đang sử dụng trong công nghệ nuôi được nhiều người quan tâm. Đã có một số nghiên cứu trên thế giới và ở Việt Nam nhằm khai thác và sử dụng tài nguyên vi sinh vật bản địa để ứng dụng vào trong công nghệ biofloc vì vi sinh vật bản địa thích nghi với điều kiện môi trường, khí hậu, hiệu quả xử lý cao hơn và giúp tiết kiệm chi phí [12-14]. Do đó, để đánh giá khả năng thích nghi của công nghệ mới này trong giai đoạn đầu nuôi tôm tại tỉnh Thừa Thiên Huế, chúng tôi ... thu hoạch từ mỗi bể, xác định khối lượng và chiều dài cơ thể. Các thông số tăng trưởng được tính theo các phương trình (1–5) SR (%) = 100 × (số lượng tôm cuối cùng/số lượng tôm ban đầu) (1) WG (%) = (W2 – W1)/W1 × 100 (2) DGR-W (g·d–1) = (W2 – W1)/N (3) LG (%) = ((L2 – L1)/ L1 × 100 (4) DGR-L (cm.d–1) = (L2 – L1)/N (5) Hệ số chuyển đổi thức ăn (FCR) = Khối lượng thức ăn sử dụng/Mức tăng khối lượng tôm trong đó W1 là khối lượng tôm ban đầu (g); W2 là khối lượng tôm sau khi kết thúc thí nghiệm (g); L1 là chiều dài tôm ban đầu (cm); L2 là chiều dài tôm sau thu mẫu (cm); N là thời gian thí nghiệm (ngày); SR là tỉ lệ sống; DGR-W là tốc độ tăng khối lượng; WG là mức tăng khối lượng tương đối; DGR-L là tốc độ tăng chiều dài; LG là mức tăng chiều dài tương đối. 2.4 Phân tích thống kê Dữ liệu được phân tích bằng phần mềm thống kê IBM SPSS v. 20, Microsoft office Excel 2019. Sự thay đổi về hàm lượng chất dinh dưỡng và tổng chất rắn lơ lửng sẽ được đánh giá bằng phân tích phương sai với mức xác suất 95%. 3 Kết quả và thảo luận 3.1 Đánh giá biến động chất lượng nước Trong hệ thử nghiệm, nhiệt độ nước (30,1 ± 1,3 °C), DO (7,5 ± 0,2 mg·L–1) và pH (7,5 ± 0,1) đều nằm trong giới hạn chấp nhận đối với nuôi tôm thẻ chân trắng vùng nhiệt đới [21] và cũng ghi nhận các giá trị tương đương của nhiệt độ (30,1 ± 1,1 °C), DO (7,4 ± 0,2 mg·L–1) và pH (7,6 ± 0,1) cũng nằm trong bể đối chứng (Bảng 1). Do quá trình sục khí liên tục nên DO luôn ở mức cao trong cả hai nhóm bể thử nghiệm và đối chứng và cũng là kết quả của quá trình nitrat hóa, kết hợp với quá trình cố định ni tơ thông qua con đường dị dưỡng để sản xuất vi sinh vật chưa phổ biến trong giai đoạn đầu phát triển của tôm [16]. Giá trị pH thường liên quan khi có quá trình nitrat hóa trong hệ thống dựa trên tổ hợp biofloc [16-18]. Tuy nhiên, pH vẫn gần như ổn định trong suốt thời gian thử nghiệm (Hình 1). Lê Công Tuấn và CS. 120 Bảng 1. Các thông số chất lượng nước trong hệ biofloc và đối chứng (ĐC) Thông số Hệ xử lý Biofloc Đối chứng Nhiệt độ (°C) 30,1 ± 1,3 30,1 ± 1,1 DO (mg·L–1) 7,5 ± 0,2 7,4 ± 0,2 pH 7,5 ± 0,1 7,6 ± 0,1 N–NH4 (mg·L–1) 0,99 ± 0,02 0,98 ± 0,02 N–NO2 (mg·L–1) 0,49 ± 0,08 0,46 ± 0,07 TSS (mg·L–1) 24,9 ± 4,2 29,7 ± 5,8 Dữ liệu được trình bày ở dưới dạng trung bình ± SD (độ lệch chuẩn), (p < 0,05). Hình 1. Biến thiên của pH của hệ biofloc và đối chứng trong thời gian thử nghiệm Hai dạng ni tơ vô cơ N–NO2 và N–NH4 có sự thay đổi đáng kể liên quan đến điều kiện xử lý và dao động rộng trong toàn bộ thời gian thử nghiệm (Hình 2). Hàm lượng N–NO2 có xu hướng tăng dần trong hai hệ thử nghiệm và đối chứng lần lượt đạt 2,31 ± 0,23 và 2,55 ± 0,17 mg·L–1 ghi nhận ở ngày hoạt động thứ 24 của hệ thống (Hình 2). Hàm lượng N–NH4 có xu hướng biến động tăng giảm trong qua trình thử nghiệm. Hàm lượng N–NH4 giảm dần sau ngày thứ 8, cho thấy mức độ nitrat hóa thấp hơn, sau đó tăng dần và đạt mức cao nhất tại ngày thứ 17 ở hàm lượng 2,3 ± 0,12 mg·L–1 và 1,98 ± 0,15 mg·L–1. Nhìn chung, động lực học của hai dạng ni tơ vô cơ trong hệ thống biofloc cho thấy sự tích lũy hàm lượng nitrit và thủy phân chất hữu cơ thành amoni thông qua quá trình nitrat hóa [4, 19]. Trong suốt quá trình nuôi thử nghiệm, hàm lượng N – NH4 và N – NO2 của hệ thống biofloc được duy trì ở mức an toàn đối với tôm con so sánh với các nghiên cứu trước đây, lần lượt nhỏ hơn 2 mg/L–1 (0,99 ± 0,02 mg·L–1) và 4,5 mg·L–1 (0,49 ±0,08 mg·L–1) [21 Hàm lượng TSS trong hệ thử nghiệm và hệ đối chứng lần lượt là 24,9 ± 4,2 và 29,7 ± 5,8 mg·L–1. TSS tăng dần cùng với mức độ dao động cao diễn ra trong suốt thời gian thử nghiệm (Bảng 1 và Hình 3). Hình 2. Biến động giá trị N–NH4 và N–NO2 trong bể biofloc và đối chứng (Số liệu được biểu diễn dưới dạng trung bình ± SD của ba bể mỗi nhóm) Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên Tập 130, Số 1A, 117–123, 2021 pISSN 1859-1388 eISSN 2615-9678 DOI: 10.26459/hueunijns.v130i1A.5914 121 Hình 3. Tổng chất rắn lơ lửng trong nhóm bể biofloc và đối chứng (Số liệu được biểu diễn dưới dạng trung bình ± SD) 3.2 Tốc độ tăng trưởng của tôm thẻ chân trắng Tăng trưởng về chiều dài Tôm ban đầu có kích thước nhỏ và tương đối đồng đều. Vì vậy, chiều dài ban đầu của tôm giữa hai hệ thống không có ý nghĩa thống kê (p > 0,05) với chiều dài ban đầu nằm trong khoảng 0,7–1 cm. Trong suốt quá trình nghiên cứu, chiều dài của tôm tăng như nhau trong hai nghiệm thức. Chiều dài của tôm khi thu hoạch có sự khác biệt giữa hai nghiệm thức nhưng không lớn. Tôm nuôi trong hệ thống thử nghiệm có chiều dài (5,45 ± 0,97 cm) cao hơn so với tôm nuôi trong hệ thống đối chứng (4,22 ± 1,04 cm), sai khác này có ý nghĩa thống kê (p < 0,05) (Bảng 2). Bảng 2. Chiều dài trung bình của tôm thẻ chân trắng ở các hệ thống nghiên cứu Chỉ tiêu Biofloc Đối chứng Chiều dài tôm ban đầu (cm) 0,85 ± 0,09a 0,84 ± 0,09a Chiều dài tôm thu hoạch (cm) 5,45 ± 0,97ab 4,22 ± 1,04ab Tốc độ tăng trưởng về chiều dài (cm·d–1) 0,2 ± 0,0a 0,1 ± 0,0a Mức tăng chiều dài tương đối (%·d–1) 7,7 ± 0,3a 6,7 ± 0,32a Các giá trị trên cùng một hàng có các ký tự giống nhau thì khác biệt không có ý nghĩa thống kê (p > 0,05). Tăng trưởng về khối lượng Khối lượng ban đầu của tôm thẻ chân trắng giữa các hệ thống là gần bằng nhau và không có sự khác biệt về mặt thống kê (p > 0,05). Khối lượng tôm sau 25 ngày nuôi khá đồng đều (trung bình 0,59 g/con) và không có sự sai khác về mức tăng khối lượng tôm giũa hai hệ thống thử nghiệm và đối chứng (Bảng 3). Tốc độ tăng trưởng của tôm nuôi trong hệ thống nghiên cứu là thấp hơn so với thực tế ương tôm của là do mật độ tôm thả là lớn hơn. Bảng 3. Khối lượng trung bình của tôm thẻ chân trắng ở hai hệ thống Chỉ tiêu Biofloc Đối chứng Khối lượng tôm ban đầu (g) 0,01 0,01 Khối lượng tôm thu hoạch (g) 0,59 ± 0,01a 0,59 ± 0,02a Tốc độ tăng trưởng khối lượng (g·d–1) 0,02 ± 0,01a 0,02 ± 0,01a Mức tăng khối lượng tương đối (%·d–1) 17,0 ± 0,01a 17,8 ± 0,01a Các giá trị trên cùng một hàng có các ký tự giống nhau thì khác biệt không có ý nghĩa thống kê (p > 0,05) Bảng 4. Hệ số chuyển đổi thức ăn ở các nghiệm thức Chỉ tiêu Biofloc Đối chứng FCR 0,83 ± 0,01a 0,85 ± 0,05a Các giá trị trên cùng một hàng có các ký tự giống nhau thì khác biệt không có ý nghĩa thống kê (p < 0,05). Hệ số chuyển đổi thức ăn trong thí nghiệm khá thấp, với FCR dao động trong khoảng 0,83– 0,85 và không có sự sai khác về mặt thống kê giữa FCR của lô thí nghiệm và lô đối chứng (p > 0,05) (Bảng 4). Trong điều kiện nuôi thâm canh, hệ số Lê Công Tuấn và CS. 122 chuyển hóa thức ăn của tôm thẻ chân trắng dao động từ 1,1 đến 1,3 [20]. Như vậy, lượng thức ăn sử dụng trong nghiên cứu nuôi tôm bằng công nghệ biofloc này là thấp hơn so với việc nuôi tôm thông thường. Điều này cho thấy tổ hợp biofloc đã có vai trò cung cấp một lượng thức ăn bổ sung cho tôm [5, 6] Tỷ lệ sống của tôm thẻ chân trắng Tỷ lệ sống của tôm sau 24 ngày nuôi ở cả hai hệ thống là gần bằng nhau và không có sai khác về mặt thống kê (p > 0,05). Tỉ lệ sống trung bình của tôm trong hệ biofloc là 82,5 ± 2,5% và trong hệ đối chứng là 82,8 ± 3,01% (Bảng 5). So sánh với nghiên cứu Tạ Văn Phương và cs. [13], nuôi tôm thẻ chân trắng theo công nghệ biofloc trong vòng 60 ngày thì tỷ lệ sống của tôm đạt 75,0–97,3% với mật độ thả 150 con·m–3. Theo Xu và cs. [9], ương tôm thẻ chân trắng theo công nghệ biofloc với tỉ lệ C/N từ 12:1 đến 15:1, với mật độ thả 600 con.m–3 thì sau 6 tuần tỷ lệ sống là trên 95,5% và không có sự khác biệt giữa các hệ bể. Không có sự khác biệt có ý nghĩa thống kê (p > 0,05) về tỷ lệ sống của tôm thẻ chân trắng giữa hệ thống thử nghiệm (82,5 ± 2,5%) và đối chứng (82,8 ± 3,01%). Đồng thời, mức tăng trọng của tôm nuôi trong hệ thống thử nghiệm (117%) không có sự khác biệt đáng kể (p > 0,05) so với tôm nuôi trong hệ thống đối chứng (117,8%). Tương tự, tốc độ tăng trưởng theo ngày cũng không có sự khác biệt giữa hai hệ thống (p > 0,05), đều là 0,02 g·d–1. Tỷ lệ sống và tăng trưởng cao của tôm thẻ chân trắng cho thấy sự đóng góp đáng kể của hệ biofloc tự nhiên trong việc hỗ trợ sinh trưởng của tôm. Bảng 5. Tỷ lệ sống của tôm ở hai hệ thống thử nghiệm và đối chứng Chỉ tiêu Biofloc Đối chứng Tỷ lệ sống (%) 82,5 ± 2,5a 82,8 ± 3,01a Các giá trị trên cùng một hàng có các ký tự giống nhau thì khác biệt không có ý nghĩa thống kê (p < 0,05). 4 Kết luận Kết quả của nghiên cứu này cho thấy rằng trong giai đoạn đầu của nuôi tôm thẻ chân trắng, việc bổ sung các chế phẩm vi sinh để cải thiện chất lượng nguồn nước là chưa cần thiết. (1) Trong tháng đầu tiên của nuôi tôm thẻ chân trắng, các thông số cơ bản của môi trường nước nuôi như pH, DO, nhiệt độ của hai hệ thống biofloc tự nhiên (thí nghiệm) và có bổ sung chế phẩm vi sinh công nghiệp (ĐC) không có sự khác biệt (p < 0,05). (2) Trong suốt quá trình nuôi thí nghiệm, hàm lượng N – NH4 và N – NO2 của hệ thống thí nghiệm được duy trì ở mức an toàn đối với tôm giống, lần lượt nhỏ hơn 2 mg/L–1 (0,99 ± 0,02 mg·L–1) và 4,5 mg·L–1 (0,49 ±0,08 mg·L–1) (3) Với mật độ độ nuôi 400 con·m–3, khối lượng tôm ban đầu là 0,01 g·con–1 ở tất cả các bể của lô thí nghiệm và lô đối chứng, sau 25 ngày nuôi cho thấy sự tăng trưởng về khối lượng lên đến 0,59 g·con–1 với tỷ lệ sống đạt 82,5%. Thông tin tài trợ Nghiên cứu này được thực hiện với sự tài trợ của Bộ Giáo dục và Đào tạo Việt Nam thông qua đề tài Khoa học và công nghệ mã số B2019-DHH- 08. Tài liệu tham khảo 1. De Schryver P, Crab R, Defoirdt T, Boon N, Verstraete W. The basics of bio-flocs technology: The added value for aquaculture. Aquaculture. 2008;277(3-4):125-137. 2. Crab R, Defoirdt T, Bossier P, Verstraete W. Biofloc technology in aquaculture: Beneficial effects and future challenges. Aquaculture. 2012;356-357:351- 356. 3. Avnimelech Y, Weber B, Hepher B, Milstein A, Zorn M. Studies in circulated fish ponds: organic matter Tạp chí Khoa học Đại học Huế: Khoa học Tự nhiên Tập 130, Số 1A, 117–123, 2021 pISSN 1859-1388 eISSN 2615-9678 DOI: 10.26459/hueunijns.v130i1A.5914 123 recycling and nitrogen transformation. Aquaculture Research. 1986;17(4):231-242. 4. Avnimelech Y. Carbon/nitrogen ratio as a control element in aquacultures systems. Aquaculture. 1999;176:227-235. 5. Hargreaves JA. Photosynthetic suspended-growth systems in aquaculture. Aquacultural Engineering. 2006;34(3):344-363. 6. Crab R, Avnimelech Y, Defoirdt T, Bossier P, Verstraete W. Nitrogen removal techniques in aquaculture for a sustainable production. Aquaculture. 2007;270(1-4):1-14. 7. Burford MA, Thompson PJ, McIntosh RP, Bauman RH, Pearson DC. Nutrient and microbial dynamics in high-intensity, zero-exchange shrimp ponds in Belize. Aquaculture. 2003;219(1-4):393-411. 8. Zhao P, Huang J, Wang X, Song X, Yang C, Zhang X, et al. The application of bioflocs technology in high‐ intensive, zero exchange farming systems of Marsupenaeus japonicus. Aquaculture. 2012;354- 355:97-106. 9. Xu W, Morris TC, Samocha TM. Effects of C/N on biofloc development, water quality and performance of Litopenaeus vannamei juveniles in a biofloc-based, high-density, zezo exchange, outdoor tank system. Aquaculture. 2016;453:169-175. 10. Pérez-Fuentes JA, Hernández-Vergara MP, Pérez- Rostro CI, Fogel I. C:N ratios affect nitrogen and production of Nile tilapia Oreochromis niloticus raised in a biofloc system under high density cultivation. Aquaculture. 2016;452:247-251. 11. Việt LQ. Ứng dụng biofloc nuôi tôm thẻ chân trắng (Litopenaeus vannamei) với mật độ khác nhau kết hợp với cá rô phi (Oreochromis niloticus). Tạp chí khoa học Trường Đại học Cần Thơ, Phần B: Nông nghiệp, Thủy sản và Công nghệ sinh học. 2015;38:44- 52. 12. Hiền NTT, Huấn NV. Nghiên cứu ứng dụng công nghệ Biofloc trong nuôi thâm canh tôm thẻ chân trắng Penaeus (Litopenaeus vannamei) quy mô sản xuất. Bản tin viện nghiên cứu nuôi trồng thủy sản. 2013;13-15. 13. Phương TV. Nghiên cứu nuôi tôm thẻ chân trắng theo quy trình biofloc với mật độ và độ mặn khác nhau. Tạp chí khoa học Trường Đại học Cần Thơ, Số chuyên đề: Thủy sản. 2014;2:44-53. 14. Nhung VTN. Nghiên cứu một số nguồn Carbonhydrate tạo biofloc để nuôi tôm thẻ chân trắng (Litopenaeus vannamei). Tạp chí khoa học Trường Đại học sư phạm thành phố Hồ Chí Minh. 2017;14:149 -160. 15. Rice EW, Baird RB, Eaton AD. Standard methods for the examination of water and wastewater. 23rd Edition. Washington, DC (US): American Public Health Association (APHA); 2017. 1796 p. 16. Azim M, Little D. The biofloc (BFT) indoor tanks: Water quality, biofloc composition and growth and welfare of Nile tilapia (Oreochromis niloticus). Aquaculture. 2008;283(1-4):29-35. 17. Azim M, Little D, Bron J. Microbial protein production in activated suspension tanks manipulating C:N ratio in feed and the implications for fish culture. Bioresource Technology. 2008;99(9):3590-3599. 18. Da Silva KR, Wasielesky W, Abreu PC. Nitrogen and phosphorus dynamic in the biofloc production of the Pacific White Shirmp, Litopenaeus vannamei. Journal of the World Aquaculture Society. 2013;44(1):30-41. 19. Burford MA, Thompson PJ, McIntosh RP, Bauman RH, Pearson DC. The contribution of flocculated material to shirmp (Litopenaeus vannamei) nutrition in a high-intensity zero-exchange system. Aquaculture. 2004;232(1-4):525-537. 20. Avnimelech Y. Feeding with microbial flocs by tilapia in minimal discharge bio-flocs technology ponds. Aquaculture. 2007;264(1-4):140-147. 21. Chen J, Chin T. Accute oxicty of nitritee to tiger prawn, Penaeus monodon, larvae. Aquaculture. 1988;69(3-4):253-262.
File đính kèm:
 thu_nghiem_tao_biofloc_tu_nguon_vi_sinh_tu_nhien_cho_uong_gi.pdf
thu_nghiem_tao_biofloc_tu_nguon_vi_sinh_tu_nhien_cho_uong_gi.pdf

