Phân hủy phenol trong môi trường nước bằng quá trình nội điện phân trên vật liệu Fe-Cu
Fe-Cu materials are preprared by chemical plating method from Fe powder and solution CuSO4 5%,
then determine the characteristics of surface morphology, structure, composition by Scanning electron
microscopy (SEM), X-ray diffraction (XRD), Energy Dispersive X-ray Spectroscopy (EDX). Materials
Fe-Cu is used removal of phenol from aqueous solution by internal microelectrolysis. The results show
that with optimal conditions for phenol decomposition is pH of 3, contact time of 12 hourss, material
weight of 1.0 g, shaking rate of 200 revolutions per minute (rpm), phenol removal efficiency is 92.7%.,
with the initial concentration is 100.98 mg/L. The results show that materials Fe-Cu can be applied to
remove phenol from aqueous solution by internal microelectrolysis

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5

Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Phân hủy phenol trong môi trường nước bằng quá trình nội điện phân trên vật liệu Fe-Cu

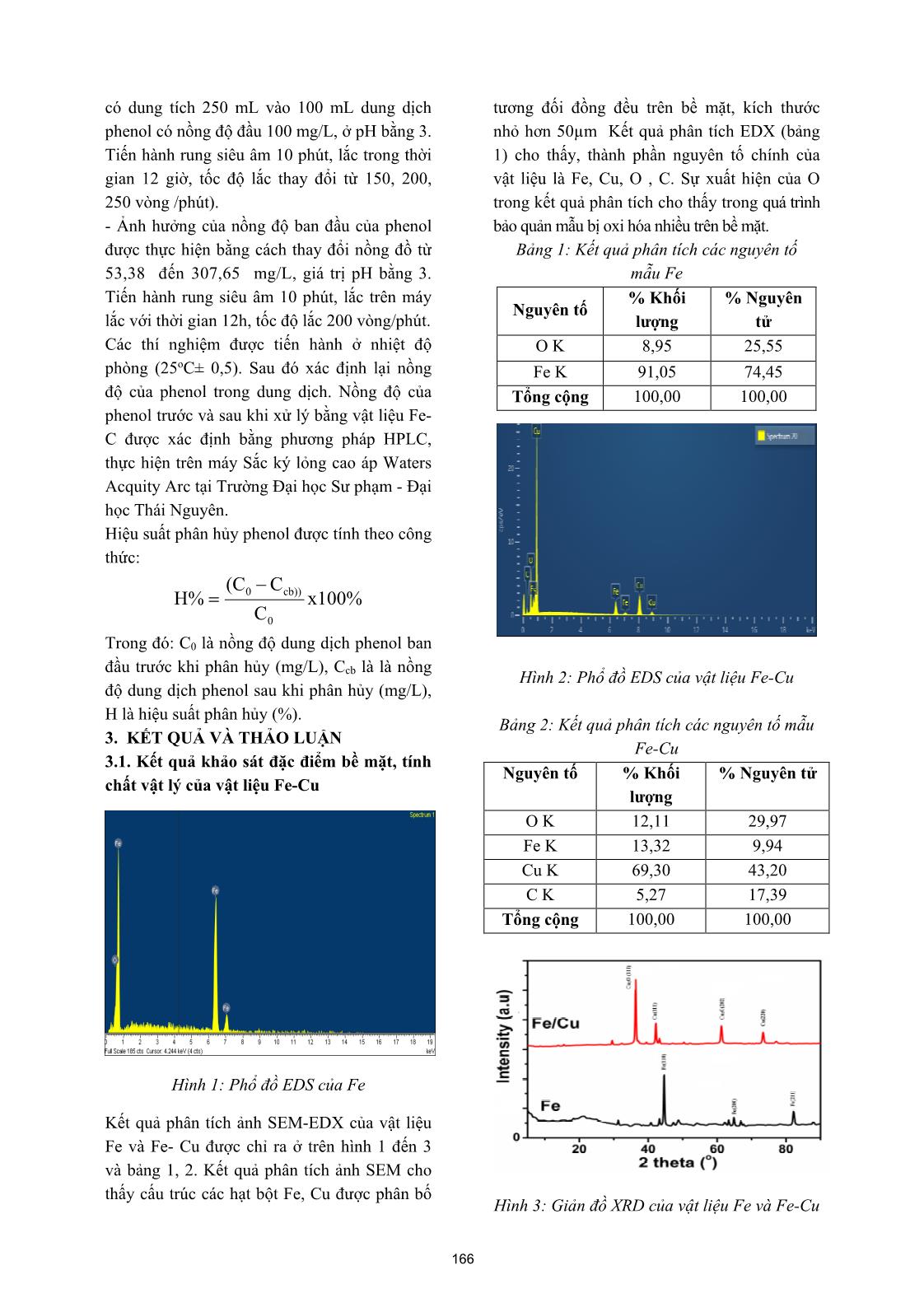
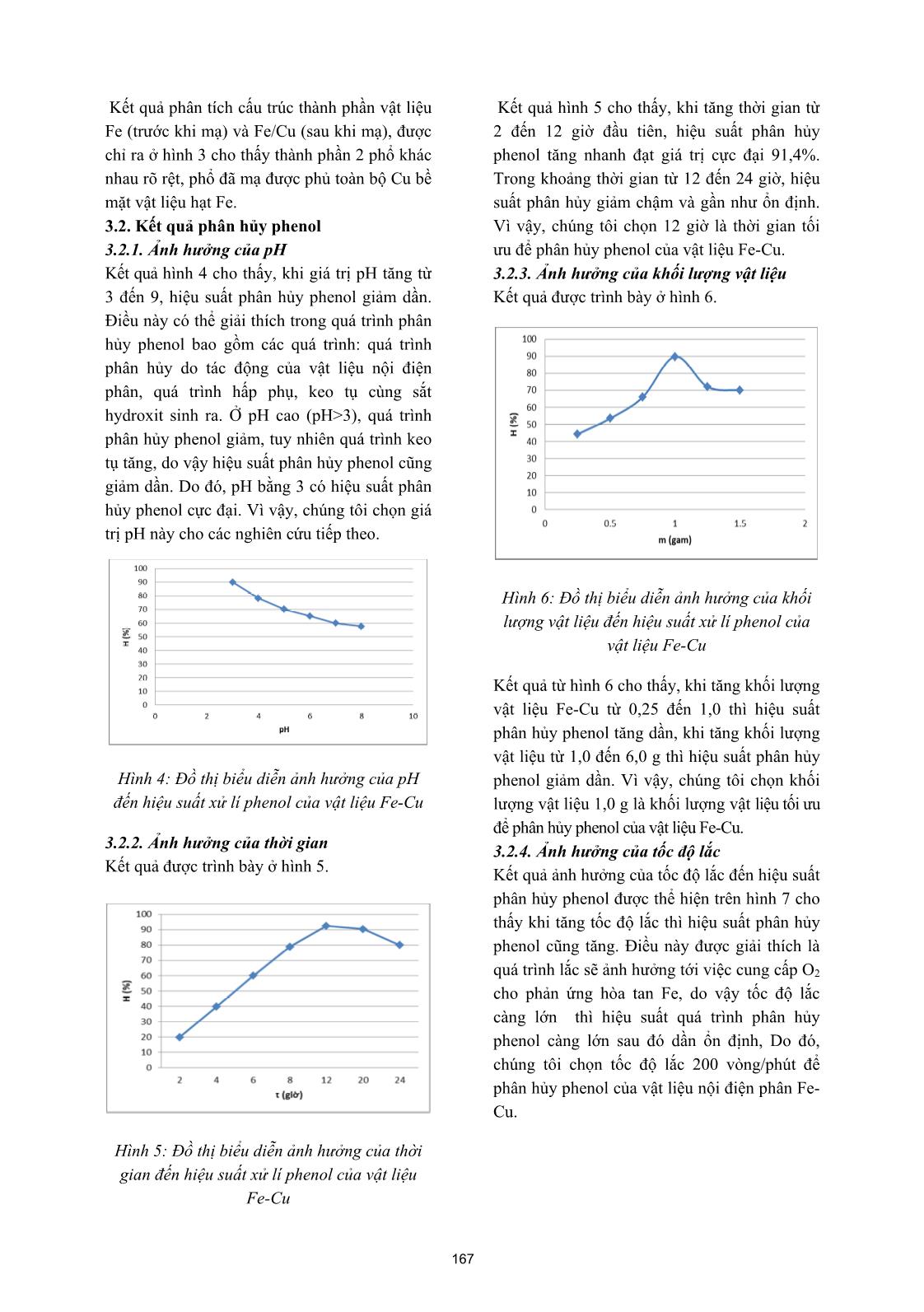
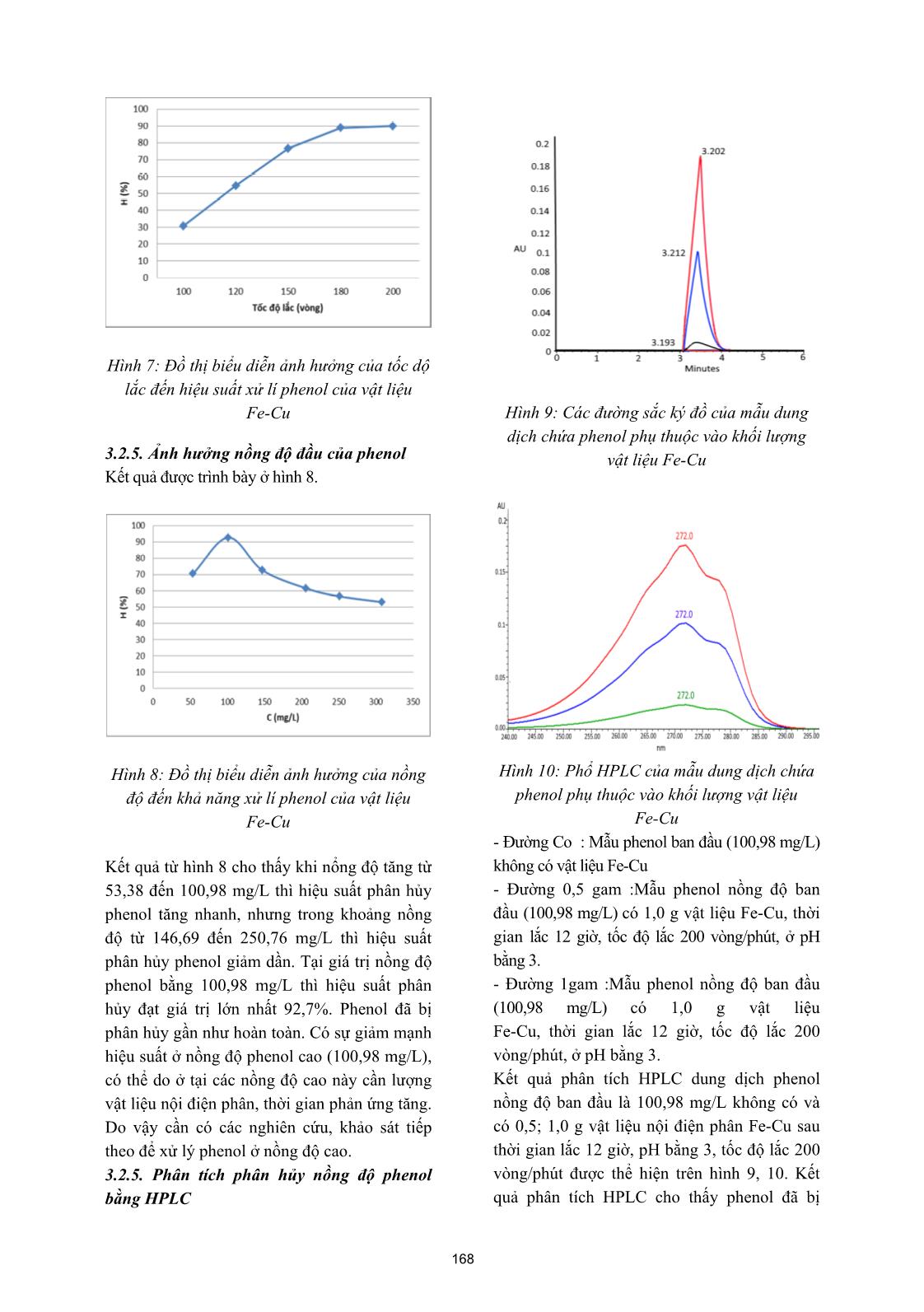
Tạp chí phân tích Hóa, Lý và Sinh học - Tập 25, Số 2/2020 PHÂN HỦY PHENOL TRONG MÔI TRƯỜNG NƯỚC BẰNG QUÁ TRÌNH NỘI ĐIỆN PHÂN TRÊN VẬT LIỆU Fe-Cu Đến tòa soạn 20-11-2019 Đỗ Trà Hương, Đào Mai Giang Trường Đại học Sư phạm - Đại học Thái Nguyên Nguyễn Văn Tú Viện Hóa học - Vật liệu, Viện Khoa học và Công nghệ Quân sự Nguyễn Anh Tiến Trường Đại học Sư phạm Thành phố Hồ Chí Minh SUMMARY REMOVAL OF PHENOL FROM AQUEOUS SOLUTIONS BY INTERNAL MICROELECTROLYSIS ON THE Fe-Cu MATERIALS Fe-Cu materials are preprared by chemical plating method from Fe powder and solution CuSO4 5%, then determine the characteristics of surface morphology, structure, composition by Scanning electron microscopy (SEM), X-ray diffraction (XRD), Energy Dispersive X-ray Spectroscopy (EDX). Materials Fe-Cu is used removal of phenol from aqueous solution by internal microelectrolysis. The results show that with optimal conditions for phenol decomposition is pH of 3, contact time of 12 hourss, material weight of 1.0 g, shaking rate of 200 revolutions per minute (rpm), phenol removal efficiency is 92.7%., with the initial concentration is 100.98 mg/L. The results show that materials Fe-Cu can be applied to remove phenol from aqueous solution by internal microelectrolysis. Keywords. Internal microelectrolysis, Fe-Cu material, Phenol, Aqueous solution, Removal. 1. MỞ ĐẦU Trong những năm qua, quá trình công nghiệp hóa, hiện đại hóa ở Việt Nam diễn ra mạnh mẽ, thúc đẩy phát triển kinh tế xã hội của đất nước, kèm theo đó là các vấn đề về ô nhiễm môi trường. Phenol là chất ô nhiễm độc hại và được liệt kê vào 129 chất ô nhiễm cần được tiền xử lý theo hướng dẫn của Cục Bảo vệ Môi trường Mỹ. Phenol thường phát sinh ra trong các dòng thải của các ngành công nghiệp như: hóa dầu, lọc dầu, sản xuất nhựa, ngành thép, dệt nhuộm, giấy và bột giấy, thuốc trừ sâu, dược phẩm, tổng hợp nhựa, nước thải của quá trình luyện cốc [1-3]. Phenol có thể gây ung thư đột biến gen, quái thai và là một hóa chất ít bị phân hủy sinh học. Phenol làm nhiễm độc nguồn nước, gây nguy hại cho con người và sinh vật, do đó ô nhiễm phenol trong nước thải đang được quan tâm nghiên cứu ở nhiều quốc gia, trong đó có Việt Nam. Để xử lý phenol, các phương pháp xử lý truyền thống đa được áp dụng như phương pháp hóa lý (hấp phụ, keo tụ, lắng) đã được áp dụng nhưng không hiệu quả cao và nước thải sau xử lý cho đạt tiêu chuẩn xả thải [4-6]. Nguyên lý của phương pháp nội điện phân: Hai vật liệu có thế điện cực khác nhau, khi tiếp xúc tạo thành cặp vi điện cực, đối với hệ Fe-C, Fe- Cu sắt đóng vai trò anot, đồng hay cacbon là catot, tương tự như cặp vi pin trong ăn mòn kim loại. Với cặp vi pin có điện thế khoảng 1,2 V, dòng điện nhỏ cỡ µA xuất hiện, đóng vai trò 164 tác nhân oxy hóa khử trong phản ứng phân hủy các hợp chất hữu cơ hấp phụ trên bề mặt điện cực. Do có nguyên lý như vậy, quá trình vi điện phân Fe-C, Fe-Cu còn gọi là quá trình nội điện phân (internal microelectrolysis). Từ đó cho thấy, có thể hòa tan sắt không cần sử dụng dòng điện ngoài, bằng cách thiết lập các cặp vi pin dưới dạng vật liệu tổ hợp Fe-C, Fe-Cu đây là ưu thế quan trọng trong kỹ thuật nội điện phân tiền xử lý nước thải [7-10]. Các phản ứng xảy ra trong quá trình nội điện phân như sau: Phản ứng tại anot (Fe): Fe Fe2+ + 2e E0(Fe2+/Fe) = - 0,44V Phản ứng tại catot (C): 2H+ + 2e 2[H] = H2 E0(H+/H2) = 0,00V Nếu trong dung dịch có mặt các chất hữu cơ: RX (hợp chất clo hữu cơ), RNO2 (hợp chất nitro vòng thơm), đây là các thành phần có khả năng nhận electron từ trên bề mặt anot (Fe kim loại), chúng bị khử theo phản ứng loại clo và amin hóa Khi đó chất ô nhiễm sẽ chuyển thành các sản phẩm không độc hoặc ít độc hơn, dễ phân hủy bằng sinh học hơn Vì phenol là một hợp chất hữu cơ bền rất khó phân hủy, nên trong nghiên cứu này, chúng tôi đã nghiên cứu ảnh hưởng của các yếu tố như pH, thời gian xử lý, khối lượng vật liệu Fe-Cu, tốc độ lắc, nồng độ đến hiệu suất phân hủy phenol của vật liệu Fe-Cu trong môi trường nước. 2. VẬT LIỆU VÀ PHƯƠNG PHÁP 2.1. Chế tạo vật liệu Bột Fe, kích thước nhỏ hơn 50µm, tinh khiết 99,9 % (PA, Trung Quốc), được ngâm trong dung dịch NaOH 30% trong 10 phút để tẩy dầu mỡ và làm sạch toàn bộ bề mặt, kích hoạt bề mặt bằng cách rửa nhiều lần và xử lý trong dung dịch HCl: H2O (1: 5; v / v) trong 3 phút. Tiếp theo rửa nhiều lần bằng nước, sấy khô ở 105oC trong 2h, để nguội, bảo quản trong lọ thủy tinh kín. Các mẫu Fe-Cu được chế tạo theo phương pháp mạ hóa học trong dung dịch CuSO4 5%. Sử dụng bột Fe cho vào dung dịch CuSO4 với nồng độ 5%, trong khoảng thời gian 2 phút, sau đó rửa nhiều lần bằng nước và sấy khô ở nhiệt độ 105oC trong 3 giờ dưới khí N2 [11, 12]. Vật liệu sau đó được bảo quản trong bình hút ẩm (desiccator) để sử dụng cho các nghiên cứu tiếp theo 2.2. Khảo sát cấu trúc, thành phần, tính chất vật lý, đặc điểm bề mặt vật liệu Fe-Cu Vật liệu Fe-Cu sau khi chế tạo được xác định đặc điểm bề mặt, thành phần bằng phương pháp hiển vi điện tử quét (SEM), phổ tán xạ năng lượng (EDS) (trên máy SEM- EDS, JSM 6610 LA - JEOL, Nhật Bản), các phép đo được tiến hành tại Viện Hóa học - Vật liệu, Viện Khoa học và Công nghệ Quân sự. Cấu trúc của vật liệu được xác định bằng phương pháp nhiễu xạ tia X (XRD) (trên máy Brucker, D5000), phép đo được tiến hành tại Khoa Hóa học - Đại học Khoa học Tự nhiên Hà Nội. 2.3. Nghiên cứu phân hủy phenol Các yếu tố ảnh hưởng đến quá trình phân hủy phenol được tiến hành khảo sát là: pH dung dịch, thời gian, khối lượng vật liệu Fe-Cu, nồng độ phenol ban đầu, tốc độ lắc. - Ảnh hưởng của pH được thực hiện bằng cách cho 1,0 g vật liệu nội điện phân Fe-Cu vào 100 mL dung dịch phenol có nồng độ ban đầu 100 mg/L, pH thay đổi trong khoảng từ 3-8, Tiến hành rung siêu âm 10 phút, lắc trên máy lắc với thời gian 12h, tốc độ lắc 200 vòng/phút. Dung dịch pH được điều chỉnh bằng các dung dịch HNO3 và NaOH 0,1M. - Ảnh hưởng của thời gian phân hủy phenol được thực hiện bằng cách cho 1,0 g vật liệu nội điện phân Fe-Cu vào 100 mL dung dịch phenol có nồng độ đầu 100 mg/L, ở pH bằng 3. Tiến hành rung siêu âm 10 phút, lắc trên máy lắc trong thời gian 2,0; 4,0; 6,0; 8,0; 12,0; 20,0; 24,0 giờ, tốc độ lắc 200 vòng/phút. - Ảnh hưởng của khối lượng vật liệu Fe-Cu được thực hiện bằng cách cho vào mỗi bình tam giác dung tích 250 mL với khối lượng vật liệu lần lượt là: 0,25; 0,5; 0,75; 1,0; 2,0; 30; 4,0; 5,0; 6,0 g. Cho tiếp vào mỗi bình cầu 100 mL dung dịch phenol có nồng độ đầu 100 mg/L, ở pH bằng 3. Tiến hành rung siêu âm 10 phút, lắc trên máy lắc với thời gian 12h, tốc độ lắc 200 vòng/phút. - Ảnh hưởng của tốc độ lắc được thực hiện bằng cách 1,0 g vật liệu vào mỗi bình tam giác 165 có dung tích 250 mL vào 100 mL dung dịch phenol có nồng độ đầu 100 mg/L, ở pH bằng 3. Tiến hành rung siêu âm 10 phút, lắc trong thời gian 12 giờ, tốc độ lắc thay đổi từ 150, 200, 250 vòng /phút). - Ảnh hưởng của nồng độ ban đầu của phenol được thực hiện bằng cách thay đổi nồng đồ từ 53,38 đến 307,65 mg/L, giá trị pH bằng 3. Tiến hành rung siêu âm 10 phút, lắc trên máy lắc với thời gian 12h, tốc độ lắc 200 vòng/phút. Các thí nghiệm được tiến hành ở nhiệt độ phòng (25oC± 0,5). Sau đó xác định lại nồng độ của phenol trong dung dịch. Nồng độ của phenol trước và sau khi xử lý bằng vật liệu Fe- C được xác định bằng phương pháp HPLC, thực hiện trên máy Sắc ký lỏng cao áp Waters Acquity Arc tại Trường Đại học Sư phạm - Đại học Thái Nguyên. Hiệu suất phân hủy phenol được tính theo công thức: x100% C C(C H% 0 cb))0 Trong đó: C0 là nồng độ dung dịch phenol ban đầu trước khi phân hủy (mg/L), Ccb là là nồng độ dung dịch phenol sau khi phân hủy (mg/L), H là hiệu suất phân hủy (%). 3. KẾT QUẢ VÀ THẢO LUẬN 3.1. Kết quả khảo sát đặc điểm bề mặt, tính chất vật lý của vật liệu Fe-Cu Hình 1: Phổ đồ EDS của Fe Kết quả phân tích ảnh SEM-EDX của vật liệu Fe và Fe- Cu được chỉ ra ở trên hình 1 đến 3 và bảng 1, 2. Kết quả phân tích ảnh SEM cho thấy cấu trúc các hạt bột Fe, Cu được phân bố tương đối đồng đều trên bề mặt, kích thước nhỏ hơn 50µm Kết quả phân tích EDX (bảng 1) cho thấy, thành phần nguyên tố chính của vật liệu là Fe, Cu, O , C. Sự xuất hiện của O trong kết quả phân tích cho thấy trong quá trình bảo quản mẫu bị oxi hóa nhiều trên bề mặt. Bảng 1: Kết quả phân tích các nguyên tố mẫu Fe Nguyên tố % Khối lượng % Nguyên tử O K 8,95 25,55 Fe K 91,05 74,45 Tổng cộng 100,00 100,00 Hình 2: Phổ đồ EDS của vật liệu Fe-Cu Bảng 2: Kết quả phân tích các nguyên tố mẫu Fe-Cu Nguyên tố % Khối lượng % Nguyên tử O K 12,11 29,97 Fe K 13,32 9,94 Cu K 69,30 43,20 C K 5,27 17,39 Tổng cộng 100,00 100,00 Hình 3: Giản đồ XRD của vật liệu Fe và Fe-Cu 166 Kết quả phân tích cấu trúc thành phần vật liệu Fe (trước khi mạ) và Fe/Cu (sau khi mạ), được chỉ ra ở hình 3 cho thấy thành phần 2 phổ khác nhau rõ rệt, phổ đã mạ được phủ toàn bộ Cu bề mặt vật liệu hạt Fe. 3.2. Kết quả phân hủy phenol 3.2.1. Ảnh hưởng của pH Kết quả hình 4 cho thấy, khi giá trị pH tăng từ 3 đến 9, hiệu suất phân hủy phenol giảm dần. Điều này có thể giải thích trong quá trình phân hủy phenol bao gồm các quá trình: quá trình phân hủy do tác động của vật liệu nội điện phân, quá trình hấp phụ, keo tụ cùng sắt hydroxit sinh ra. Ở pH cao (pH>3), quá trình phân hủy phenol giảm, tuy nhiên quá trình keo tụ tăng, do vậy hiệu suất phân hủy phenol cũng giảm dần. Do đó, pH bằng 3 có hiệu suất phân hủy phenol cực đại. Vì vậy, chúng tôi chọn giá trị pH này cho các nghiên cứu tiếp theo. Hình 4: Đồ thị biểu diễn ảnh hưởng của pH đến hiệu suất xử lí phenol của vật liệu Fe-Cu 3.2.2. Ảnh hưởng của thời gian Kết quả được trình bày ở hình 5. Hình 5: Đồ thị biểu diễn ảnh hưởng của thời gian đến hiệu suất xử lí phenol của vật liệu Fe-Cu Kết quả hình 5 cho thấy, khi tăng thời gian từ 2 đến 12 giờ đầu tiên, hiệu suất phân hủy phenol tăng nhanh đạt giá trị cực đại 91,4%. Trong khoảng thời gian từ 12 đến 24 giờ, hiệu suất phân hủy giảm chậm và gần như ổn định. Vì vậy, chúng tôi chọn 12 giờ là thời gian tối ưu để phân hủy phenol của vật liệu Fe-Cu. 3.2.3. Ảnh hưởng của khối lượng vật liệu Kết quả được trình bày ở hình 6. Hình 6: Đồ thị biểu diễn ảnh hưởng của khối lượng vật liệu đến hiệu suất xử lí phenol của vật liệu Fe-Cu Kết quả từ hình 6 cho thấy, khi tăng khối lượng vật liệu Fe-Cu từ 0,25 đến 1,0 thì hiệu suất phân hủy phenol tăng dần, khi tăng khối lượng vật liệu từ 1,0 đến 6,0 g thì hiệu suất phân hủy phenol giảm dần. Vì vậy, chúng tôi chọn khối lượng vật liệu 1,0 g là khối lượng vật liệu tối ưu để phân hủy phenol của vật liệu Fe-Cu. 3.2.4. Ảnh hưởng của tốc độ lắc Kết quả ảnh hưởng của tốc độ lắc đến hiệu suất phân hủy phenol được thể hiện trên hình 7 cho thấy khi tăng tốc độ lắc thì hiệu suất phân hủy phenol cũng tăng. Điều này được giải thích là quá trình lắc sẽ ảnh hưởng tới việc cung cấp O2 cho phản ứng hòa tan Fe, do vậy tốc độ lắc càng lớn thì hiệu suất quá trình phân hủy phenol càng lớn sau đó dần ổn định, Do đó, chúng tôi chọn tốc độ lắc 200 vòng/phút để phân hủy phenol của vật liệu nội điện phân Fe- Cu. 167 Hình 7: Đồ thị biểu diễn ảnh hưởng của tốc dộ lắc đến hiệu suất xử lí phenol của vật liệu Fe-Cu 3.2.5. Ảnh hưởng nồng độ đầu của phenol Kết quả được trình bày ở hình 8. Hình 8: Đồ thị biểu diễn ảnh hưởng của nồng độ đến khả năng xử lí phenol của vật liệu Fe-Cu Kết quả từ hình 8 cho thấy khi nổng độ tăng từ 53,38 đến 100,98 mg/L thì hiệu suất phân hủy phenol tăng nhanh, nhưng trong khoảng nồng độ từ 146,69 đến 250,76 mg/L thì hiệu suất phân hủy phenol giảm dần. Tại giá trị nồng độ phenol bằng 100,98 mg/L thì hiệu suất phân hủy đạt giá trị lớn nhất 92,7%. Phenol đã bị phân hủy gần như hoàn toàn. Có sự giảm mạnh hiệu suất ở nồng độ phenol cao (100,98 mg/L), có thể do ở tại các nồng độ cao này cần lượng vật liệu nội điện phân, thời gian phản ứng tăng. Do vậy cần có các nghiên cứu, khảo sát tiếp theo để xử lý phenol ở nồng độ cao. 3.2.5. Phân tích phân hủy nồng độ phenol bằng HPLC Hình 9: Các đường sắc ký đồ của mẫu dung dịch chứa phenol phụ thuộc vào khối lượng vật liệu Fe-Cu Hình 10: Phổ HPLC của mẫu dung dịch chứa phenol phụ thuộc vào khối lượng vật liệu Fe-Cu - Đường Co : Mẫu phenol ban đầu (100,98 mg/L) không có vật liệu Fe-Cu - Đường 0,5 gam :Mẫu phenol nồng độ ban đầu (100,98 mg/L) có 1,0 g vật liệu Fe-Cu, thời gian lắc 12 giờ, tốc độ lắc 200 vòng/phút, ở pH bằng 3. - Đường 1gam :Mẫu phenol nồng độ ban đầu (100,98 mg/L) có 1,0 g vật liệu Fe-Cu, thời gian lắc 12 giờ, tốc độ lắc 200 vòng/phút, ở pH bằng 3. Kết quả phân tích HPLC dung dịch phenol nồng độ ban đầu là 100,98 mg/L không có và có 0,5; 1,0 g vật liệu nội điện phân Fe-Cu sau thời gian lắc 12 giờ, pH bằng 3, tốc độ lắc 200 vòng/phút được thể hiện trên hình 9, 10. Kết quả phân tích HPLC cho thấy phenol đã bị 168 phân hủy gần như hoàn toàn khi sử dụng khối lượng vật liệu là 1,0 g, thời gian lắc 12 giờ, tốc độ lắc 200 vòng/phút, pH bằng 4. 4. KẾT LUẬN Đã chế tạo được mẫu vật liệu nội điện phân Fe- Cu đi từ nguyên liệu bột Fe và chế tạo theo phương pháp mạ hóa học, có hàm lượng Cu ở bề mặt đạt 69,30 % (về khối lượng).Vật liệu sau khi chế tạo được xác định đặc điểm bề mặt, cấu trúc, thành phần bằng phương pháp phổ hiển vi điện tử quét (SEM), phổ tán xạ năng lượng (EDS), giản đồ nhiễu xạ tia X (XRD). Đã nghiên cứu một số yếu tố ảnh hưởng đến khả năng phân hủy phenol như: pH, thời gian, khối lượng vật liệu Fe-Cu, nồng độ đầu phenol, tốc độ lắc. Kết quả cho thấy tại giá trị pH bằng 3, thời gian lắc 12 giờ, tốc độ lắc 200 vòng/phút, khối lượng vật liệu Fe-Cu là 1,0 g, ở nhiệt độ phòng (25oC± 0,5), nồng độ phenol ban đầu bằng 100,98 mg/L thì hiệu suất phân hủy phenol là 92,7%. Từ các kết quả trên cho thấy, vật liệu Fe-Cu chế tạo có thể được áp dụng vào trong thực tế để xử lý nước thải cốc hóa trong môi trường nước trước khi xử lý bằng phương pháp sinh học. Lời cảm ơn: Nghiên cứu này được tài trợ bởi đề tài Khoa học và Công nghệ Cấp bộ, mã số B2019-TNA-08. TÀI LIỆU THAM KHẢO 1. Do Tra Huong, Nguyen Van Tu, Nguyen Anh Tien, Hoang Minh Hao, Nguyen Phuong Chi, “Removal of methylene blue from aqueous solutions by internal microelectrolysis on the Fe-C materials”, Vietnam Journal of Chemistry, Vol 57, No 2E12, pp 63-68 (2019). 2. Mengmeng Kang, Qingguo Chen, Jingjing Li ,Mei Liu, Yisong Weng, “Preparation and study of a new type of Fe-C microelectrolysis filler in oil-bearing ballast water treatment”, Environmental Science and Pollution Researc, https://doi.org/10.1007/s11356-019-04480 (2019). 3. Xiaoying Zheng MengqiJin, Xiang Zhou, Wei Chen, DanLu, YuanZhang, Xiaoyao Shao, “Enhanced removal mechanism of iron carbon micro-electrolysis constructed wetland on C, N, and P in salty permitted effluent of wastewater treatment plant”, Science of the Total Environment, 649, pp 21-30 (2019). 4. Longlong Zhang, Qinyan Yue, Kunlun Yang, Pin Zhao, Baoyu Gao, “Analysis of extracellular polymeric substances (EPS) and ciprofloxacin-degrading microbial community in the combined Fe-C microelectrolysis - UBAF process for the elimination of high-level ciprofloxacin”, Chemosphere, 193, pp 645e654 (2018). 5. Yan Wang, Xianwei Wu, Ju Yi, Lijun Chen, Tianxiang Lan and Jie Dai, “Pretreatment of printing and dyeing wastewater by Fe/C micro- electrolysis combined with H2O2 process”, Water Science & Technology, doi: 10.2166/wst..244 (2018). 6. Weiwei Ma, Yuxing Han, ChunyanXu, Hongjun Han, Wencheng Ma, Hao Zhu Kun Li,Dexin Wang, “Enhanced degradation of phenolic compounds in coal gasification wastewater by a novel integration of micro- electrolysis with biological reactor (MEBR) under the micro-oxygen condition”, Bioresource Technology, 251, pp 303-310 (2018). 7. Mingyou Liua, Lu Wang, Xianying Xiaoa, Zhibin He, “Fe/C micro electrolysis and Fenton oxidation process for the removal of recalcitrant colored pollutants from mid-stage pulping effluent”, Journal of Bioresources and Bioproducts. 3(3), pp 118-122 (2018). 8. Qinhong Ji, Salma Tabassum, Sufia Hena, Claudia G. Silva, Guangxin Yu, Zhenjia Zhang. “A review on the coal gasification wastewater treatment technologies: past, present and future outlook”, Journal of Cleaner Production, 126, 38-55 (2016). 9. Qian Zhao, Yu Liu. “State of the art of biological processes for coal gasification wastewater treatment”. Biotechnology Advances, 3, 1064 –1072 (2016). 10. Lili Xu, Jun Wang, Xiaohui Zhang, Deyin Hou, Yang Yu, “Development of a novel integrated membrane system incorporatedwith an activated coke adsorption unit for advanced 169 coal gasification wastewater treatment”, Colloids and Surfaces A: Physicochem. Eng. Aspects, 484, 99–107 (2015). 11.Jin-Hong Fan, Lu-Ming Ma, “The pretreatment by the Fe/Cu process for enhancing biologicaldegradability of the mixed wastewater”, Journal of Hazardous Materials, 164, (2009)1392-1397. 12. Bo Lai, Yun Zhang, Zhaoyun Chen, Ping Yang, Yuexi Zhou, Juling Wang, “Removal of p-nitrophenol (PNP) in aqueous solution by the micron-scale iron–copper (Fe/Cu) bimetallic particles”, Applied Catalysis B: Environmental, 144, (2014) 816-830. _____________________________________________________________________ NGHIÊN CỨU CHẾ TẠO THAN SINH HỌC TỪ BÃ ĐẬU ......... Tiếp theo Tr. 163 Dựa vào phương trình đẳng nhiệt: y = 0,0685x + 0,6008 với R2 = 0,9639 ta tính được dung lượng hấp phụ Pb2+ cực đại đại Qmax = 1/0,0685 = 14,598 mgPb/g. 4. KẾT LUẬN Nghiên cứu đã chế tạo được vật liệu than sinh học và vật liệu than sinh học biến tính từ bã đậu nành. Khảo sát hiệu suất hấp phụ ion Cu2+, Pb2+ của 2 loại vật liệu này cho thấy vật liệu than sinh học biến tính bằng axit H3PO4 từ bã đậu nành đạt kết quả tốt hơn. Kết quả chụp IR của vật liệu cho thấy quá trình biến tính và nung vật liệu đã làm thay đổi cấu trúc vật liệu do đó làm tăng tổng diện tích bề mặt vật liệu nên khả năng hấp phụ tăng. Khảo sát ảnh hưởng của nồng độ ion Cu2+, Pb2+ tới quá trình hấp phụ ta thấy quá trình hấp phụ tuân theo mô hình đường hấp phụ đẳng nhiệt Lăngmuir với dung lượng hấp phụ cực đại (Qmax) của vật liệu là 14,598 mgPb/g đối với Pb2+ và 16,37 mgCu/g đối với Cu2+ TÀI LIỆU THAM KHẢO [1] Babich, H., Devanas, M.A., Stotzky, G., The mediation of mutagenicity and clastogenicity of heavy metals by physicochemical factors. Environmental Research 37 (1985), 253–286. [2] Fenglian Fu, Qi Wang Removal of heavy metal ions from wastewaters: A review, Journal of Environmental Management 92 (2011) 407-418. [3] Ningchuan Feng, Xueyi Guoa, Sha Lianga, Yanshu Zhub, Jianping Liu, Biosorption of heavy metals from aqueous solutions by chemically modified orange peel, Journal of Hazardous Materials 185 (2011) 49–54. [4] Yi-Chao Lee, Shui-Ping Chang, The biosorption of heavy metals from aqueous solution by Spirogyra and Cladophora filamentous macroalgae, Bioresource Technology 102 (2011) 5297–5304. [5] J.M.Patra, S.S.Panda, 2016, Biochar as a low-cost adsorbent for heavy metal removal, North Orissa University Baripada, India. 170
File đính kèm:
 phan_huy_phenol_trong_moi_truong_nuoc_bang_qua_trinh_noi_die.pdf
phan_huy_phenol_trong_moi_truong_nuoc_bang_qua_trinh_noi_die.pdf

