Nghiên cứu tối ưu hóa quá trình tách tế bào đơn nhân máu ngoại vi và chuyển nạp tạo khối tế bào car-T cho điều trị lơ-xê-mi cấp dòng lympho
Tối ưu hóa quá trình thu nhận tế bào đơn nhân máu ngoại vi (peripheral blood
mononuclear cell - PBMC) và quá trình chuyển nạp tạo tế bào CAR-T. Đối tượng và phương
pháp: Máu ngoại vi từ người hiến tặng khỏe mạnh được tiến hành tách PBMC bằng FicollPaque. Phản ứng chuyển nạp tạo khối tế bào CAR-T được thực hiện ngay sau khi thu nhận
PBMC hoặc sau khi kích hoạt tế bào bằng bi từ gắn kháng thể kháng CD3 và CD28. Các thông
số: Hệ thống chuyển nạp, số lượng tế bào cho một phản ứng và lượng plasmid DNA được tối
ưu hóa. Kết quả: Máu pha loãng 2 lần với PBS 1X cho hiệu suất thu nhận PBMC và tỷ lệ tế
bào sống cao nhất. Thực hiện phản ứng chuyển nạp trên hệ thống Nucleofector 2b (Lonza) với
2 × 107 PBMC không kích hoạt, lượng plasmid DNA 1 µg SB100X và 10 µg pSB-CAR19 cho
kết quả tốt nhất. Kết luận: Tối ưu hóa được quá trình tách PBMC và chuyển nạp tạo khối tế
bào CAR-T cho điều trị lơ-xê-mi cấp dòng lympho

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5
Trang 6

Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Nghiên cứu tối ưu hóa quá trình tách tế bào đơn nhân máu ngoại vi và chuyển nạp tạo khối tế bào car-T cho điều trị lơ-xê-mi cấp dòng lympho

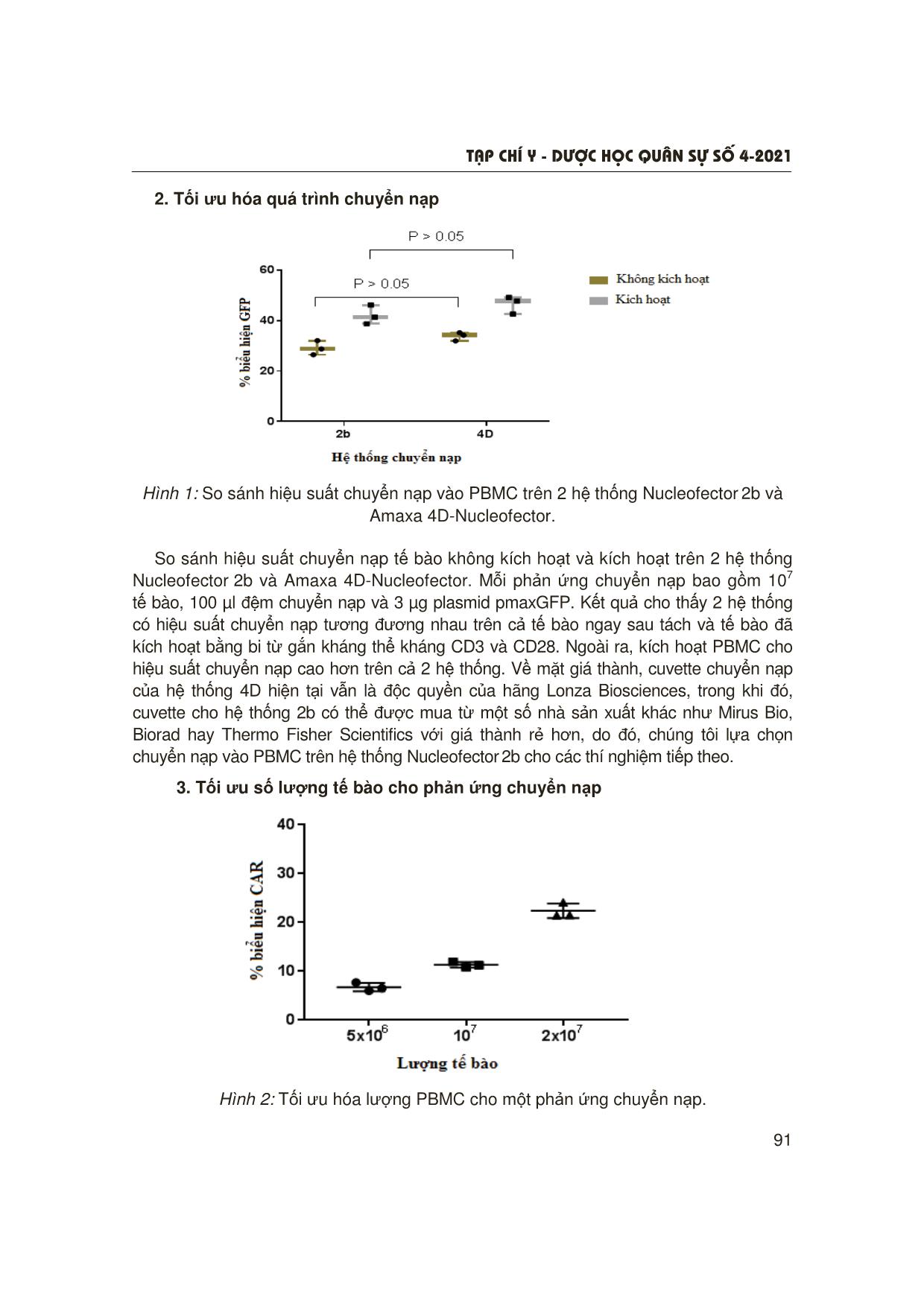
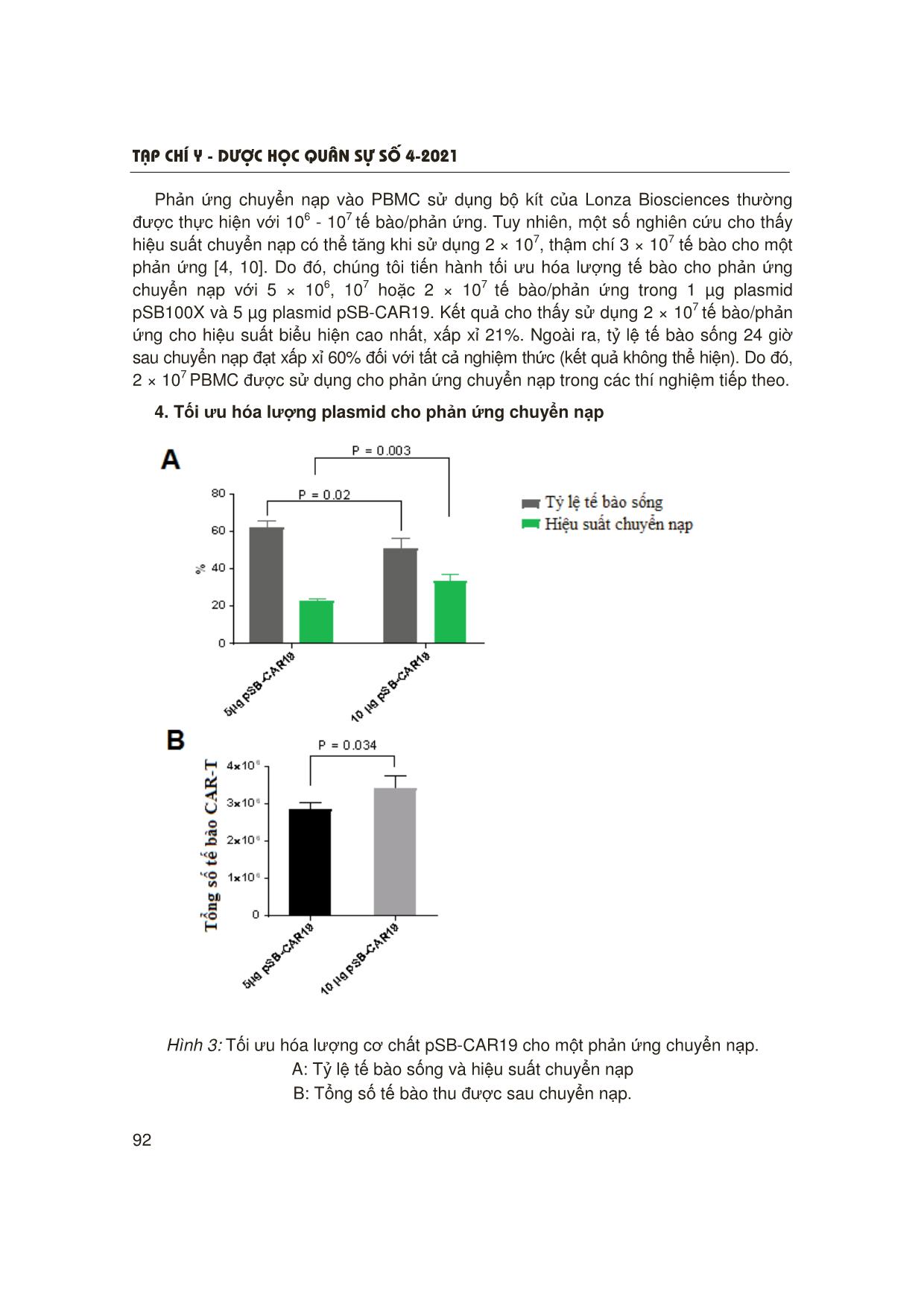
T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 87 NGHIÊN CỨU TỐI ƯU HÓA QUÁ TRÌNH TÁCH TẾ BÀO ĐƠN NHÂN MÁU NGOẠI VI VÀ CHUYỂN NẠP TẠO KHỐI TẾ BÀO CAR-T CHO ĐIỀU TRỊ LƠ-XÊ-MI CẤP DÒNG LYMPHO Hồ Viết Hoành1, Đặng Thành Chung2 Nguyễn Thị Phương Thảo3, Cấn Văn Mão2 TÓM TẮT Mục tiêu: Tối ưu hóa quá trình thu nhận tế bào đơn nhân máu ngoại vi (peripheral blood mononuclear cell - PBMC) và quá trình chuyển nạp tạo tế bào CAR-T. Đối tượng và phương pháp: Máu ngoại vi từ người hiến tặng khỏe mạnh được tiến hành tách PBMC bằng Ficoll- Paque. Phản ứng chuyển nạp tạo khối tế bào CAR-T được thực hiện ngay sau khi thu nhận PBMC hoặc sau khi kích hoạt tế bào bằng bi từ gắn kháng thể kháng CD3 và CD28. Các thông số: Hệ thống chuyển nạp, số lượng tế bào cho một phản ứng và lượng plasmid DNA được tối ưu hóa. Kết quả: Máu pha loãng 2 lần với PBS 1X cho hiệu suất thu nhận PBMC và tỷ lệ tế bào sống cao nhất. Thực hiện phản ứng chuyển nạp trên hệ thống Nucleofector 2b (Lonza) với 2 × 107 PBMC không kích hoạt, lượng plasmid DNA 1 µg SB100X và 10 µg pSB-CAR19 cho kết quả tốt nhất. Kết luận: Tối ưu hóa được quá trình tách PBMC và chuyển nạp tạo khối tế bào CAR-T cho điều trị lơ-xê-mi cấp dòng lympho. * Từ khóa: CAR-T, CD19; Tế bào đơn nhân máu ngoại vi; Chuyển nạp; Hệ thống Sleeping Beauty. Optimization of Peripheral Blood Mononuclear Cells Isolation and Nucleofection for Development of Anti-CD19 CAR-T Cells in Treatment of B Lymphoblastic Leukemia Summary Objectives: To optimize isolation and nucleofection (based on Sleeping Beauty system) of peripheral blood mononuclear cells (PBMC). Materials and methods: PBMCs were isolated from peripheral blood of healthy donors using Ficoll-Paque. Different dilutions of whole blood and PBS 1X were tested. Nucleofection was performed on either unstimulated PBMC or stimulated PBMC (using CD3/CD28 dynalbeads). Parameters including nucleofector, number of cells, 1Trung tâm Ung bướu, Bệnh viện Quân y 103, Học viện Quân y 2Bộ môn Sinh lý bệnh, Học viện quân y 3Viện Công nghệ Sinh học và Công nghệ Thực phẩm, Trường Đại học Bách Khoa Hà Nội Người phản hồi: Cấn Văn Mão (canvanmao2011@gmail.com) Ngày nhận bài: 05/02/2021 Ngày bài báo được đăng: 27/4/2021 T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 88 Bài viết là sản phẩm của đề tài nghiên cứu KC 10.39/16-20 được tài trợ bởi chương trình KC.10/16-20. and amount of DNA substrate were optimized. Results: The best result was obtained when 2 × 107 unstimulated PBMCs were nucleofected using Nucleofector 2b, 1 µg sSB100X, and 10 µg pSB-CAR19. Conclusion: We have successfully developed an optimized protol for PBMC isolation and nucleofection for development of anti-CD19 CAR-T cells. * Keywords: CAR-T; CD19; Peripheral blood mononuclear cell; Nucleofection; Sleeping Beauty system. ĐẶT VẤN ĐỀ Trên thế giới, lơ-xê-mi cấp dòng lympho (acute lymphoblastic leukemia - ALL) là một trong những bệnh ung thư phổ biến ở trẻ em, chiếm khoảng 75% tất cả các loại ung thư máu [1]. Bệnh được đặc trưng bởi sự phát triển của một số lượng lớn tế bào lympho chưa trưởng thành. Triệu chứng thường bao gồm thiếu máu, xuất huyết, nhiễm khuẩn, hạch to... Bệnh tiến triển nhanh và thường gây tử vong trong thời gian ngắn [2]. Điều trị bệnh lơ-xê-mi cấp dòng lympho nhằm tiêu diệt các tế bào bạch cầu ác tính và phục hồi tuỷ xương trở lại bình thường. Liệu pháp điều trị tiêu chuẩn cho lơ-xê-mi cấp dòng lympho hiện nay là hóa trị liệu, thường chia thành 3 giai đoạn: Cảm ứng, củng cố và duy trì. Tuy nhiên, hạn chế của hóa trị liệu là hầu như không có khả năng chữa khỏi bệnh hoàn toàn mà chỉ thuyên giảm một phần. Bệnh cũng có thể được điều trị bằng xạ trị khi đã lan đến não. Ghép tế bào gốc được sử dụng khi bệnh tái phát sau liệu trình điều trị tiêu chuẩn [3]. Tuy nhiên, tỷ lệ khỏi bệnh hoàn toàn theo hướng điều trị này cũng không cao, chỉ đạt tối đa 20% ở người trưởng thành. Liệu pháp miễn dịch sử dụng tế bào T mang thụ thể nhân tạo CAR (chimeric antigen receptors) là một hướng tiếp cận mới. Nguyên tắc của liệu pháp CAR-T trong điều trị ung thư là tạo ra các tế bào T mang thụ thể nhân tạo có khả năng nhận biết kháng nguyên đặc hiệu trên bề mặt tế bào ung thư, từ đó kích hoạt khả năng phân giải tế bào ung thư của tế bào T. Năm 2017, Cơ quan Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã cấp phép cho 2 dạng điều trị sử dụng CAR-T là Kymriah (hãng Novartis) cho điều trị bệnh bạch cầu lympho cấp ở trẻ em và Yescarta (hãng Kite Pharma) cho bệnh u lympho ác tính không Hodgkin ở người lớn. Ngoài sử dụng retrovirus, khối tế bào CAR-T có thể được tạo bằng phương pháp “non-virus”, sử dụng hệ thống chuyển nạp Sleeping Beauty. Nguyên lý cơ bản của phương pháp này là chuyển nạp đồng thời 2 thành phần SB transposase và SB transposon. SB transposase có chức năng cắt đoạn trình tự đích trên transposon và gắn vào thể gen tế bào chủ tại các vị trí giàu nucleotide T và A [4]. Tuy liệu pháp CAR-T đã được FDA công nhận và ứng dụng nhưng ở Việt Nam chưa có nghiên cứu nào về liệu pháp tế bào CAR-T trong điều trị ung thư nói chung và lơ-xê-mi cấp dòng lympho nói riêng. Do đó, chúng tôi tiến hành nghiên cứu này nhằm: Tối ưu hóa quá trình tách PBMC và chuyển nạp tạo khối tế bào CAR-T ứng dụng trong điều trị lơ-xê-mi cấp dòng lympho. T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 89 ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU 1. Đối tượng, vật liệu nghiên cứu - Đối tượng nghiên cứu: Tế bào máu ngoại vi tách từ máu toàn phần của người hiến khỏe mạnh. - Nguyên vật liệu nghiên cứu: + Plasmid pmaxGFP (Lonza Biosciences). + Plasmid pSB100X (pCMV(CAT)T7- SB100, #34879). + Plasmid pSB-CAR19 mã hóa phân tử CAR thế hệ thứ hai kháng CD19. + Môi trường nuôi cấy tế bào RPMI- 1640, huyết thanh bào thai bò (fetal bovin serum - FBS), dung dịch penicillin và streptomycin 1%. - Ficoll-Paque PREMIUM (Cytiva Life Sciences, Hoa Kỳ). - Kít chuyển nạp P3 Primary Cell 4D-Nucleofector. - Kít chuyển nạp Human T cell nucleofector. - Hệ thống chuyển nạp Nucleofector 2b. - Hệ thống chuyển nạp Amaxa 4D- Nucleofector. - Hệ thống BD FACSLyric Clinical System. - Các vật tư tiêu hao cần thiết phục vụ cho nuôi cấy tế bào: Chai nuôi cấy tế bào, pipet, chai đựng môi trường, lọc vi khuẩn 0,45 µm (hãng ATCC, Hoa Kỳ). - Hệ thống phòng thí nghiệm phục vụ nuôi cấy tế bào: Phòng sạch, tủ ấm CO2, kính hiển vi soi ngược, máy ly tâm, tủ mát 40C, tủ âm -200C, -800C, bình chứa nitơ lỏng. 2. Phương pháp nghiên cứu * Tách PBMC: Máu tươi (đã xử lý chống đông) được pha loãng với PBS 1X (pH 7,2) ở các tỷ lệ khác nhau. Sau đó, đưa nhẹ nhàng 10 ml hỗn hợp trên vào ống falcon 15 ml chứa sẵn 3 ml Ficoll-Paque PREMIUM (p = 1,077 g/ml) sao cho 2 lớp Ficoll và máu không trộn lẫn với nhau. Các ống falcon được ly tâm lạnh tại 400g trong 35 phút (không sử dụng chế độ phanh). Sau khi ly tâm, lớp PBMC (nằm giữa plasma và Ficoll) được hút ra và hòa vào 10 ml PBS 1X (0,5% BSA; pH 7,2). Sau đó tế bào được rửa 2 lần bằng PBS 1X (ly tâm 300 ×g, 10 phút) và hòa tan bằng 4 ml môi trường nuôi cấy (RPMI-1640 bổ sung 10% FBS). 200 µl PBMC được sử dụng cho đếm tế bào và phân tích bằng flow cytometry. PBMC thu được quan sát dưới kính hiển vi soi ngược, đếm sống/chết bằng nhuộm trypan blue 0,4% và phân tích bằng flow cytometry. Các thông số tổng lượng tế bào đơn nhân thu được, tỷ lệ tế bào sống và tỷ lệ lymphocyte trong quần thể PBMC được xác định. * Chuyển nạp vào PBMC tạo khối tế bào CAR-T: Tế bào đơn nhân máu ngoại vi ngay sau khi tách hoặc kích hoạt được sử dụng cho chuyển nạp. Kích hoạt tế bào được thực hiện bằng bi từ Dynabeads Human T-Activator CD3/CD28 (Thermo Fisher Scientific, Hoa Kỳ) theo đúng hướng dẫn của nhà sản xuất. Hệ thống chuyển nạp, lượng tế bào, lượng DNA cho mỗi phản ứng chuyển nạp được tối ưu. Sau khi thu đủ số tế bào yêu cầu (ly tâm 200 ×g, 10 phút, nhiệt độ phòng, không sử dụng phanh), hòa tan trong 100 µl đệm chuyển nạp và bổ sung các lượng DNA khác nhau. T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 90 Hỗn hợp này sau đó được chuyển vào Cuvette chuyên dụng (Lonza Biosciences), được xung điện bằng chương trình U-014 hoặc T-020 (đối với hệ thống Nucleofector 2b) hoặc EO-115 (đối với hệ thống Amaxa 4D-Nucleofector). Ngay sau khi xung điện, 500 µl môi trường nuôi cấy đã làm ấm được bổ sung vào Cuvette và toàn bộ hỗn hợp trên được chuyển vào đĩa 6 giếng chứa 5 ml môi trường nuôi cấy mỗi giếng. Tế bào được nuôi 24 giờ trước khi đánh giá hiệu suất chuyển nạp bằng phân tích tế bào theo dòng chảy. * Đánh giá hiệu suất chuyển nạp bằng phân tích tế bào theo dòng chảy: Thu được ít nhất 106 tế bào sau 24 giờ chuyển nạp và nhuộm với CD19 tái tổ hợp gắn FITC (rCD19-FITC, abcam, # ab246020) và PI hoặc 7-AAD (hãng Thermo Fisher Scientifics, Hoa Kỳ) theo hướng dẫn của nhà sản xuất. Sau khi nhuộm, tế bào được rửa bằng PBS 1X và hòa tan trong PBS 1X bổ sung 1% FBS trước khi phân tích với hệ thống BD FACSLyric Clinical System. * Xử lý số liệu: So sánh trung bình của 2 nhóm độc lập bằng T-test, so sánh trung bình của 3 nhóm bằng phân tích phương sai ANOVA. Xử lý số liệu bằng phần mềm SPSS 20.0 và GraphPad Prism 6, khác biệt có ý nghĩa thống kê khi p < 0,05. KẾT QUẢ NGHIÊN CỨU 1. Tối ưu hóa tỷ lệ pha loãng máu với PBS Bảng 1: Kết quả đếm tế bào và phân tích flow cytometry các mẫu PBMC với tỷ lệ pha loãng máu trong PBS 1X khác nhau. Pha loãng Tổng số tế bào thu được (× 107) Tỷ lệ tế bào sống (%) Tỷ lệ tế bào lympho (%) 2 lần 1,66 ± 0,13 94,5 ± 2,1 63,04 ± 2,9 4 lần 1,84 ± 0,49 95,5 ± 0,7 60,82 ± 6,9 Không pha loãng 0,97 ± 0,21 77 ± 1,4 60,9 ± 1,1 Tổng cộng 30 ml máu tươi được chia thành 3 phần bằng nhau và pha loãng với PBS 1X theo 3 tỷ lệ: Không pha loãng, pha loãng 2 lần và pha loãng 4 lần (do các nhà sản xuất thường khuyến cáo tỷ lệ pha loãng từ 2 - 4 lần). Sau đó, 3 mẫu trên được thực hiện tách PBMC như đã trình bày. Đếm tế bào bằng máy Countess II FL Automated Cell Counter; quan sát các mẫu PBMC thu được qua kính hiển vi thấy pha loãng máu 2 lần và 4 lần với PBS 1X cho kết quả tương đương nhau. Cụ thể, lượng tế bào sống đạt > 90% và tổng lượng PBMC thu được từ 10 ml máu đạt xấp xỉ 1,7 × 107 tế bào. Tuy nhiên, không pha loãng máu khiến tỷ lệ tế bào sống giảm còn 78%; tổng lượng tế bào thu được từ 10 ml máu cũng thấp hơn, ở mức 0,97 × 107 tế bào. Phân tích flow cytometry cho thấy tỷ lệ tế bào lympho trong các mẫu PBMC thu được tương đương nhau, ở mức 60%. Như vậy, các thí nghiệm tách PBMC sẽ được thực hiện với tỷ lệ pha loãng máu 2 lần trong PBS 1X (do pha loãng 4 lần có kết quả tốt hơn một chút so với 2 lần nhưng tốn kém vật tư hóa chất hơn nhiều và thời gian xử lý mẫu kéo dài so với pha loãng máu 2 lần). T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 91 2. Tối ưu hóa quá trình chuyển nạp Hình 1: So sánh hiệu suất chuyển nạp vào PBMC trên 2 hệ thống Nucleofector 2b và Amaxa 4D-Nucleofector. So sánh hiệu suất chuyển nạp tế bào không kích hoạt và kích hoạt trên 2 hệ thống Nucleofector 2b và Amaxa 4D-Nucleofector. Mỗi phản ứng chuyển nạp bao gồm 107 tế bào, 100 µl đệm chuyển nạp và 3 µg plasmid pmaxGFP. Kết quả cho thấy 2 hệ thống có hiệu suất chuyển nạp tương đương nhau trên cả tế bào ngay sau tách và tế bào đã kích hoạt bằng bi từ gắn kháng thể kháng CD3 và CD28. Ngoài ra, kích hoạt PBMC cho hiệu suất chuyển nạp cao hơn trên cả 2 hệ thống. Về mặt giá thành, cuvette chuyển nạp của hệ thống 4D hiện tại vẫn là độc quyền của hãng Lonza Biosciences, trong khi đó, cuvette cho hệ thống 2b có thể được mua từ một số nhà sản xuất khác như Mirus Bio, Biorad hay Thermo Fisher Scientifics với giá thành rẻ hơn, do đó, chúng tôi lựa chọn chuyển nạp vào PBMC trên hệ thống Nucleofector 2b cho các thí nghiệm tiếp theo. 3. Tối ưu số lượng tế bào cho phản ứng chuyển nạp Hình 2: Tối ưu hóa lượng PBMC cho một phản ứng chuyển nạp. T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 92 Phản ứng chuyển nạp vào PBMC sử dụng bộ kít của Lonza Biosciences thường được thực hiện với 106 - 107 tế bào/phản ứng. Tuy nhiên, một số nghiên cứu cho thấy hiệu suất chuyển nạp có thể tăng khi sử dụng 2 × 107, thậm chí 3 × 107 tế bào cho một phản ứng [4, 10]. Do đó, chúng tôi tiến hành tối ưu hóa lượng tế bào cho phản ứng chuyển nạp với 5 × 106, 107 hoặc 2 × 107 tế bào/phản ứng trong 1 µg plasmid pSB100X và 5 µg plasmid pSB-CAR19. Kết quả cho thấy sử dụng 2 × 107 tế bào/phản ứng cho hiệu suất biểu hiện cao nhất, xấp xỉ 21%. Ngoài ra, tỷ lệ tế bào sống 24 giờ sau chuyển nạp đạt xấp xỉ 60% đối với tất cả nghiệm thức (kết quả không thể hiện). Do đó, 2 × 107 PBMC được sử dụng cho phản ứng chuyển nạp trong các thí nghiệm tiếp theo. 4. Tối ưu hóa lượng plasmid cho phản ứng chuyển nạp Hình 3: Tối ưu hóa lượng cơ chất pSB-CAR19 cho một phản ứng chuyển nạp. A: Tỷ lệ tế bào sống và hiệu suất chuyển nạp B: Tổng số tế bào thu được sau chuyển nạp. T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 93 Lượng plasmid ảnh hưởng lớn tới hiệu suất và tỷ lệ tế bào sống sau chuyển nạp. Do đó, chúng tôi tiến hành so sánh 2 thông số trên khi thực hiện chuyển nạp với 5 µg pSB-CAR19 (theo khuyến cáo của nhà sản xuất Lonza Biosciences) hoặc 10 µg pSB-CAR19. Đối với pSB100X, lượng plasmid quá nhiều được chứng minh là gây chết lượng lớn PBMC sau chuyển nạp, do vậy, pSB100X được giữ nguyên ở mức 1 µg/phản ứng. Kết quả cho thấy hiệu suất chuyển nạp cải thiện rõ rệt (22,86 - 33,42%) khi tăng lượng cơ chất pSB-CAR19. Bên cạnh đó, tỷ lệ tế bào sống khi tăng lượng DNA giảm từ 62,05% còn 50,84%. Như vậy, có thể tính được tổng lượng tế bào CAR-T sau chuyển nạp khi sử dụng 5 hoặc 10 µg pSB-CAR19 lần lượt là 2,8 × 106 và 3,39 × 106. Qua đó, sử dụng 10 µg cơ chất pSB-CAR19 cho kết quả tốt hơn sử dụng 5 µg cơ chất. BÀN LUẬN Những nỗ lực đầu tiên nhằm chuyển gen vào tế bào T tạo khối tế bào CAR-T được thực hiện vào đầu những năm 2000, dựa trên sự xung điện plasmid mã hóa phân tử CAR hướng đích CD19 kết hợp với gen kháng kháng sinh nhằm sàng lọc và tăng sinh tế bào CAR-T. Tuy nhiên, những nỗ lực này cho kết quả chuyển gen thấp, cho đến khi hệ thống Sleeping Beauty ra đời. Nghiên cứu của Huang và CS tại trường Đại học Minnesota [5] và Singh và CS tại Trung tâm Ung thư MD Anderson [6] chỉ ra tất cả các lợi thế của việc sử dụng hệ thống chuyển vị SB so với các phương pháp virus được sử dụng phổ biến hoặc các vector DNA trần khác. Ngoài ra, plasmid transposase thế hệ mới SB100X ra đời giúp cải thiện đáng kể hiệu suất chuyển nạp vào tế bào T nói riêng và PBMC nói chung [7], cho thấy hiệu quả chuyển nạp cao hơn 10 - 100 lần so với plasmid SB11 thế hệ cũ. Chất lượng và số lượng PBMC được phân lập từ máu toàn phần tác động đáng kể đến quá trình chuyển nạp và tăng sinh tế bào CAR-T sau đó [8]. Do đó, chúng tôi thực hiện tối ưu hóa quá trình tách PBMC từ máu ngoại vi của người hiến khỏe mạnh. Phương pháp tiêu chuẩn cho tách PBMC từ máu ngoại vi hiện nay vẫn là ly tâm mật độ trên môi trường tỷ trọng (Ficoll polysaccharide). Kết quả cho thấy tỷ lệ pha loãng máu ngoại vi ≥ 2 lần trước khi ly tâm cho hiệu suất thu hồi tế bào > 60% và tỷ lệ tế bào sống khoảng 95%. Kết quả này tương tự với các nghiên cứu đã được công bố trên thế giới, với khuyến cáo thực hiện pha loãng máu ngoại vi trước khi ly tâm tỷ trọng [9]. Trong nghiên cứu, chúng tôi tiến hành tối ưu hóa phản ứng chuyển nạp vào PBMC từ máu ngoại vi của người khỏe mạnh. Kết quả cho thấy điều kiện chuyển gen tối ưu đạt được khi sử dụng hệ thống Nucleofector 2b, chương trình xung điện U-014, bộ kít chuyển nạp Human T Cell Nucleofector, 2 × 107 tế bào/phản ứng, 1 µg SB100X và 10 µg pSB-CAR19. Ngoài ra, hiệu suất chuyển nạp đạt được tương đương với một số công bố quốc tế trong cùng lĩnh vực [10]. T¹p chÝ y - d−îc häc qu©n sù sè 4-2021 94 KẾT LUẬN Tối ưu hóa thành công quá trình tách PBMC và chuyển nạp tạo khối tế bào CAR-T hướng đích CD19 cho điều trị lơ- xê-mi cấp dòng lympho. TÀI LIỆU THAM KHẢO 1. Jemal A, Siegel R, Xu J, Ward E. Cancer statistics. CA Cancer J Clin 2010; 60(5):277-300. 2. Terwilliger T, Abdul-Hay M. Acute lymphoblastic leukemia: A comprehensive review and 2017 update. Blood Cancer Journal 2017; 7(6):e577-e577. doi:10.1038/bcj.2017.53. 3. Hunger SP, Mullighan CG. Acute lymphoblastic leukemia in children. N Engl J Med 2015; 373(16):1541-1552. doi:10.1056/ NEJMra1400972. 4. Singh H, Figliola MJ, Dawson MJ, Olivares S, Zhang L, Yang G, et al. Manufacture of clinical-grade CD19-specific T cells stably expressing chimeric antigen receptor using Sleeping Beauty system and artificial antigen presenting cells. PLOS ONE 2013; 8(5):e64138. doi:10.1371/journal.pone.0064138. 5. Huang X, Guo H, Kang J, Choi S, Zhou TC, Tammana S, et al. Sleeping Beauty Transposon‐ mediated engineering of human primary T cells for therapy of CD19+ lymphoid malignancies. Molecular Therapy 2008; 16(3):580-589. doi:10.1038/sj.mt.6300404. 6. Singh H, Manuri PR, Olivares S, Dara N, Dawson MJ, Huls H, et al. Redirecting specificity of T-cell populations for CD19 using the Sleeping Beauty system. Cancer Res 2008; 68(8): 2961-2971. doi:10.1158/0008- 5472.Can-07-5600. 7. Jin Z, Maiti S, Huls H, Singh H, Olivares S, Mátés L, et al. The hyperactive Sleeping Beauty transposase SB100X improves the genetic modification of T cells to express a chimeric antigen receptor. Gene Therapy 2011; 18(9):849-856. doi:10.1038/gt.2011.40. 8. Nazarpour R, Zabihi E, Alijanpour E, Abedian Z, Mehdizadeh H, Rahimi F. Optimization of human peripheral blood mononuclear cells (PBMCs) cryopreservation. International Journal of Molecular and Cellular Medicine 2012; 1(2):88-93. 9. Kleiveland CR. Peripheral blood mononuclear cells. In K Verhoeckx, P Cotter, I López-Expósito, C Kleiveland, T Lea, A Mackie, T Requena, D Swiatecka, H Wichers (Eds.). The impact of food bioactives on health: In vitro and ex vivo models (pp.161-167). Cham: Springer International Publishing 2015. 10. Chicaybam L, Abdo L, Viegas M, Marques LVC, de Sousa P, Batista-Silva LR, et al. Transposon-mediated generation of CAR- T cells shows efficient anti B-cell leukemia response after ex vivo expansion. Gene Therapy 2020; 27(1):85-95. doi:10.1038/ s41434-020-0121-4. KẾT QUẢ ĐIỀU TRỊ GIÃN NÃO THẤT BẰNG PHẪU THUẬT DẪN LƯU NÃO THẤT Ổ BỤNG Ngô Mạnh Hùng1 TÓM TẮT Mục tiêu: Đánh giá kết quả điều trị phẫu thuật dẫn lưu não thất ổ bụng trong điều trị giãn não thất (GNT) ở người trưởng thành. Đối tượng và phương pháp: Nghiên cứu mô tả, cắt
File đính kèm:
 nghien_cuu_toi_uu_hoa_qua_trinh_tach_te_bao_don_nhan_mau_ngo.pdf
nghien_cuu_toi_uu_hoa_qua_trinh_tach_te_bao_don_nhan_mau_ngo.pdf

