Bài giảng Hóa đại cương - Chương 13: Cân bằng ion của nước - Huỳnh Kỳ Phương Hạ
LÝ THUYẾT ACID - BASE
• THUYẾT ACID – BASE BRONSTED-LOWRY
• Dựa trên tính chất proton, H+: không có lớp vỏ
electron, chỉ là hạt nhân nên kích thước rất nhỏ, H+
có thể xâm nhập sâu vào lớp vỏ của các ion, phân
tử khác để thưc hiện phản ứng trao đổi ion.
• ĐỊNH NGHĨA:
• Acid là tiểu phân cho proton, còn base là tiểu phân
nhận proton trong phản ứng.

Trang 1

Trang 2

Trang 3

Trang 4

Trang 5
Trang 6

Trang 7

Trang 8

Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa đại cương - Chương 13: Cân bằng ion của nước - Huỳnh Kỳ Phương Hạ", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa đại cương - Chương 13: Cân bằng ion của nước - Huỳnh Kỳ Phương Hạ

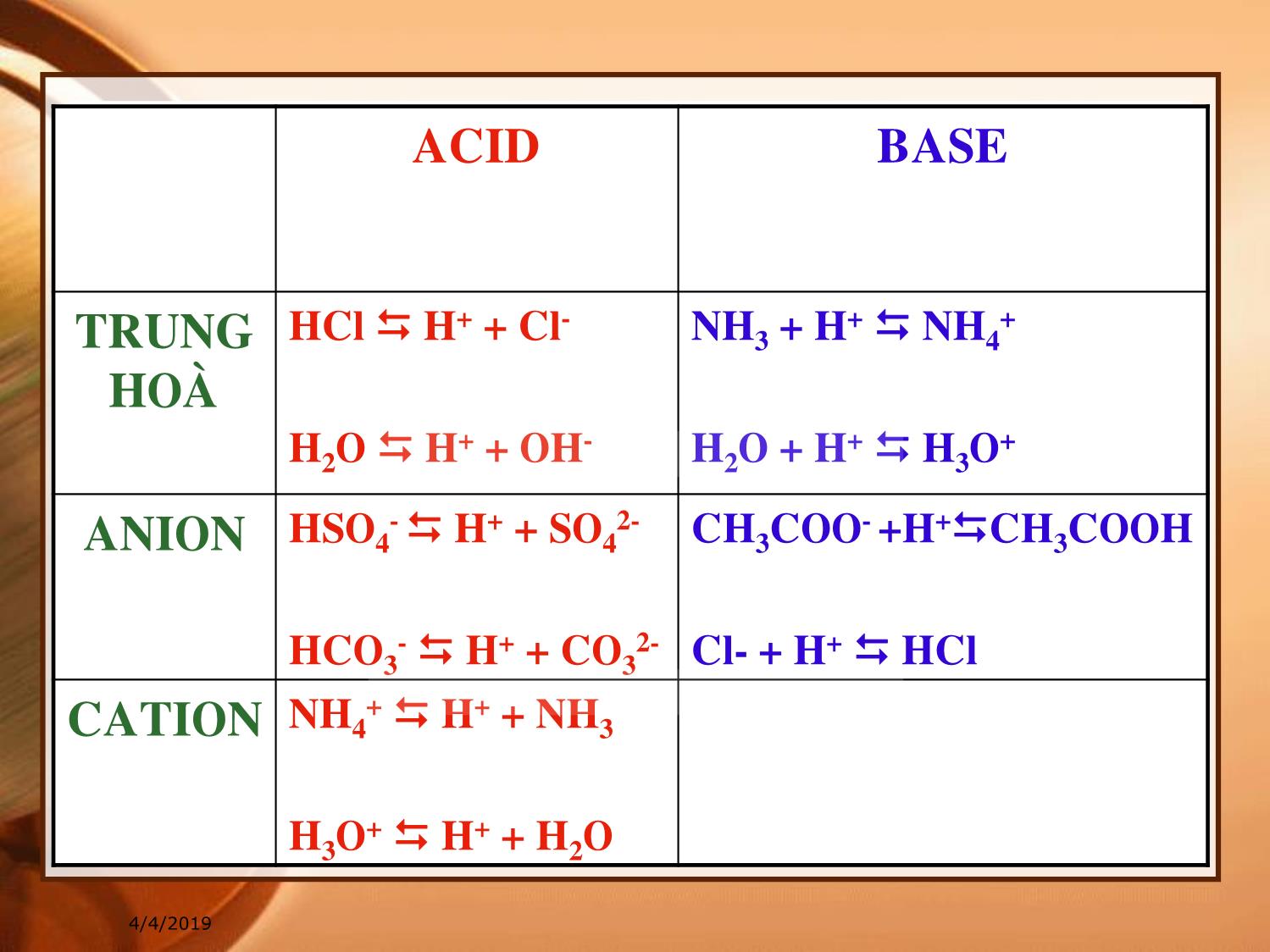
4/4/2019 Chương 13 CÂN BẰNG ION CỦA NƯỚC 4/4/2019 SỰ ĐIỆN LY CỦA NƯỚC VÀ TÍCH SỐ ION CỦA NƯỚC • Nước là chất điện ly yếu H 2 O (l) H+ + OH- Hằng số điện ly của nước Ở 22 0 C Do độ điện ly của nước quá nhỏ nên nồng độ của H 2 O xem như không đổi: OH OHH OH C CC K 2 2 16 1081 2 .K OH OHH OHOH CCconstCK 22 4/4/2019 • Tích số ion của nước: K n • Ở 220C, ta có: • Môi trường axit có • Môi trường bazơ có • Môi trường trung tính có OHH n CCK 1416 10 18 1000 1081 22 .CKK oHOHn 77 1010 OHH C,C 77 1010 OHH C,C 77 1010 OHH C,C 4/4/2019 LÝ THUYẾT ACID - BASE • THUYẾT ACID – BASE BRONSTED-LOWRY • Dựa trên tính chất proton, H+: không có lớp vỏ electron, chỉ là hạt nhân nên kích thước rất nhỏ, H + có thể xâm nhập sâu vào lớp vỏ của các ion, phân tử khác để thưc hiện phản ứng trao đổi ion. • ĐỊNH NGHĨA: • Acid là tiểu phân cho proton, còn base là tiểu phân nhận proton trong phản ứng. 4/4/2019 • Ví dụ: HCl H+ + Cl- H 2 SO 4 H+ + HSO 4 - • Vì acid là chất nhường H+ và base nhận H+, nên trong 2 ví dụ trên ta có các cặp acid, base: HCl/Cl - và H 2 SO 4 /HSO 4 - Những cặp acid/base như vậy gọi là cặp acid/base liên hợp. Các acid, base Bronsted có thể là phân tử trung hoà, cation hoặc anion. 4/4/2019 ACID BASE TRUNG HOÀ HCl H+ + Cl- H 2 O H+ + OH- NH 3 + H + NH 4 + H 2 O + H + H 3 O + ANION HSO4 - H+ + SO 4 2- HCO 3 - H+ + CO 3 2- CH 3 COO - +H + CH 3 COOH Cl- + H + HCl CATION NH4 + H+ + NH 3 H 3 O + H+ + H 2 O 4/4/2019 • Do H+ không tồn tại được ở dạng tự do, nên các acid chỉ cho proton khi có base nhận và ngược lại. • Phản ứng trao đổi proton xảy ra tổng quát giữa hai cặp acid-base liên hợp như sau: A 1 + B 2 A 2 + B 1 4/4/2019 Trong dung dịch, các phân tử và ion do dung môi điện ly ra cũng đóng vai trò của cặp acid-base liên hợp. H 3 O + /H 2 O; H 2 O/OH - Các hợp chất có chứa H + luôn là chất lưỡng tính, phụ thuộc vào chất phản ứng với nó có khả năng cho, nhận H + mạnh hay yếu hơn nó. 4/4/2019 THUYẾT ACID – BASE LEWIS • ĐỊNH NGHĨA: • Base là chất cho cặp electron và acid là chất nhận cặp electron để tạo thành liên kết hóa học. • Khái niệm này liên quan đến liên kết cộng hóa trị cho – nhận. • Acid Lewis: • Là những tiểu phân có dư mật độ điện tích dương, trong phân tử (ion) có các orbital trống có thể tiếp nhận cặp e chuyển đến từ base. 4/4/2019 • Ví dụ: Đa số các cation là acid Lewis (Ag+, Co3+, Cr 3+), hay các halogen, hydrua của B, Al • Base Lewis: • Là những tiểu phân có khả năng cho đi cặp e. Ví dụ: Các anion (Cl - , Br - , OH -), các phân tử trung hoà hoặc ion trong thành phần có các nguyên tử còn cặp e chưa liên kết như N, O (NH 3 , rượu, cetone). Ag + + NH 3 [Ag(NH 3 ) 2 ] + Acid Base BF 3 + F - [BF 4 ] - HCl + NH 3 NH 4 Cl 4/4/2019 CHỈ SỐ HYDRO (pH) • Quy ước: • Trong các dung dịch có nồng độ cao hoặc các dung dịch axit bazơ mạnh thì: • Môi trường axit pH 7 trung tính pH = 7 • Ta có: hay KpK OHpOHHpH lg lg,lg H algpH OH H C C 14 10 14pOHpH 4/4/2019 TÍNH pH CỦA CÁC DUNG DỊCH ĐIỆN LY • pH CỦA DUNG DỊCH ACID MẠNH • Acid mạnh điện ly hoàn toàn HA H + + A - a H HA ClgClgpHCH 4/4/2019 pH ACID YẾU ĐƠN BẬC HA H+ + A- Lúc đầu C a 0 0 Cân bằng C a -x x x Hằng số cân bằng điện ly được gọi là hằng số axit, K a Do acid yếu HA AH a C CC K HCKxCxCCx aaaaa aa ClgKlgHlgpH 2 1 4/4/2019 • pH DUNG DỊCH ACID YẾU ĐA BẬC • Do K 1 >>K 2 >>K 3 (ví dụ với H 3 PO 4 , K 1 =10 -2,12 , K 2 =10 -7.21 , K 3 =10 -12.38 ), do đó để tính pH, ta chỉ tính cho bậc phân ly đầu. Nên cách tính cũng giống trường hợp acid yếu đơn bậc. • pH DUNG DỊCH BASE MẠNH MOH M+ + OH- C OH- C b a ClgKlgpH 1 2 1 bb OH ClgpHClgClgpOH 14 4/4/2019 • pH DUNG DỊCH BASE YẾU ĐƠN BẬC • Lập luận tương tự trường hợp acid yếu đơn bậc. Ta có: • pH DUNG DỊCH BASE YẾU ĐA BẬC bb ClgKlgpOH 2 1 bb ClgKlgpH 2 1 14 bbbb ClgKlgpHClgKlgpOH 1 2 1 14 2 1 1 MOH OHM b C CC K 4/4/2019 CHẤT CHỈ THỊ MÀU • Chất chỉ thị màu có nhiều loại: Chất chỉ thị màu pH, chỉ thị màu Oxy hóa – khử, chỉ thị màu phứcỞ đây ta xét chất chỉ thị màu pH. • Chất chỉ thị màu pH là các hợp chất hoá học có khả năng thay đổi màu theo pH (theo nồng độ H 3 O + , hay H + -theo Arrhenius). Thường đây là các acid hay base hữu cơ yếu. 4/4/2019 • Ký hiệu chất chỉ thị màu Acid yếu là HInd HInd H+ + Ind- Màu dạng acid Màu dạng base Ký hiệu chất chỉ thị màu là Base yếu là IndOH IndOH OH- + Ind+ Màu dạng base Màu dạng acid Màu dạng acid khác với màu dạng base. • Ví dụ: phenolphthalein (HP) hay quì tím (HQ) HP H+ + P- Acid không màu Base màu hồng HQ H+ + Q- Acid màu đỏ Base màu xanh 4/4/2019 Hằng số điện ly của chất chỉ thị màu Chuyển qua pH C H+ tăng thì màu dạng axit chiếm ưu thế, pH giảm thì ngược lại. azơMàudạngB xitMàudạngA K C C KC C CC K Ind Ind HInd Ind H HInd IndH Ind HInd Ind Ind C C lgpKpH 4/4/2019 DUNG DỊCH ĐỆM • Định nghĩa: Dung dịch đệm là dung dịch có giá trị pH xác định và hầu như không thay đổi khi pha loãng, hay thêm vào một lượng nhỏ acid hoặc base mạnh. • Nói chung dung dịch đệm được tạo thành bằng cách trộn một acid yếu với muối của nó (hệ đệm acid) hoặc trộn một base yếu với muối của nó (hệ đệm base). • Ví dụ: • Hệ đệm acid: CH 3 COOH + CH 3 COONa • Hệ đệm base: NH 4 OH + NH 4 Cl 4/4/2019 Cơ chế tác dụng của dung dịch đệm • Xét hệ: CH 3 COOH CH 3 COO - + H + (1) CH 3 COONa CH 3 COO - + Na + (2) Khi thêm acid mạnh: HA H + + A - thì theo nguyên lý Le Chatelier cân bằng (1) sẽ dịch chuyển theo chiều nghịch (tức là H + tác dụng với CH 3 COO - ở (2) tạo CH 3 COOH) làm giảm H + . 4/4/2019 Khi thêm base mạnh: MOH M + + OH - , thì OH - sẽ kết hợp với H + (ở cân bằng 1) làm giảm nồng độ OH - , đồng thời cân bằng (1), do bị giảm H + , cũng sẽ dịch chuyển theo chiều thuận để tạo ra H + . Với hệ đệm base lập luận tương tự. Tóm lại, khi cho H + hay OH - vào hệ đệm thì pH dung dịch thay đổi rất ít. 4/4/2019 TÍNH pH DUNG DỊCH ĐỆM • Hệ đệm acid • Ví dụ hệ acetate trên, gọi C m và C a là nồng độ muối và acid. • Khi hệ đã đạt trạng thái cân bằng (ở 1), ta có: • Trong đó,vì nồng độ muối không có cách biệt lớn so với nồng độ acid, mà acid là chất kém điện ly, do đó • [CH 3 COO - ] = C m + C a C m (vì <<1) COOCH COOHCH aH C C KC 3 3 4/4/2019 • Cũng vì acid kém điện ly, <<1: • Thay vào công thức tính [H+] để tính pH, ta có: aaaCOOHCH C.CCC 3 a m a m a ah C C pKpH C C KC lg 4/4/2019 • Hệ đệm base • Lý luận tương tự trên, ta có: • Pha chế dung dịch đệm: • Trước hết chọn axit hoặc bazơ có pK a , 14-pK b gần với pH cần có, sau đó tính tỉ số nồng độ muối và acid (base) để có pH cần thiết. b m b C C lgpKpH 14 4/4/2019 Indicator Low pH color Transition pH range High pH color Gentian violet (Methyl violet) yellow 0.0–2.0 blue-violet Leucomalachite green (first transition) yellow 0.0–2.0 green Thymol blue (first transition) red 1.2–2.8 yellow Methyl yellow red 2.9–4.0 yellow Bromophenol blue yellow 3.0–4.6 purple Congo red blue-violet 3.0–5.0 red Methyl orange red 3.1–4.4 yellow Bromocresol green yellow 3.8–5.4 blue-green Methyl red red 4.4–6.2 yellow Azolitmin red 4.5–8.3 blue Bromocresol purple yellow 5.2–6.8 purple Bromothymol blue yellow 6.0–7.6 blue Phenol red yellow 6.8–8.4 red Neutral red red 6.8–8.0 yellow Naphtholphthalein colorless to reddish 7.3–8.7 greenish to blue Cresol Red yellow 7.2–8.8 reddish-purple Thymol blue (second transition) yellow 8.0–9.6 blue Phenolphthalein colorless 8.2–10.0 pink Thymolphthalein colorless 9.3–10.5 blue Alizarine Yellow R yellow 10.2–12.0 red Leucomalachite green (second transition) green 11.6–14 colorless
File đính kèm:
 bai_giang_hoa_dai_cuong_chuong_13_can_bang_ion_cua_nuoc_huyn.pdf
bai_giang_hoa_dai_cuong_chuong_13_can_bang_ion_cua_nuoc_huyn.pdf

