Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 MG bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC)
Nghiên cứu hướng đến mục tiêu là xây dựng và thẩm định quy trình phân tích định lượng
hoạt chất cefixim trong viên nang cứng cefixim 100 mg bằng phương pháp sắc ký lỏng hiệu
năng cao (HPLC) theo tiêu chuẩn dược điển USP 34. Quá trình sắc ký được thực hiện trên cột
HiQ Sil C18HS 4,6 mm (I.D) x 100 mm (L), phát hiện bằng đầu dò diod quang (PDA) ở bước
sóng 254 nm. Quá trình rửa giải đẳng dòng với pha động gồm acetonitril : tetrabutylamonium
hydroxyd theo tỷ lệ 1:3, tốc độ dòng là 1,1 mL/phút. Mẫu được hòa tan trong dung dịch đệm
phosphat pH 7,0. Độ tuyến tính của phương pháp đạt trong khoảng nồng độ 0,04-0,4 mg/mL.
Giới hạn phát hiện (LOD) là 0,003 mg/mL, giới hạn định lượng (LOQ) là 0,01 mg/mL. Độ
đúng của phương pháp được xác định bằng % tỷ lệ phục hồi trong khoảng 99,72-101,25%. Độ
chính xác gồm độ lặp lại có %RSD = 0,062% và độ chính xác trung gian được thực hiện bởi
2 kiểm nghiệm viên có %RSD = 0,063%. Các kết quả khảo sát đều đạt yêu cầu về các chỉ tiêu
tính đặc hiệu, độ tuyến tính, độ đúng, độ chính xác, giới hạn phát hiện (LOD) và giới hạn định
lượng (LOQ). Phương pháp đề xuất này có thể áp dụng để xác định hàm lượng cefixime trong
công thức dược phẩm.

Trang 1

Trang 2

Trang 3

Trang 4

Trang 5
Trang 6

Trang 7
Trang 8
Trang 9

Trang 10
Tóm tắt nội dung tài liệu: Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 MG bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC)

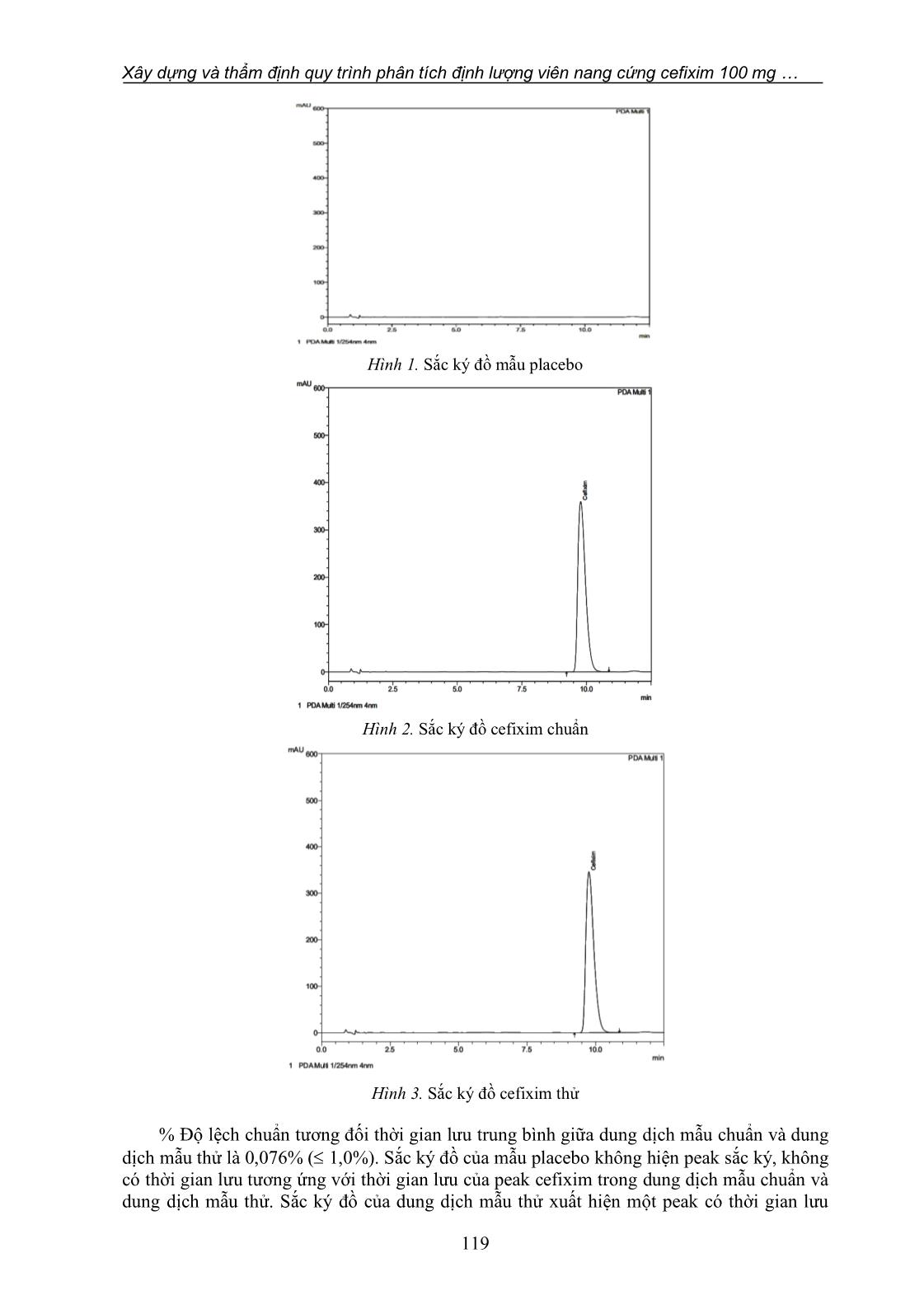
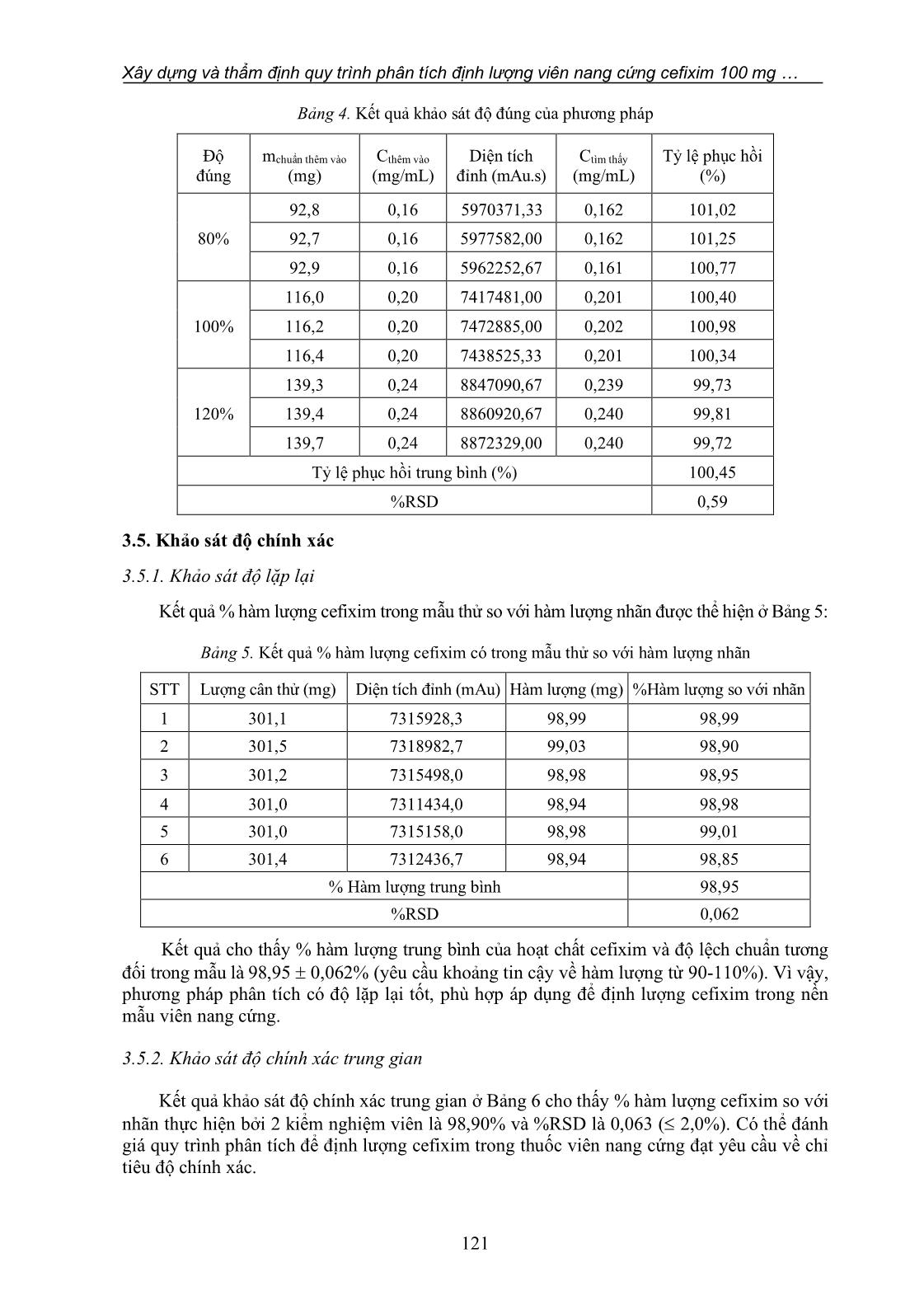
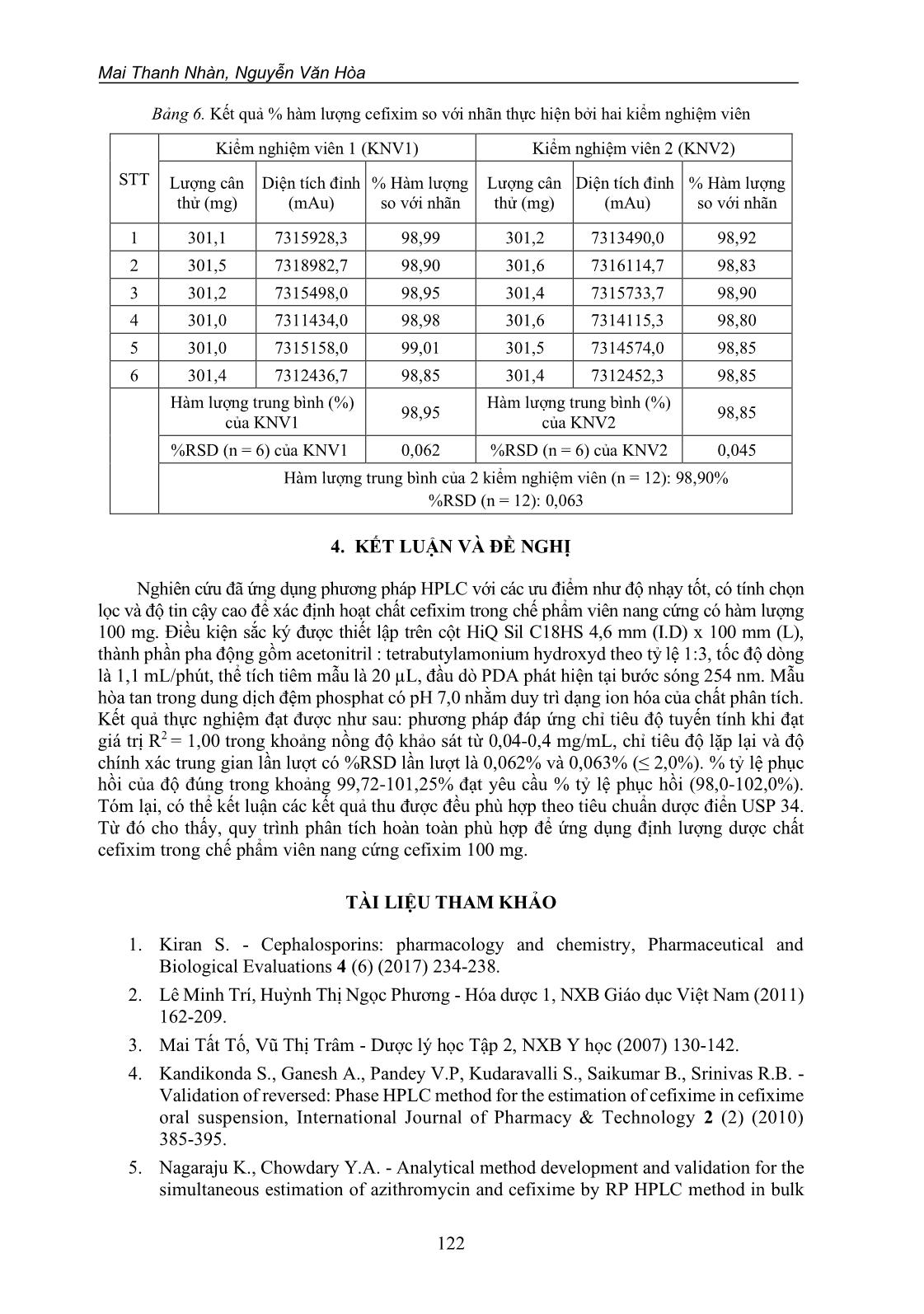
Tạp chí Khoa học Công nghệ và Thực phẩm 21 (2) (2021) 114-123 114 XÂY DỰNG VÀ THẨM ĐỊNH QUY TRÌNH PHÂN TÍCH ĐỊNH LƯỢNG VIÊN NANG CỨNG CEFIXIM 100 MG BẰNG PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO (HPLC) Mai Thanh Nhàn1*, Nguyễn Văn Hòa2 1Trường Đại học Nguyễn Tất Thành 2Trường Đại học Công nghiệp Thực phẩm TP.HCM *Email: mtnhan@ntt.edu.vn Ngày nhận bài: 08/10/2020; Ngày chấp nhận đăng: 01/3/2021 TÓM TẮT Nghiên cứu hướng đến mục tiêu là xây dựng và thẩm định quy trình phân tích định lượng hoạt chất cefixim trong viên nang cứng cefixim 100 mg bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC) theo tiêu chuẩn dược điển USP 34. Quá trình sắc ký được thực hiện trên cột HiQ Sil C18HS 4,6 mm (I.D) x 100 mm (L), phát hiện bằng đầu dò diod quang (PDA) ở bước sóng 254 nm. Quá trình rửa giải đẳng dòng với pha động gồm acetonitril : tetrabutylamonium hydroxyd theo tỷ lệ 1:3, tốc độ dòng là 1,1 mL/phút. Mẫu được hòa tan trong dung dịch đệm phosphat pH 7,0. Độ tuyến tính của phương pháp đạt trong khoảng nồng độ 0,04-0,4 mg/mL. Giới hạn phát hiện (LOD) là 0,003 mg/mL, giới hạn định lượng (LOQ) là 0,01 mg/mL. Độ đúng của phương pháp được xác định bằng % tỷ lệ phục hồi trong khoảng 99,72-101,25%. Độ chính xác gồm độ lặp lại có %RSD = 0,062% và độ chính xác trung gian được thực hiện bởi 2 kiểm nghiệm viên có %RSD = 0,063%. Các kết quả khảo sát đều đạt yêu cầu về các chỉ tiêu tính đặc hiệu, độ tuyến tính, độ đúng, độ chính xác, giới hạn phát hiện (LOD) và giới hạn định lượng (LOQ). Phương pháp đề xuất này có thể áp dụng để xác định hàm lượng cefixime trong công thức dược phẩm. Từ khóa: Cefixim, HPLC, sắc ký ghép cặp ion, thẩm định quy trình. 1. GIỚI THIỆU Cefixim là một kháng sinh bán tổng hợp thuộc nhóm Cephalosporin thế hệ 3 với nhiều ưu điểm nổi bật. Hiệu quả kháng khuẩn của cefixim dựa trên khả năng ức chế quá trình tổng hợp thành tế bào của vi khuẩn. Cụ thể là cefixim ức chế hoạt động của men transpeptidase, là enzym tham gia vào quá trình tổng hợp peptidoglycan. Thành tế bào là một phần không thể thiếu trong cấu trúc của vi khuẩn, giúp vi khuẩn sống sót ở điều kiện môi trường không thuận lợi, nếu không có vách tế bào, vi khuẩn sẽ chết [1]. Sự hiện diện của dị vòng 2-amino thiazolyl và nhóm acid acetic oxy-imine làm cho Cefixim có hoạt tính kháng khuẩn mạnh, ngoài ra còn có nhóm vinyl giúp cefixim được hấp thu nguyên vẹn qua ruột bằng đường uống [2]. Bên cạnh các ưu điểm chung của nhóm Cephalosporin như ít độc, nguy cơ dị ứng thấp và có hiệu quả cao trong điều trị các bệnh nhiễm khuẩn, thì cefixim còn được ưa chuộng vì có thể sử dụng bằng đường uống và phổ kháng khuẩn rộng, nên thuốc cho hiệu quả điều trị cao [3]. Trên cơ sở đó, nhiều công trình nghiên cứu khoa học nhằm thẩm định, đánh giá cefixim đã được tiến hành trong khoảng 10 năm trở lại đây. Năm 2010, Kandikonda và cộng sự đã ứng dụng phương pháp HPLC để thẩm định cefixim trong thuốc hỗn dịch [4]. Năm 2018, Nagaraju và cộng sự tiến hành nghiên cứu phân tích và định lượng đồng thời cefixim và azithromycin Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg 115 trong chế phẩm dược bằng phương pháp HPLC. Nghiên cứu đã chứng minh tính hiệu quả và chính xác của phương pháp HPLC trong việc phân tích các hoạt chất dược phẩm [5]. Qua các nghiên cứu trên, có thể nhận thấy rằng phương pháp HPLC nổi bật lên với nhiều ưu điểm và có khả năng đáp ứng yêu cầu phân tích cefixim. Chính vì thế, nhóm tác giả thực hiện nghiên cứu: “Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC)” với mục tiêu thẩm định lại quy trình định lượng cefixim theo tiêu chuẩn USP 34 để phù hợp với đối tượng mẫu (viên nang cứng) và điều kiện phòng thí nghiệm, từ đó cung cấp dữ liệu cho việc áp dụng quy trình phân tích này tại các cơ sở sản xuất dược phẩm trong nước. 2. VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU 2.1. Nguyên vật liệu và thiết bị 2.1.1. Nguyên vật liệu - Cefixim chuẩn: Cefixim hàm lượng nguyên trạng 86,17% (Viện Kiểm nghiệm thuốc Trung ương). - Cefixim thử: viên nang cứng A100 chứa hoạt chất cefixim, hàm lượng 100 mg, số đăng ký VD - 20173 - 13, số lô 030718. - Dung môi: Acetonitril, tetrabutylamonium hydroxyd, đệm phosphat pH 7,0 (Merck, Mỹ). - Dung dịch mẫu chuẩn: Cân chính xác 40 mg cefixim chuẩn vào bình định mức 100 mL, thêm 70 mL dung dịch đệm pH 7,0, siêu âm để hòa tan và pha loãng bằng dung dịch đệm đến vạch, trộn và ly tâm. Sau đó, hút chính xác 10 mL dung dịch này cho vào bình định mức 20 mL và pha loãng với đệm đến vạch, trộn đều. Lọc qua màng lọc milipore 0,45 µm [6]. - Dung dịch mẫu thử: Cân chính xác một lượng thuốc bột tương ứng với 100 mg cefixim thử vào bình định mức 100 mL, thêm 75 mL dung dịch đệm phosphat pH 7,0, siêu âm để hòa tan và pha loãng bằng dung dịch đệm vừa đủ đến vạch, trộn và ly tâm. Hút chính xác 10 mL dung dịch này vào bình định mức 50 mL và pha loãng bằng dung dịch đệm vừa đủ đến vạch, trộn đều. Lọc qua màng lọc milipore 0,45 µm [6]. - Dung dịch mẫu placebo: Tạo mẫu placebo tá dược tương ứng với 20 viên, trộn đều. Cân chính xác 301 mg bột placebo cho vào bình định mức 100 mL, thêm 75 mL dung dịch đệm phosphat pH 7,0, siêu âm để hòa tan và pha loãng bằng dung dịch đệm vừa đủ đến vạch, trộn và ly tâm. Hút chính xác 10 mL dung dịch này vào bình định mức 50 mL và pha loãng bằng dung dịch đệm vừa đủ đến vạch, trộn đều. Lọc qua màng lọc milipore 0,45 µm [6]. 2.1.2. Thiết bị - Bộ lọc chân không Glassco. - Màng lọc 0,45 µm Syringe Millex-HV Filter Uni. - Máy siêu âm Daihan Labtech LUC-420. - Máy đo pH điện cực thủy tinh Mettler Toledo S220-K. - Cân phân tích 4 số lẻ GS Shinko GS-623W. - Máy sắc ký lỏng Shimadzu LC-20A. Điều kiện sắc ký gồm có: Cột: HiQ Sil C18HS 4,6 mm (I.D) x 100 mm (L), đầu dò PDA: 254 nm, tốc độ dòng: 1,1 mL/phút, thể tích tiêm: 20 µL, nhiệt độ cột: 40 °C, thành ... ng dãy chuẩn có 5 nồng độ khác nhau 0,04; 0,1; 0,2; 0,3 và 0,4 mg/mL để xác định khoảng tuyến tính. Tiến hành tiêm mẫu, mỗi nồng độ tiêm 3 lần, lấy kết quả trung bình và vẽ đồ thị khảo sát sự tương quan giữa đại lượng y (diện tích đỉnh trung bình mỗi mẫu dung dịch chuẩn) và x (nồng độ cefixim). Kết quả đạt tiêu chuẩn nếu giá trị của hệ số tương quan: 0,99 ≤ R2 ≤ 1. Dựa trên độ tuyến tính, xác định giá trị LOD và LOQ theo công thức: Giới hạn phát hiện (LOD): LOD = 3.3 ×S a Giới hạn định lượng (LOQ): LOQ = 10 ×S a Trong đó: S là độ lệch chuẩn; a là hệ số gốc của đường thẳng y = ax + b. 2.2.4. Khảo sát độ đúng Độ đúng là mức độ gần sát của giá trị tìm thấy so với giá trị thực, chịu ảnh hưởng của sai số hệ thống và được biểu thị bằng % tỷ lệ phục hồi của giá trị tìm thấy sau khi thêm chất chuẩn vào mẫu placebo. Cách tiến hành: chuẩn bị 9 mẫu thử placebo, thêm chính xác khoảng 80%; 100%; 120% cefixim chuẩn vào mẫu placebo (so với nồng độ lí thuyết), mỗi nồng độ chuẩn bị 3 mẫu. Sau đó, tiêm 20 L các dung dịch mẫu vào hệ thống sắc ký, mỗi mẫu tiêm 3 lần. Dựa vào kết quả thu được, tính % tỷ lệ độ phục hồi của các mẫu thử tại mỗi nồng độ [6]. Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg 117 Kết quả đạt tiêu chuẩn nếu phù hợp yêu cầu: tỷ lệ phục hồi trong khoảng 98,0-102,0%. Tỷ lệ phục hồi (%) được tính theo công thức: 𝑀 𝑚 × 100% Trong đó: M là lượng cefixim tìm thấy (mg/mL); m là lượng cefixim thêm vào (mg/mL). 2.2.5. Khảo sát độ chính xác 2.2.5.1. Khảo sát độ lặp lại Độ lặp lại là độ chính xác được khảo sát trong các điều kiện giống nhau (phương pháp, phòng thí nghiệm, người phân tích, dụng cụ). Cách tiến hành: thực hiện như quy trình định lượng trên dung dịch mẫu thử (6 lần) và tính % hàm lượng cefixim trong chế phẩm so với hàm lượng nhãn. Xác định các giá trị theo công thức: Giá trị trung bình: 6 1 == n i ix X Độ lệch chuẩn (Standard Deviation): 5 )( 1 2 = − == n i i xx SSD Độ lệch chuẩn tương đối (Relative Standard Deviation) hay hệ số phân tán (Coefficient of Variation): %100 == X S CVRSD % Hàm lượng cefixim trong chế phẩm so với hàm lượng nhãn được tính theo công thức: %Hàm lượng = ST SC × mC × P 100 × ĐPLT ĐPLC × mTB mT × 100 HLN Trong đó: - SC, ST: diện tích đỉnh mẫu chuẩn, thử. - mTB: khối lượng trung bình của 20 viên nang cứng (mg). - mC, mT: khối lượng cân của mẫu chuẩn, thử (mg). - P: hàm lượng nguyên trạng chuẩn cefixim là 86,17%. - ĐPLC, ĐPLT: độ pha loãng lần lượt của mẫu chuẩn, thử. - HLN: hàm lượng nhãn cefixim 100 (mg). Kết quả đạt tiêu chuẩn nếu phù hợp yêu cầu: % hàm lượng hoạt chất cefixim trong chế phẩm khoảng 90-110%. 2.2.5.2. Khảo sát độ chính xác trung gian Cách tiến hành: thực hiện tương tự như độ lặp lại, nhưng với các điều kiện sau: cùng mẫu thử (lô chế phẩm) và định lượng 6 lần nhưng khác ngày phân tích và khác kiểm nghiệm viên. Mai Thanh Nhàn, Nguyễn Văn Hòa 118 Xác định giá trị trung bình và % độ lệch chuẩn tương đối (%RSD) của hàm lượng hoạt chất có trong các mẫu do mỗi kiểm nghiệm viên phân tích và giữa hai kiểm nghiệm viên. Kết quả đạt tiêu chuẩn nếu phù hợp yêu cầu: %RSD 2,0%. 3. KẾT QUẢ NGHIÊN CỨU 3.1. Khảo sát tính tương thích hệ thống Kết quả khảo sát tính tương thích của hệ thống khi tiêm lặp 6 lần dung dịch chuẩn cefixim có nồng độ 0,2 mg/mL vào hệ thống máy sắc ký lỏng, sau đó ghi nhận lại hình dạng và kết quả sắc ký đồ được thể hiện ở Bảng 1: Bảng 1. Kết quả khảo sát tính tương thích hệ thống STT Thời gian lưu (phút) Diện tích đỉnh (mAu.s) Số đĩa lý thuyết Hệ số kéo đuôi 1 9,777 7407002 5277,430 1,630 2 9,781 7422778 5293,600 1,628 3 9,785 7424494 5269,994 1,645 4 9,770 7420065 5304,544 1,621 5 9,772 7421748 5319,229 1,619 6 9,769 7421308 5320,160 1,617 TB 9,776 7419565 5297,500 1,627 %RSD 0,07 0,09 0,40 0,63 Kết quả khảo sát tính tương thích hệ thống ở Bảng 1 cho thấy phần trăm độ lệch chuẩn tương đối của 6 lần tiêm lặp %RSD = 0,07% ( 2,0%). Hệ số kéo đuôi của các peak sắc ký khoảng 1,617-1,645 (khoảng chấp nhận 0,9 ≤ AS ≤ 2,0), số đĩa lý thuyết là 5297,500 (≥ 4000 đĩa). Vì vậy, phương pháp đạt về tính tương thích hệ thống. 3.2. Khảo sát tính đặc hiệu Kết quả khảo sát cho thấy, trên sắc ký đồ của mẫu giả dược (placebo) không xuất hiện peak sắc ký, sắc ký đồ giữa mẫu thử và mẫu chuẩn lần lượt cho peak sắc ký tương ứng với thời gian lưu (Bảng 2). Sắc ký đồ mẫu placebo, mẫu chuẩn và mẫu thử được thể hiện lần lượt ở Hình 1, 2 và 3. Bảng 2. Giá trị thời gian lưu mẫu chuẩn và mẫu thử STT Thời gian lưu mẫu chuẩn (phút) Thời gian lưu mẫu thử (phút) 1 9,777 9,761 2 9,781 9,764 3 9,785 9,759 4 9,770 9,760 5 9,772 9,780 6 9,767 9,760 TB 9,775 9,764 %RSD 0,07 0,082 %RSD trung bình của mẫu chuẩn và mẫu thử: 0,076 Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg 119 Hình 1. Sắc ký đồ mẫu placebo Hình 2. Sắc ký đồ cefixim chuẩn Hình 3. Sắc ký đồ cefixim thử % Độ lệch chuẩn tương đối thời gian lưu trung bình giữa dung dịch mẫu chuẩn và dung dịch mẫu thử là 0,076% ( 1,0%). Sắc ký đồ của mẫu placebo không hiện peak sắc ký, không có thời gian lưu tương ứng với thời gian lưu của peak cefixim trong dung dịch mẫu chuẩn và dung dịch mẫu thử. Sắc ký đồ của dung dịch mẫu thử xuất hiện một peak có thời gian lưu Mai Thanh Nhàn, Nguyễn Văn Hòa 120 tương ứng với thời gian lưu của dung dịch mẫu chuẩn. Kết quả đã chỉ ra thành phần tá dược không ảnh hưởng đến quy trình định lượng. Do đó, quy trình phân tích đạt yêu cầu về chỉ tiêu tính đặc hiệu. 3.3. Khảo sát độ tuyến tính Kết quả khảo sát độ tuyến tính được trình bày ở Bảng 3 như sau: Bảng 3. Giá trị diện tích đỉnh theo nồng độ của cefixim Nồng độ (mg/mL) Diện tích đỉnh (mAu.s) Trung bình 0,04 3085966 3086010 3086015 3085997,0 0,10 4642494 4642362 4642343 4642399,7 0,20 7296185 7296220 7296196 7296200,3 0,30 9853304 9853318 9853296 9853306,0 0,40 12505608 12505564 12505530 12505567,3 Xây dựng đường chuẩn y = ax + b (Hình 4). Trong đó, (x) biểu thị nồng độ cefixim, (y) là diện tích đỉnh trung bình mỗi mẫu dung dịch chuẩn. Hình 4. Sự phụ thuộc giữa diện tích đỉnh trung bình mỗi mẫu dung dịch chuẩn và nồng độ của cefixim Từ các kết quả thu được, sử dụng phần mềm Excel, tính toán phương trình hồi quy biểu diễn nồng độ của cefixim theo diện tích đỉnh trung bình mỗi mẫu dung dịch chuẩn. Kết quả cho thấy đường biễu diễn là tuyến tính trong khoảng khảo sát với R2 = 1,00 (0,99 ≤ R2 ≤ 1,00), giới hạn phát hiện: LOD = 0,003 mg/mL, giới hạn định lượng: LOQ = 0,01 mg/mL. Vì thế, quy trình định lượng đạt yêu cầu về chỉ tiêu độ tuyến tính. 3.4. Khảo sát độ đúng Kết quả khảo sát độ đúng được trình bày ở Bảng 4 cho thấy % tỷ lệ độ phục hồi của 3 mẫu tại mỗi nồng độ trong khoảng từ 98-102%, % tỷ lệ độ phục hồi của 9 mẫu trong khoảng từ 99,72-101,25% (yêu cầu tỷ lệ phục hồi trong khoảng từ 98,0-102,0%), %RSD độ đúng của 9 mẫu tại 3 nồng độ là 0,59 (%RSD 2,0%). Như vậy, quy trình phân tích đạt yêu cầu về chỉ tiêu độ đúng. y = 26.141.847,09x + 2.039.189,80 R² = 1,00 0 2000000 4000000 6000000 8000000 10000000 12000000 14000000 0.00 0.10 0.20 0.30 0.40 0.50 D iệ n t íc h đ ỉn h ( m A u ) Nồng độ (mg/mL) Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg 121 Bảng 4. Kết quả khảo sát độ đúng của phương pháp Độ đúng mchuẩn thêm vào (mg) Cthêm vào (mg/mL) Diện tích đỉnh (mAu.s) Ctìm thấy (mg/mL) Tỷ lệ phục hồi (%) 80% 92,8 0,16 5970371,33 0,162 101,02 92,7 0,16 5977582,00 0,162 101,25 92,9 0,16 5962252,67 0,161 100,77 100% 116,0 0,20 7417481,00 0,201 100,40 116,2 0,20 7472885,00 0,202 100,98 116,4 0,20 7438525,33 0,201 100,34 120% 139,3 0,24 8847090,67 0,239 99,73 139,4 0,24 8860920,67 0,240 99,81 139,7 0,24 8872329,00 0,240 99,72 Tỷ lệ phục hồi trung bình (%) 100,45 %RSD 0,59 3.5. Khảo sát độ chính xác 3.5.1. Khảo sát độ lặp lại Kết quả % hàm lượng cefixim trong mẫu thử so với hàm lượng nhãn được thể hiện ở Bảng 5: Bảng 5. Kết quả % hàm lượng cefixim có trong mẫu thử so với hàm lượng nhãn STT Lượng cân thử (mg) Diện tích đỉnh (mAu) Hàm lượng (mg) %Hàm lượng so với nhãn 1 301,1 7315928,3 98,99 98,99 2 301,5 7318982,7 99,03 98,90 3 301,2 7315498,0 98,98 98,95 4 301,0 7311434,0 98,94 98,98 5 301,0 7315158,0 98,98 99,01 6 301,4 7312436,7 98,94 98,85 % Hàm lượng trung bình 98,95 %RSD 0,062 Kết quả cho thấy % hàm lượng trung bình của hoạt chất cefixim và độ lệch chuẩn tương đối trong mẫu là 98,95 0,062% (yêu cầu khoảng tin cậy về hàm lượng từ 90-110%). Vì vậy, phương pháp phân tích có độ lặp lại tốt, phù hợp áp dụng để định lượng cefixim trong nền mẫu viên nang cứng. 3.5.2. Khảo sát độ chính xác trung gian Kết quả khảo sát độ chính xác trung gian ở Bảng 6 cho thấy % hàm lượng cefixim so với nhãn thực hiện bởi 2 kiểm nghiệm viên là 98,90% và %RSD là 0,063 ( 2,0%). Có thể đánh giá quy trình phân tích để định lượng cefixim trong thuốc viên nang cứng đạt yêu cầu về chỉ tiêu độ chính xác. Mai Thanh Nhàn, Nguyễn Văn Hòa 122 Bảng 6. Kết quả % hàm lượng cefixim so với nhãn thực hiện bởi hai kiểm nghiệm viên STT Kiểm nghiệm viên 1 (KNV1) Kiểm nghiệm viên 2 (KNV2) Lượng cân thử (mg) Diện tích đỉnh (mAu) % Hàm lượng so với nhãn Lượng cân thử (mg) Diện tích đỉnh (mAu) % Hàm lượng so với nhãn 1 301,1 7315928,3 98,99 301,2 7313490,0 98,92 2 301,5 7318982,7 98,90 301,6 7316114,7 98,83 3 301,2 7315498,0 98,95 301,4 7315733,7 98,90 4 301,0 7311434,0 98,98 301,6 7314115,3 98,80 5 301,0 7315158,0 99,01 301,5 7314574,0 98,85 6 301,4 7312436,7 98,85 301,4 7312452,3 98,85 Hàm lượng trung bình (%) của KNV1 98,95 Hàm lượng trung bình (%) của KNV2 98,85 %RSD (n = 6) của KNV1 0,062 %RSD (n = 6) của KNV2 0,045 Hàm lượng trung bình của 2 kiểm nghiệm viên (n = 12): 98,90% %RSD (n = 12): 0,063 4. KẾT LUẬN VÀ ĐỀ NGHỊ Nghiên cứu đã ứng dụng phương pháp HPLC với các ưu điểm như độ nhạy tốt, có tính chọn lọc và độ tin cậy cao để xác định hoạt chất cefixim trong chế phẩm viên nang cứng có hàm lượng 100 mg. Điều kiện sắc ký được thiết lập trên cột HiQ Sil C18HS 4,6 mm (I.D) x 100 mm (L), thành phần pha động gồm acetonitril : tetrabutylamonium hydroxyd theo tỷ lệ 1:3, tốc độ dòng là 1,1 mL/phút, thể tích tiêm mẫu là 20 µL, đầu dò PDA phát hiện tại bước sóng 254 nm. Mẫu hòa tan trong dung dịch đệm phosphat có pH 7,0 nhằm duy trì dạng ion hóa của chất phân tích. Kết quả thực nghiệm đạt được như sau: phương pháp đáp ứng chỉ tiêu độ tuyến tính khi đạt giá trị R2 = 1,00 trong khoảng nồng độ khảo sát từ 0,04-0,4 mg/mL, chỉ tiêu độ lặp lại và độ chính xác trung gian lần lượt có %RSD lần lượt là 0,062% và 0,063% (≤ 2,0%). % tỷ lệ phục hồi của độ đúng trong khoảng 99,72-101,25% đạt yêu cầu % tỷ lệ phục hồi (98,0-102,0%). Tóm lại, có thể kết luận các kết quả thu được đều phù hợp theo tiêu chuẩn dược điển USP 34. Từ đó cho thấy, quy trình phân tích hoàn toàn phù hợp để ứng dụng định lượng dược chất cefixim trong chế phẩm viên nang cứng cefixim 100 mg. TÀI LIỆU THAM KHẢO 1. Kiran S. - Cephalosporins: pharmacology and chemistry, Pharmaceutical and Biological Evaluations 4 (6) (2017) 234-238. 2. Lê Minh Trí, Huỳnh Thị Ngọc Phương - Hóa dược 1, NXB Giáo dục Việt Nam (2011) 162-209. 3. Mai Tất Tố, Vũ Thị Trâm - Dược lý học Tập 2, NXB Y học (2007) 130-142. 4. Kandikonda S., Ganesh A., Pandey V.P, Kudaravalli S., Saikumar B., Srinivas R.B. - Validation of reversed: Phase HPLC method for the estimation of cefixime in cefixime oral suspension, International Journal of Pharmacy & Technology 2 (2) (2010) 385-395. 5. Nagaraju K., Chowdary Y.A. - Analytical method development and validation for the simultaneous estimation of azithromycin and cefixime by RP HPLC method in bulk Xây dựng và thẩm định quy trình phân tích định lượng viên nang cứng cefixim 100 mg 123 and pharmaceutical formulations, International Journal of Scientific Research in Science & Technology 4 (5) (2018) 669-674. 6. United States Pharmacopeial Convention - USP 34 NF 29: United States Pharmacopeia and National Formulary 29 (3) (2012) 616. 7. Đặng Văn Hòa, Vĩnh Định - Kiểm nghiệm thuốc, NXB Giáo dục Việt Nam (2011) 135-163. ABSTRACT ANALYTICAL METHOD DEVELOPMENT AND VALIATION FOR CEFIXIME FROM HARD CAPSULES 100 MG BY HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) Mai Thanh Nhan1*, Nguyen Van Hoa2 1Nguyen Tat Thanh University 2Ho Chi Minh City University of Food Industry *Email: mtnhan@ntt.edu.vn This research project aims to construct and determine the Cefĩxime from hard capsules 100 mg by high performance liquid chromatography (HPLC) according to USP 34. The chromatography was performed on a HiQ Sil C18HS 4,6 mm I.D x 100 mm L column, PDA detector at 254 nm. The isocratic elution with flow rate of 1.1 mL/min, mobile phase composition of acetonitrile: tetrabutylammonium hydroxide (1:3). The sample was dissolved in phosphate buffer pH 7.0. The linearity of cefixime were found in the range of 0,04-0,4 mg/mL. The limit of detection and the limit of quantitation were 0,003 mg/mL and 0,01 mg/mL, respectively. The accuracy of the proposed method was determined by recovery studies and ranged from 99.72 to 101.25%. The precision with repeatability %RSD = 0.062% and intermediate precision %RSD = 0.063% was achieved by two technicians. All the validation parameters were within the range. The method was validated for specificity, linearity, accuracy, precision, limit of detection and limit of quantitation. This proposed method is applicable for the determination of the cefixime in pharmaceutical formulations. Keywords: Cefixime, HPLC, ion chromatography pair, validation of quantitation analytical.
File đính kèm:
 xay_dung_va_tham_dinh_quy_trinh_phan_tich_dinh_luong_vien_na.pdf
xay_dung_va_tham_dinh_quy_trinh_phan_tich_dinh_luong_vien_na.pdf

