Hiệu quả và tính an toàn phác đồ hóa xạ trị tuần tự trên bệnh nhân ung thư hạ họng thanh quản giai đoạn không mổ
Mục tiêu: So sánh kết quả điều trị phác đồ TC và TCF ở bệnh nhân ung thư hạ họng thanh quản. Phương pháp Nghiên cứu thuần tập 74 bệnh nhân ung thư hạ họng thanh quản giai đoạn III, IV (Mo); trong đó 36 trường hợp được điều trị bằng phác đồ TCF và 38 bệnh nhân được điều trị bằng phác đồ TC. Kết quả: Không có sự khác biệt về đáp ứng sau hóa chất trước và sau hóa xạ trị giữa TC và TCF (p>0,05). Bệnh nhân điều trị phác đồ TCF có nhiều độc tính hơn về bạch cầu, bạch cầu hạt, buồn nôn, nôn, viêm miệng, tiêu chảy và rụng tóc (p<0,05). Sau 36 tháng theo dõi, không có sự khác biệt nguy cơ tử vong giữa TCF và TC (logrank p>0,05). Kết luận: Bệnh nhân điều trị TC có tính an toàn hơn TCF

Trang 1
Trang 2
Trang 3
Trang 4

Trang 5

Trang 6
Bạn đang xem tài liệu "Hiệu quả và tính an toàn phác đồ hóa xạ trị tuần tự trên bệnh nhân ung thư hạ họng thanh quản giai đoạn không mổ", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Hiệu quả và tính an toàn phác đồ hóa xạ trị tuần tự trên bệnh nhân ung thư hạ họng thanh quản giai đoạn không mổ

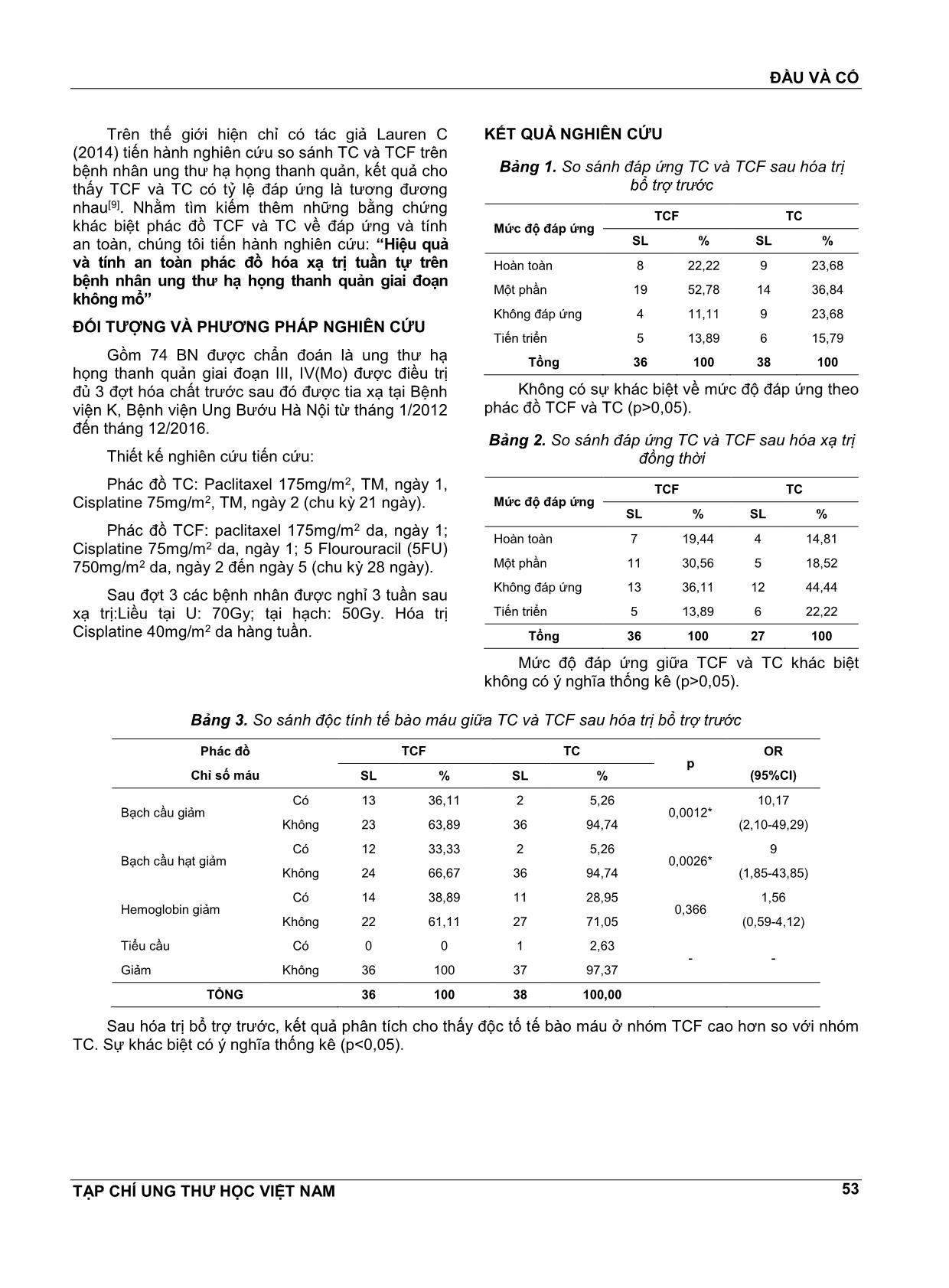
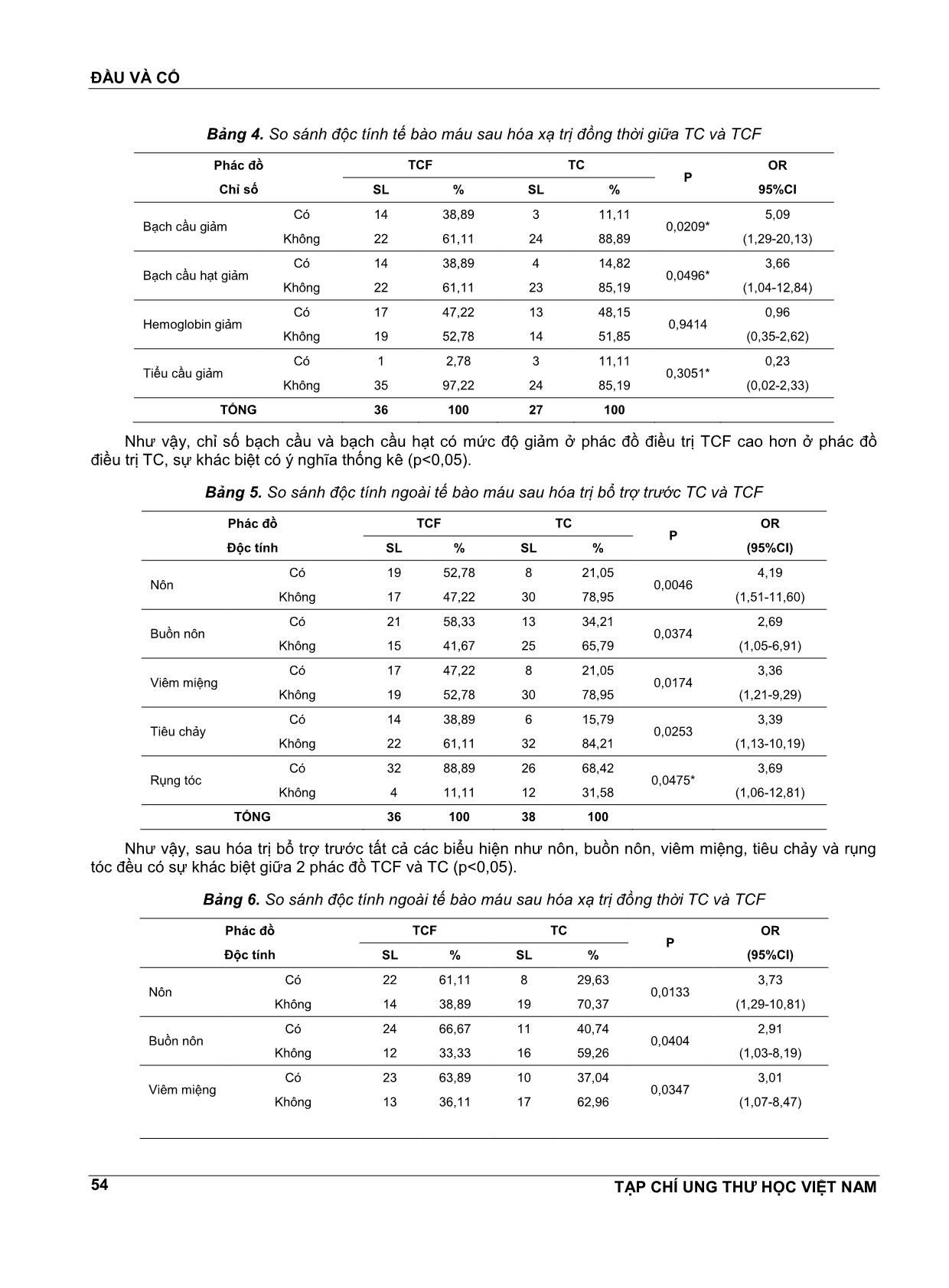
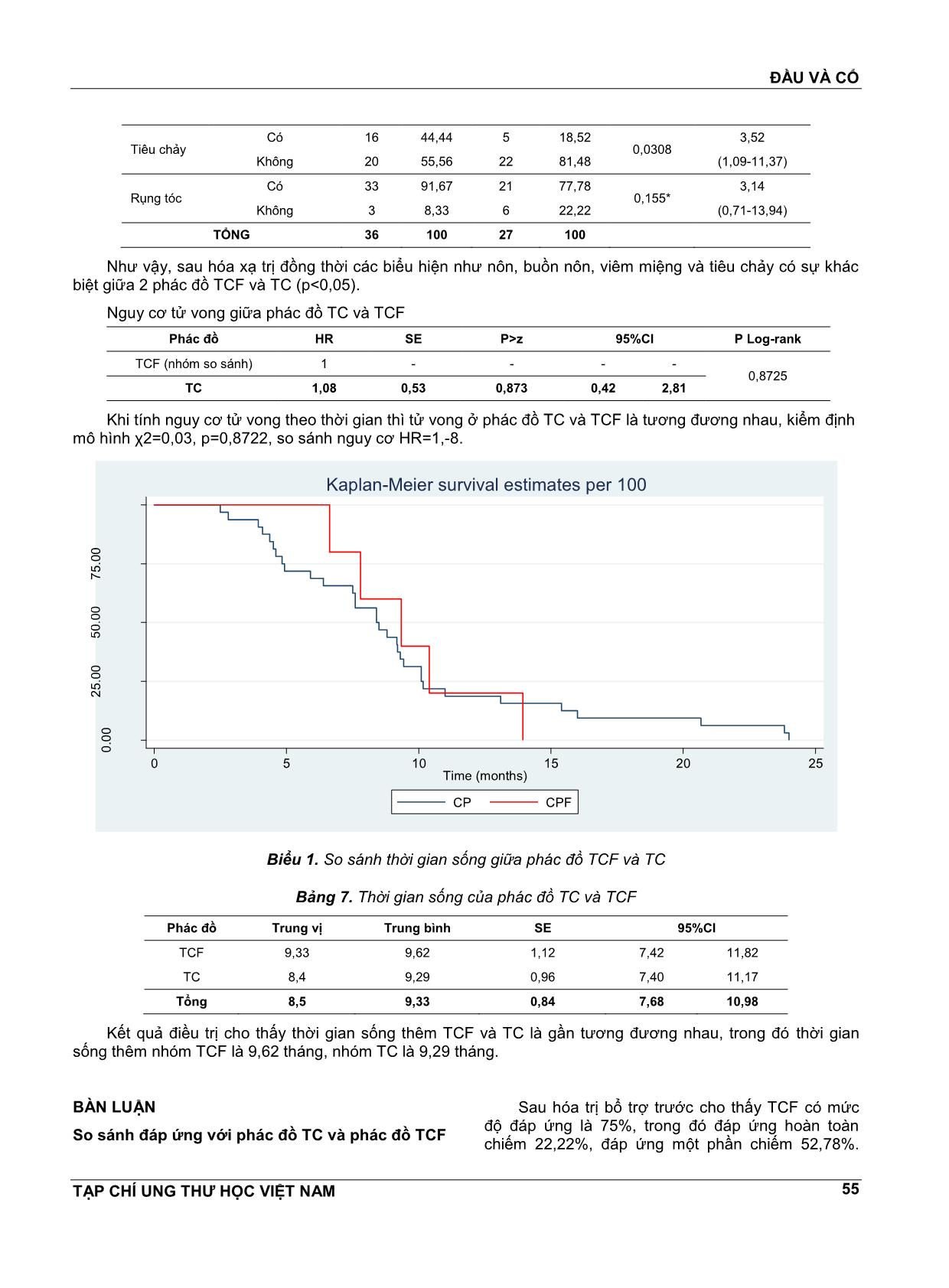
ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 52 HIỆU QUẢ VÀ TÍNH AN TOÀN PHÁC ĐỒ HÓA XẠ TRỊ TUẦN TỰ TRÊN BỆNH NHÂN UNG THƯ HẠ HỌNG THANH QUẢN GIAI ĐOẠN KHÔNG MỔ ĐÀM TRỌNG NGHĨA1,TRẦN ĐĔNG KHOA2, LÊ CHÍNH ĐẠI3, NGUYỄN ĐÌNH PHÚC4 TÓM TẮT NGHIÊN CỨU Mục tiêu: So sánh kết quả điều trị phác đồ TC và TCF ở bệnh nhân ung thư hạ họng thanh quản. Phương pháp Nghiên cứu thuần tập 74 bệnh nhân ung thư hạ họng thanh quản giai đoạn III, IV (Mo); trong đó 36 trường hợp được điều trị bằng phác đồ TCF và 38 bệnh nhân được điều trị bằng phác đồ TC. Kết quả: Không có sự khác biệt về đáp ứng sau hóa chất trước và sau hóa xạ trị giữa TC và TCF (p>0,05). Bệnh nhân điều trị phác đồ TCF có nhiều độc tính hơn về bạch cầu, bạch cầu hạt, buồn nôn, nôn, viêm miệng, tiêu chảy và rụng tóc (p<0,05). Sau 36 tháng theo dõi, không có sự khác biệt nguy cơ tử vong giữa TCF và TC (logrank p>0,05). Kết luận: Bệnh nhân điều trị TC có tính an toàn hơn TCF. SUMMMARY Efficacy and safety of induction regimen followed by chemoradiotherapy for patients with advanced laryngeal and hypopharyngeal cancer Objective: In order to compare outcomes of patients with advanced laryngeal, hypopharyngeal cancer, treated with either TC or TCF as induction chemotherapy followed by CRT. Methods: We conducted a longitudinal study, the data was collected from 74 patients with advanced laryngeal, hypopharyngeal cancer, stage III to IV(Mo), in which 36 patients received TC induction and 38 patients received TCF induction. Results: There are no differences in the overall response rate after induction, CRT betweenTC and TCF (p>0,05). Patients with TCF are higher rate in toxicities of white blood cell, granulocyte, nausea, vomiting, stomatitis, diarrhea and hair loss (p<0,05). In survival analysis after 36 months, the hazard ratio was no significance beeween TCF and TC (logrank p>0,05). Conclusions: Patient receivedTC was safer than patients received TCF. 1 ThS.BS - Bệnh viện Ung Bướu Hà Nội 2 PGS.TS - Bệnh viện Ung Bướu Hà Nội 3 PGS.TS - Đại học Y Hà Nội 4 GS.TS - Đại học Y Hà Nội ĐẶT VẤN ĐỀ Ung thư hạ họng thanh quản có tỷ lệ bệnh mắc cao, ước tính nĕm 2012 có khoảng 115130 bệnh nhân mới mắc trên toàn cầu[1]. Ở Việt Nam, theo Nguyễn Tuấn Hưng, tỷ lệ mắc ung thư hạ họng thanh quản ở Nam: 2,8/100 000/nĕm, Nữ: 0,3/100 000/nĕm[2]. Nghiên cứu điều trị ung thư hạ họng thanh quản trong 30 nĕm trở lại đây, cho thấy hóa trị kết hợp xạ trị là những phác đồ cơ bản[3]. Từ nghiên cứu TAX 323 và TAX 324 chỉ ra rằng phác đồ có docetaxel, cisplatine, và 5-fluorouracil (TCF) cải thiện sống thêm tốt hơn so với phác đồ cisplatine và 5- fluorouracil[4,5]. Phác đồ TCF là phác đồ hóa trị bổ trợ trước được chấp nhận nhiều nhất[6]. Mặc dù vậy, phác đồ này với tỷ lệ độc tính cao và bệnh nhân khó theo đủ liệu trình điều trị[4,7]. Nghiên cứu của Pointreau (2009) cho thấy phác đồ TCF đáp ứng tốt hơn, tuy nhiên có độc tính nhiều hơn so với PF[8]. ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 53 Trên thế giới hiện chỉ có tác giả Lauren C (2014) tiến hành nghiên cứu so sánh TC và TCF trên bệnh nhân ung thư hạ họng thanh quản, kết quả cho thấy TCF và TC có tỷ lệ đáp ứng là tương đương nhau[9]. Nhằm tìm kiếm thêm những bằng chứng khác biệt phác đồ TCF và TC về đáp ứng và tính an toàn, chúng tôi tiến hành nghiên cứu: “Hiệu quả và tính an toàn phác đồ hóa xạ trị tuần tự trên bệnh nhân ung thư hạ họng thanh quản giai đoạn không mổ” ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU Gồm 74 BN được chẩn đoán là ung thư hạ họng thanh quản giai đoạn III, IV(Mo) được điều trị đủ 3 đợt hóa chất trước sau đó được tia xạ tại Bệnh viện K, Bệnh viện Ung Bướu Hà Nội từ tháng 1/2012 đến tháng 12/2016. Thiết kế nghiên cứu tiến cứu: Phác đồ TC: Paclitaxel 175mg/m2, TM, ngày 1, Cisplatine 75mg/m2, TM, ngày 2 (chu kỳ 21 ngày). Phác đồ TCF: paclitaxel 175mg/m2 da, ngày 1; Cisplatine 75mg/m2 da, ngày 1; 5 Flourouracil (5FU) 750mg/m2 da, ngày 2 đến ngày 5 (chu kỳ 28 ngày). Sau đợt 3 các bệnh nhân được nghỉ 3 tuần sau xạ trị:Liều tại U: 70Gy; tại hạch: 50Gy. Hóa trị Cisplatine 40mg/m2 da hàng tuần. KẾT QUẢ NGHIÊN CỨU Bảng 1. So sánh đáp ứng TC và TCF sau hóa trị bổ trợ trước Mức độ đáp ứng TCF TC SL % SL % Hoàn toàn 8 22,22 9 23,68 Một phần 19 52,78 14 36,84 Không đáp ứng 4 11,11 9 23,68 Tiến triển 5 13,89 6 15,79 Tổng 36 100 38 100 Không có sự khác biệt về mức độ đáp ứng theo phác đồ TCF và TC (p>0,05). Bảng 2. So sánh đáp ứng TC và TCF sau hóa xạ trị đồng thời Mức độ đáp ứng TCF TC SL % SL % Hoàn toàn 7 19,44 4 14,81 Một phần 11 30,56 5 18,52 Không đáp ứng 13 36,11 12 44,44 Tiến triển 5 13,89 6 22,22 Tổng 36 100 27 100 Mức độ đáp ứng giữa TCF và TC khác biệt không có ý nghĩa thống kê (p>0,05). Bảng 3. So sánh độc tính tế bào máu giữa TC và TCF sau hóa trị bổ trợ trước Phác đồ Chỉ số máu TCF TC p OR (95%CI) SL % SL % Bạch cầu giảm Có 13 36,11 2 5,26 0,0012* 10,17 (2,10-49,29) Không 23 63,89 36 94,74 Bạch cầu hạt giảm Có 12 33,33 2 5,26 0,0026* 9 (1,85-43,85) Không 24 66,67 36 94,74 Hemoglobin giảm Có 14 38,89 11 28,95 0,366 1,56 (0,59-4,12) Không 22 61,11 27 71,05 Tiểu cầu Giảm Có 0 0 1 2,63 - - Không 36 100 37 97,37 TỔNG 36 100 38 100,00 Sau hóa trị bổ trợ trước, kết quả phân tích cho thấy độc tố tế bào máu ở nhóm TCF cao hơn so với nhóm TC. Sự khác biệt có ý nghĩa thống kê (p<0,05). ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 54 Bảng 4. So sánh độc tính tế bào máu sau hóa xạ trị đồng thời giữa TC và TCF Phác đồ Chỉ số TCF TC P OR 95%CI SL % SL % Bạch cầu giảm Có 14 38,89 3 11,11 0,0209* 5,09 (1,29-20,13) Không 22 61,11 24 88,89 Bạch cầu hạt giảm Có 14 38,89 4 14,82 0,0496* 3,66 (1,04-12,84) Không 22 61,11 23 85,19 Hemoglobin giảm Có 17 47,22 13 48,15 0,9414 0,96 (0,35-2,62) Không 19 52,78 14 51,85 Tiểu cầu giảm Có 1 2,78 3 11,11 0,3051* 0,23 (0,02-2,33) Không 35 97,22 24 85,19 TỔNG 36 100 27 100 Như vậy, chỉ số bạch cầu và bạch cầu hạt có mức độ giảm ở phác đồ điều trị TCF cao hơn ở phác đồ điều trị TC, sự khác biệt có ý nghĩa thống kê (p<0,05). Bảng 5. So sánh độc tính ngoài tế bào máu sau hóa trị bổ trợ trước TC và TCF Phác đồ Độc tính TCF TC P OR (95%CI) SL % SL % Nôn Có 19 52,78 8 21,05 0,0046 4,19 (1,51-11,60) Không 17 47,22 30 78,95 Buồn nôn Có 21 58,33 13 34,21 0,0374 2,69 (1,05-6,91) Không 15 41,67 25 65,79 Viêm miệng Có 17 47,22 8 21,05 0,0174 3,36 (1,21-9,29) Không 19 52,78 30 78,95 Tiêu chảy Có 14 38,89 6 15,79 0,0253 3,39 (1,13-10,19) Không 22 61,11 32 84,21 Rụng tóc Có 32 88,89 26 68,42 0,0475* 3,69 (1,06-12,81) Không 4 11,11 12 31,58 TỔNG 36 100 38 100 Như vậy, sau hóa trị bổ trợ trước tất cả các biểu hiện như nôn, buồn nôn, viêm miệng, tiêu chảy và rụng tóc đều có sự khác biệt giữa 2 phác đồ TCF và TC (p<0,05). Bảng 6. So sánh độc tính ngoài tế bào máu sau hóa xạ trị đồng thời TC và TCF Phác đồ Độc tính TCF TC P OR (95%CI) SL % SL % Nôn Có 22 61,11 8 29,63 0,0133 3,73 (1,29-10,81) Không 14 38,89 19 70,37 Buồn nôn Có 24 66,67 11 40,74 0,0404 2,91 (1,03-8,19) Không 12 33,33 16 59,26 Viêm miệng Có 23 63,89 10 37,04 0,0347 3,01 (1,07-8,47) Không 13 36,11 17 62,96 ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 55 Tiêu chảy Có 16 44,44 5 18,52 0,0308 3,52 (1,09-11,37) Không 20 55,56 22 81,48 Rụng tóc Có 33 91,67 21 77,78 0,155* 3,14 (0,71-13,94) Không 3 8,33 6 22,22 TỔNG 36 100 27 100 Như vậy, sau hóa xạ trị đồng thời các biểu hiện như nôn, buồn nôn, viêm miệng và tiêu chảy có sự khác biệt giữa 2 phác đồ TCF và TC (p<0,05). Nguy cơ tử vong giữa phác đồ TC và TCF Phác đồ HR SE P>z 95%CI P Log-rank TCF (nhóm so sánh) 1 - - - - 0,8725 TC 1,08 0,53 0,873 0,42 2,81 Khi tính nguy cơ tử vong theo thời gian thì tử vong ở phác đồ TC và TCF là tương đương nhau, kiểm định mô hình χ2=0,03, p=0,8722, so sánh nguy cơ HR=1,-8. 0 .0 0 2 5. 00 5 0. 00 7 5. 00 1 00 .0 0 0 5 10 15 20 25 Time (months) CP CPF Kaplan-Meier survival estimates per 100 Biểu 1. So sánh thời gian sống giữa phác đồ TCF và TC Bảng 7. Thời gian sống của phác đồ TC và TCF Phác đồ Trung vị Trung bình SE 95%CI TCF 9,33 9,62 1,12 7,42 11,82 TC 8,4 9,29 0,96 7,40 11,17 Tổng 8,5 9,33 0,84 7,68 10,98 Kết quả điều trị cho thấy thời gian sống thêm TCF và TC là gần tương đương nhau, trong đó thời gian sống thêm nhóm TCF là 9,62 tháng, nhóm TC là 9,29 tháng. BÀN LUẬN So sánh đáp ứng với phác đồ TC và phác đồ TCF Sau hóa trị bổ trợ trước cho thấy TCF có mức độ đáp ứng là 75%, trong đó đáp ứng hoàn toàn chiếm 22,22%, đáp ứng một phần chiếm 52,78%. ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 56 Mức độ đáp đáp ứng của phác đồ TC thấp hơn với tỷ lệ là 60,52%, trong đó đáp ứng hoàn toàn là 23,68%, đáp ứng một phần là 36,84%. Sự khác biệt có ý nghĩa thống kê với p<0,001. Điều đó cho thấy là TCF có mức độ đáp ứng tốt hơn so với TC sau giai đoạn hóa trị bổ trợ trước. Sau giai đoạn hóa xạ trị đồng thời, ở phác đồ TCF mức độ đáp ứng là 50%, trong đó đáp ứng hoàn toàn là 19,44%, đáp ứng một phần là 30,56%. Mức độ đáp ứng của phác đồ TC là 33,33%, trong đó đáp ứng hoàn toàn là 14,81%, đáp ứng một phần là 18,52%. Có sự khác biệt giữa mức độ đáp ứng giữa TCF và TC ở giai đoạn sau hóa xạ trị đồng thời với p=0,002. Tương tự với nghiên cứu của chúng tôi tác giả Lauren C và các cs (2014) mức độ đáp ứng giữa TCF và TC không có ý nghĩa thống kê với p=0,83[9]. So sánh độc tính giữa phác đồ TC và TCF Nghiên cứu của chúng tôi cho thấy độc tố tế bào có sự khác biệt giữa TCF và TC ở các chỉ số bạch cầu, bạch cầu hạt ở cả 2 trường hợp sau hóa trị bổ trợ trước và sau hóa xạ trị đồng thời. Như vậy ở chỉ số máu có sự khác biệt ở việc giảm bạch cầu giữa hai phác đồ điều trị TC và TCF. Điều này có thể dẫn tới là sự khác biệt giữa 2 nhóm bệnh nhân về nguy cơ mắc các bệnh nhiễm trùng cơ hội là khác nhau. Nghiên cứu của chúng tôi có sự khác biệt khi so sánh với nghiên cứu của Lauren C và cs (2014), tác giả so sánh giữa 2 phác đồ hóa xạ trị đồng thời carboplatin-paclitaxel và docetaxel-cisplatine-5- flurouracil ở những bệnh nhân ung thư đầu cổ tác giả cho thấy tỷ giảm bạch cầu trung tính dẫn đến hoãn điều trị 7,5% ở nhóm docetaxel-cisplatine-5- flurouracil so với 23,3% ở nhóm carboplatin- paclitaxel[9]. Kết quả nghiên cứu của chúng tôi cũng cho thấy độc tính ngoài máu sau hóa trị bổ trợ trướcTC và TCF có sự khác biệt ở tất cả các chỉ số ở cả hai trường hợp sau hóa trị bổ trợ trước và sau hóa xạ trị đồng thời (p<0,05) ngoại trừ rụng tóc sau hóa xạ trị đồng thời. Trong đó nhóm TCF đều có các chỉ số cao hơn so với nhóm TC. Phác đồ TC được sử dụng trong nghiên cứu của chúng tôi đã chứng minh được tính an toàn và có thể chấp nhận được với độc tố thấp trong giai đoạn điều trị. Thực tế phác đồ TCF có sự đáp ứng cao hơn TC, tuy nhiên độc tính TCF lại cao hơn so với TC, kết quả nghiên cứu cũng cho thấy là nguy cơ tử vong và thời gian sống còn giữa hai phác đồ là gần tương đương nhau. Điều đó, cho thấy cần cân nhắc kỹ khi lựa chọn phác đồ điều trị cho mỗi bệnh nhân. So sánh nguy cơ tử vong giữa phác đồ TC và TCF Kết quả phân tích cho thấy không có sự khác biệt giữa nguy cơ tử vong giữa 2 phác đồ TCF và TC với kiểm định Log-rank p=0,8725. Đo lường nguy cơ cho thấy nguy cơ tử vong của TC so với TCF là tương đương nhau với HR=1,08 (95%CI 0,42-2,81). Phân tích thời gian sống thêm giữa TCF và TC cho thấy kết quả là gần tương đương nhau, trong đó thời gian sống thêm nhóm TCF là 9,62 tháng, nhóm TC là 9,29 tháng. Trung vị giữa 2 nhóm TCF và TC lần lượt là 9,33 tháng và 8,4 tháng. Kết quả nghiên cứu của chúng tôi tương tự khi so sánh với nghiên cứu của Lauren C và cs (2014)[9]. KẾT LUẬN Nghiên cứu cho thấy mức độ đáp ứng nhóm TCF cao hơn nhóm TC, tuy vậy sự khác biệt không có ý nghĩa thống kê (p>0,05). Bệnh nhân điều trị phác đồ TCF có nhiều độc tính hơn. Sau 36 tháng theo dõi, không có sự khác biệt nguy cơ tử vong giữa TCF và TC. TÀI LIỆU THAM KHẢO 1. “GLOBOCAN 2012”. [Online]. Available at: 2. Nguyễn Tuấn Hưng, “Đặc điểm dịch tể học mô tả ung thư cộng đồng dân cư Hà Nội giai đoạn 2001-2005 2008-LUẬN ÁN TIẾN SĨ - Cơ sở dữ liệu toàn vĕn”, Luận án Tiến sỹ, Viện Vệ sinh Dịch tễ Trung ương., 2008. 3. R. Haddad và c.s., “Docetaxel, cisplatine, 5- fluorouracil (TCF)-based induction chemotherapy for head and neck cancer and the case for sequential, combined-modality treatment”, The Oncologist, vol 8, số p.h 1, tr 35-44, 2003. 4. J. B. Vermorken và c.s., “Cisplatine, fluorouracil, and docetaxel in unreseCTable head and neck cancer”, N. Engl. J. Med., vol 357, số p.h 17, tr 1695–1704, tháng 10 2007. 5. M. R. Posner và c.s., “Cisplatine and fluorouracil alone or with docetaxel in head and neck cancer”, N. Engl. J. Med., vol 357, số p.h 17, tr 1705-1715, tháng 10 2007. 6. S. Billan và c.s., “Toxicity of induCTion chemotherapy with docetaxel, cisplatine and 5- fluorouracil for advanced head and neck cancer”, Isr. Med. Assoc. J. IMAJ, vol 15, số p.h 5, tr 231- 235, tháng 5 2013. ĐẦU VÀ CỔ TẠP CHÍ UNG THƯ HỌC VIỆT NAM 57 7. R. Hitt và c.s., “A randomized phase III trial comparing induCTion chemotherapy followed by chemoradiotherapy versus chemoradiotherapy alone as treatment of unreseCTable head and neck cancer”, Ann. Oncol. Off. J. Eur. Soc. Med. Oncol., vol 25, số p.h 1, tr 216-225, tháng 1 2014. 8. Y. Pointreau và c.s., “Randomized trial of induCTion chemotherapy with cisplatine and 5- fluorouracil with or without docetaxel for larynx preservation”, J. Natl. Cancer Inst., vol 101, số p.h 7, tr 498-506, tháng 4 2009. 9. L. C. Herman và c.s., “Comparison of carboplatin-paclitaxel to docetaxel-cisplatine-5- flurouracil induCTion chemotherapy followed by concurrent chemoradiation for locally advanced head and neck cancer”, Oral Oncol., vol 50, số p.h 1, tr 52-58, tháng 1 2014.
File đính kèm:
 hieu_qua_va_tinh_an_toan_phac_do_hoa_xa_tri_tuan_tu_tren_ben.pdf
hieu_qua_va_tinh_an_toan_phac_do_hoa_xa_tri_tuan_tu_tren_ben.pdf

