Cắt lớp vi tính hai mức năng lượng trong đánh giá hẹp xơ vữa vôi hoá động mạch cảnh ngoài sọ
Sử dụng cắt lớp vi tính (CLVT) hai mức năng lượng (Dual energy Computed Tomographic: DECT) với kỹ thuật tạo ảnh xoá xơ vữa vôi hoá để đánh giá mức độ hẹp động mạch cảnh trong (Internal Carotide Artery: ICA) có so sánh với ảnh cắt lớp vi tính mạch máu thường qui (Computed Tomographic Angiography: CTA) trên 27 bệnh nhân với 43 động mạch cảnh trong bị hẹp. Mức độ hẹp được đánh giá theo NASCET trên cả hai kỹ thuật CTA thường qui và DECT có loại bỏ vôi hoá. Kết quả cho thấy có sự phù hợp với mức độ rất tốt giữa hai phương thức chẩn đoán này trong đánh giá mức độ hẹp ICA với hệ số Kappa = 0,812. Mức độ hẹp trung bình ICA đo trên hình ảnh CTA thông thường và DECT lần lượt là 63,3 ± 25,0% và 59,5 ± 24,4%, sự khác biệt có ý nghĩa thống kê (p < 0,001). Như vậy, DECT loại bỏ mảng xơ vữa vôi hoá đã tạo điều kiện thuận lợi cho việc đánh giá mức độ hẹp trong mọi trường hợp, như vậy nó phân loại hẹp ICA tốt hơn CTA thông thường

Trang 1

Trang 2
Trang 3

Trang 4
Trang 5

Trang 6

Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Cắt lớp vi tính hai mức năng lượng trong đánh giá hẹp xơ vữa vôi hoá động mạch cảnh ngoài sọ

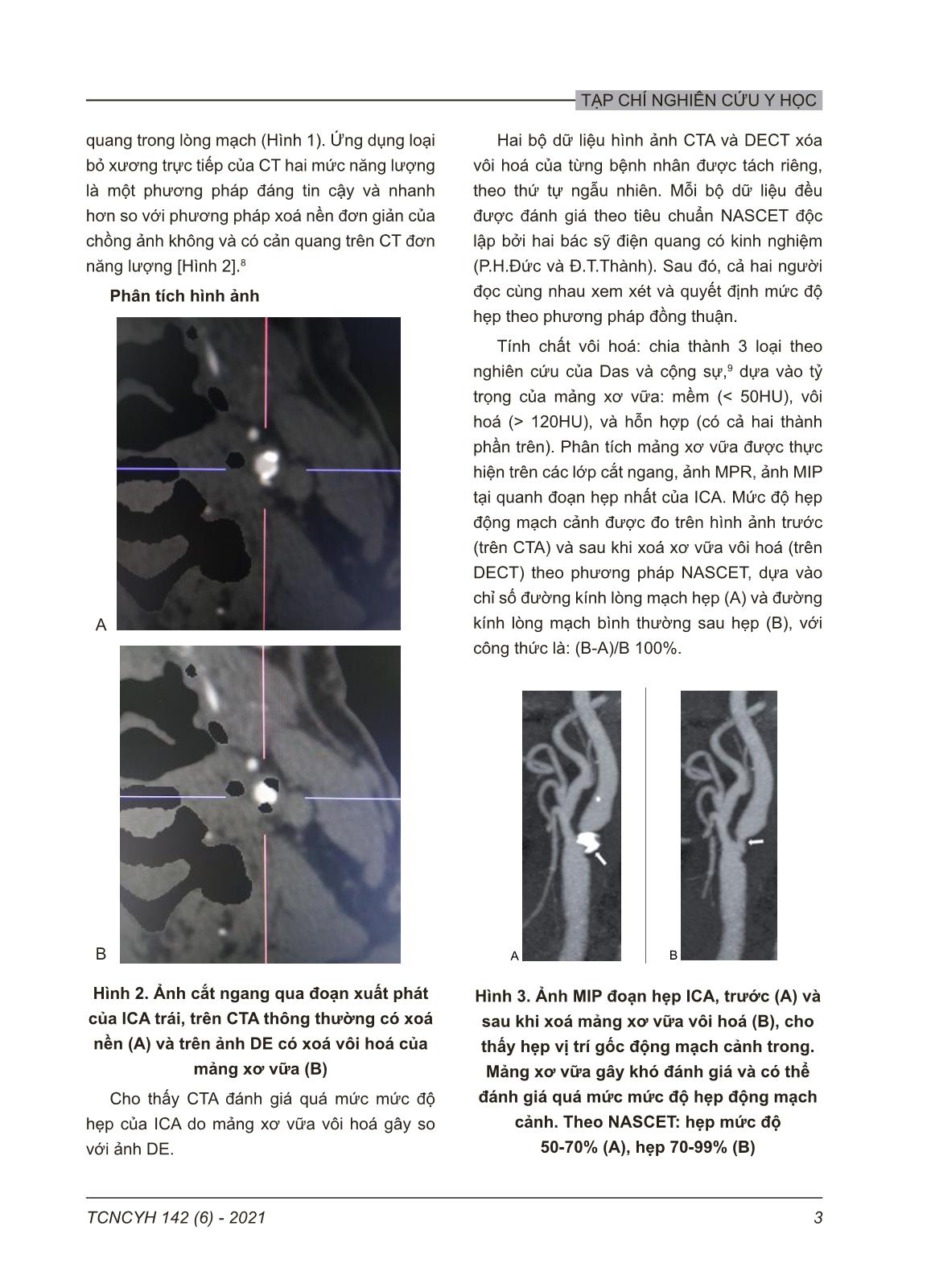
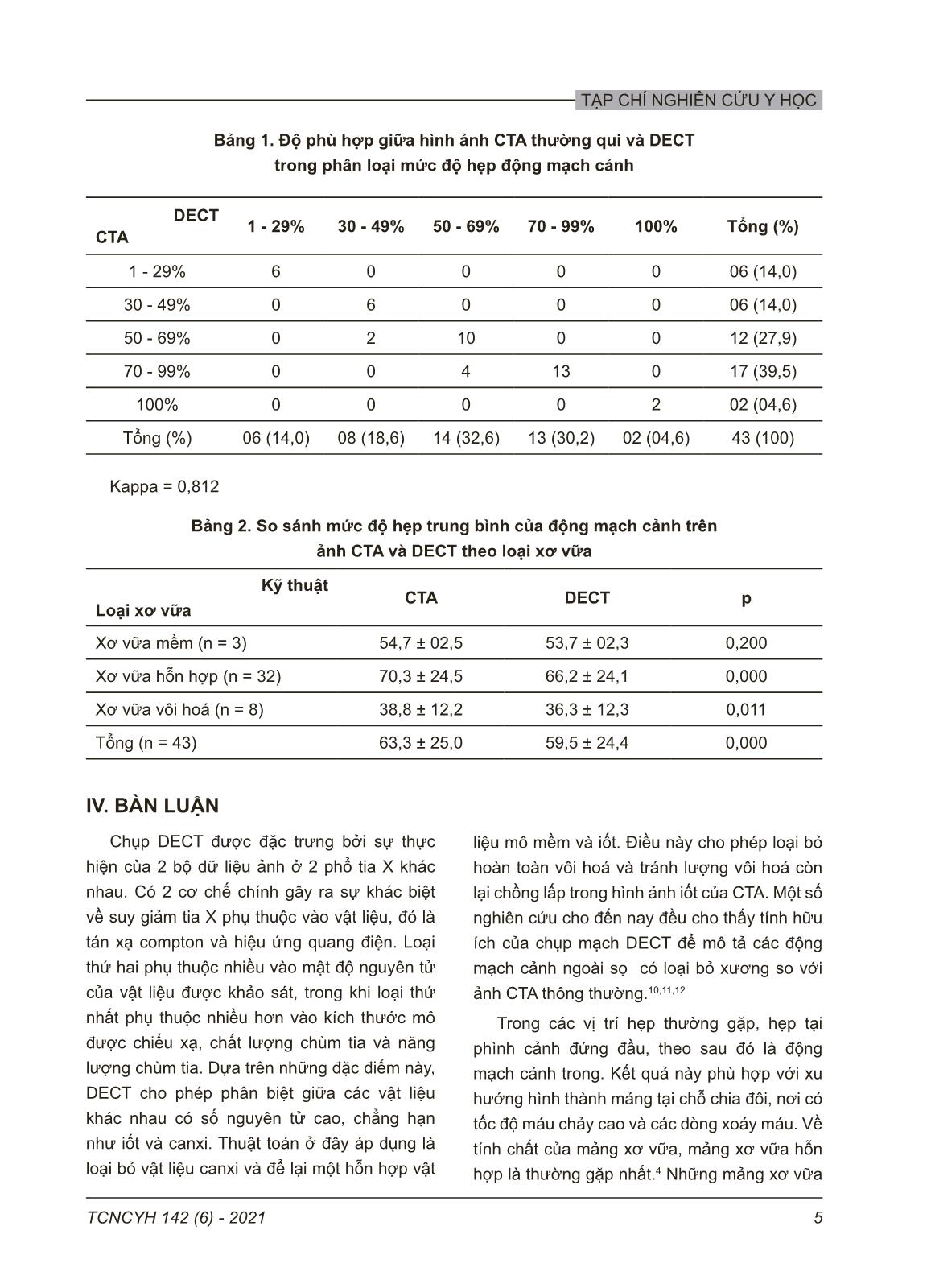
TẠP CHÍ NGHIÊN CỨU Y HỌC 1TCNCYH 142 (6) - 2021 CẮT LỚP VI TÍNH HAI MỨC NĂNG LƯỢNG TRONG ĐÁNH GIÁ HẸP XƠ VỮA VÔI HOÁ ĐỘNG MẠCH CẢNH NGOÀI SỌ Phạm Hồng Đức1,2, , Nguyễn Hữu Thuyết1, Đinh Trung Thành2 1Trường Đại học Y Hà Nội 2Bệnh viện đa khoa Xanh Pôn Hà Nội Từ khóa: hẹp động mạch cảnh, mảng xơ vữa, CLVT hai mức năng lượng. Sử dụng cắt lớp vi tính (CLVT) hai mức năng lượng (Dual energy Computed Tomographic: DECT) với kỹ thuật tạo ảnh xoá xơ vữa vôi hoá để đánh giá mức độ hẹp động mạch cảnh trong (Internal Carotide Artery: ICA) có so sánh với ảnh cắt lớp vi tính mạch máu thường qui (Computed Tomographic Angiography: CTA) trên 27 bệnh nhân với 43 động mạch cảnh trong bị hẹp. Mức độ hẹp được đánh giá theo NASCET trên cả hai kỹ thuật CTA thường qui và DECT có loại bỏ vôi hoá. Kết quả cho thấy có sự phù hợp với mức độ rất tốt giữa hai phương thức chẩn đoán này trong đánh giá mức độ hẹp ICA với hệ số Kappa = 0,812. Mức độ hẹp trung bình ICA đo trên hình ảnh CTA thông thường và DECT lần lượt là 63,3 ± 25,0% và 59,5 ± 24,4%, sự khác biệt có ý nghĩa thống kê (p < 0,001). Như vậy, DECT loại bỏ mảng xơ vữa vôi hoá đã tạo điều kiện thuận lợi cho việc đánh giá mức độ hẹp trong mọi trường hợp, như vậy nó phân loại hẹp ICA tốt hơn CTA thông thường. Tác giả liên hệ: Phạm Hồng Đức Trường Đại học Y Hà Nội Email: phamhongduc@hmu.edu.vn Ngày nhận: 05/03/2021 Ngày được chấp nhận: 24/05/2021 I. ĐẶT VẤN ĐỀ Trong các bệnh lý liên quan đến tim mạch, đột quỵ chiếm tỷ lệ đáng kể và thiếu máu não là thể bệnh lý thường gặp nhất trong nhóm đột quỵ. Bệnh xơ vữa động mạch cảnh trong ngoài sọ là một nguyên nhân thường gặp gây ra đột quỵ thiếu máu não, chiếm khoảng 7-18%.1 Các phương thức chẩn đoán hình ảnh được sử dụng để đánh giá hẹp động mạch cảnh ngoài sọ bao gồm: Siêu âm Doppler mạch máu, cắt lớp vi tính mạch máu (Computed Tomographic Angiography: CTA), cộng hưởng từ mạch máu (Magnetic Resonance Angiography: MRA), chụp mạch số hoá xoá nền (Digital Subtraction Angiography: DSA). Siêu âm Doppler là phương pháp rẻ tiền, dễ áp dụng và thường được sử dụng như một xét nghiệm sàng lọc để quyết định có thực hiện DSA hay không.2 Tuy nhiên, DSA mặc dù là tiêu chuẩn vàng, nhưng có hạn chế là phương thức xâm phạm nên không dùng thường qui tầm soát tổn thương hẹp mạch cảnh.3 Do vậy, CTA và MRA là những phương thức ngày càng được sử dụng rộng rãi, không những để đánh giá hẹp động mạch cảnh với độ chính xác cao mà còn cho những thông tin về mạch nội sọ và tình trạng quai động mạch chủ để lập kế hoạch can thiệp.2 CTA có lợi thế hơn MRA trong đánh giá đặc điểm vôi hoá của mảng xơ vữa.4 Tuy nhiên, giá trị chẩn đoán của CTA thông thường trong đánh giá mức độ hẹp có thể bị hạn chế khi xơ vữa vôi hoá do khó phân biệt lòng mạch có thuốc cản quang có cùng tỷ trọng.5 Chụp cắt lớp vi tính hai mức năng lượng (DECT) là một kỹ thuật mới có khả năng khắc phục hạn chế này. Hệ thống dùng hai nguồn phát tia X với kilovolt khác nhau. Nguyên tử khối của iốt và canxi khác nhau nên có sự suy giảm tia X khác nhau ở các mức năng lượng khác nhau, do đó kỹ thuật này có khả năng phân biệt giữa iốt cản quang TẠP CHÍ NGHIÊN CỨU Y HỌC 2 TCNCYH 142 (6) - 2021 và cấu trúc vôi hoá, và cho phép loại bỏ mảng xơ vữa vôi hoá giúp đánh giá mức độ hẹp lòng mạch chính xác hơn.4,6,7 Mục đích của nghiên cứu này là góp phần khẳng định vai trò của DECT so với CTA trong xác định mức độ hẹp động mạch cảnh do xơ vữa. II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP 1. Đối tượng Nghiên cứu gồm 27 bệnh nhân trên siêu âm Doppler có hẹp động mạch cảnh ngoài sọ một hoặc hai bên, có hoặc không có biểu hiện triệu chứng thần kinh liên quan đến mạch não, được chỉ định chụp DECT để đánh giá tình trạng vôi hoá và mức độ hẹp động mạch cảnh ngoài sọ tại Bệnh viện Xanh Pôn, trong thời gian từ 06/2018 đến 06/2020. 2. Phương pháp Cách thức chụp và tạo ảnh DECT Tất cả bệnh nhân đều được chụp cắt lớp vi tính 384 dãy hai nguồn năng lượng (SOMATOM Force, Siemens, Đức). Qui trình chụp gồm sử dụng hai bóng: bóng A (150 kV, 250 mA) và bóng B (80 kV, 410 mA) với độ dày 2 x 192 x 0,6 mm, bước nhảy pitch 0,75 và thời gian quay 0,25 giây. Để đánh giá thời gian bơm thuốc cản quang tối ưu trước khi chụp, thử test được thực hiện với bơm 10 ml cản quang (Xenetix 350mgIod/ml, Guerbet, Pháp) với tốc độ 5 ml/s, tiếp theo là 40 ml nước muối sinh lý, qua đường truyền tĩnh mạch bằng kim 18-gauge ở nếp khuỷu tay. Sau khi xác định thời gian đạt đỉnh thuốc cản quang ở quai động mạch chủ, tiến hành chụp hệ mạch cảnh với bơm 40 ml cản quang và tốc độ như thử test. Quá trình quét được thực hiện theo hướng từ quai động mạch chủ đến giữa hộp sọ. Hình ảnh được dựng lại với độ dày lát cắt 0,625 mm, trên cửa sổ rộng và trung tâm (WW: 600, WL:150). Hình ảnh hiển thị ICA được sử dụng là hình tái tạo nhiều mặt phẳng (Multi- Planar Reformation: MPR) với độ dày 1,5 mm, và tái tạo hình chiếu cường độ tối đa (Maximum Intensity Projection: MIP). Hình ảnh thu được đồng thời cho hai bộ ảnh tương ứng với hai nguồn năng lượng khác nhau (80KV và 150KV) bằng phầm mềm 3D (Syngo, Siemens Medical Solutions, Đức). Hình 1. MD (Material decomposition) là thuật toán tạo ra một số hình ảnh DE (Dual energy) Thuật toán này có thể phân biệt một vật liệu với các vật liệu khác như xương (Bone) và iốt (Iodine) bằng cách sử dụng một đường phân cách (Separation line). Thuật ngữ này đã được sử dụng cho ứng dụng loại bỏ xương trực tiếp DE.8 Đầu tiên, tạo ảnh CTA thường qui bằng kết hợp hai bộ ảnh quét năng lượng thấp với năng lượng cao (giống như CTA năng lượng đơn) với hệ số trọng là 0,5. Sau đó, dữ liệu thô của hai ảnh quét có năng lượng khác nhau này được chuyển đến trạm xử lý để tạo ảnh bằng kỹ thuật Head Bone Removal, giúp loại bỏ cấu trúc có canxi (xương, vôi hoá). Kỹ thuật này sử dụng thuật toán loại trừ vật liệu (Material decomposi ... c sỹ điện quang có kinh nghiệm (P.H.Đức và Đ.T.Thàn ). Sau đó, cả hai người đọc cùng nhau xem xét và quyết định mức độ hẹp theo phương pháp đồng thuận. Tính chất vôi hoá: chia thành 3 loại theo nghiên cứu của Das và cộng sự9, dựa vào tỷ trọng của mảng xơ vữa: mềm (120HU), và hỗn hợp (có cả hai thành phần trên). Phân tíc mảng xơ vữa được thực hiện trên các lớp cắt ngang, ảnh MPR, ảnh MIP tại quanh đoạn hẹp nhất của ICA. Mức độ hẹp động mạch cảnh được đo trên hình ảnh trước (trên CTA) và sau khi xoá xơ vữa vôi hoá (trên DECT) theo phương pháp NASCET, dựa vào chỉ số đường kính lòng mạch hẹp (A) và đường kính lòng mạch bình thường sau hẹp (B), với công thức là: (B-A)/B 100%. A B TẠP CHÍ NGHIÊN CỨU Y HỌC 4 TCNCYH 142 (6) - 2021 Phân tích thống kê Các giá trị của mức độ hẹp được ghi lại bằng các phương tiện số học và độ lệch chuẩn, hệ số tương quan Pearson r được thực hiện giữa kết quả CTA và DE xóa vôi hoá, thống kê Cohen’s κ-test cũng được sử dụng cho mức độ phù hợp giữa hai phương thức hình ảnh này (kappa < 0,2 = không đạt, 0,61 - 0,8 = tốt, 0,81 - 1 = rất tốt). So sánh trung bình của hai nhóm ghép cặp có phân phối chuẩn được thực hiện bằng kiểm định Paired-Sample T-Test, với nhóm nhỏ phân bố không chuẩn dùng kiểm định Wilcoxon ghép cặp. Tất cả các số liệu thống kê được phân tích bằng phần mềm SPSS (release 23.0; IBM, Chicago, IL). 4. Đạo đức nghiên cứu Đây là một phần của đề tài tốt nghiệp bác sỹ nội trú của tác giả và đã được thông qua hội đồng đề cương của trường Đại học Y Hà nội. Tất cả các qui trình kỹ thuật được thực hiện theo Dữ liệu thông tin là nghiên cứu mô tả không can thiệp, nên không ảnh hưởng đến quyền và nghĩa vụ của bệnh nhân tham gia nghiên cứu. Biểu đồ 1. Phân tán điểm số NASCET của DECT với CTA thể hiện mối quan hệ tuyến tính thuận (r = 0,996; p < 0,001) Tất cả các BN được đánh giá bằng DECT với chất lượng hình ảnh rất tốt (100%). Trong 27 BN có 16 trường hợp là mảng xơ vữa gây hẹp cả hai bên và đều ở đoạn phình cảnh, như vậy tổng có 43 động mạch cảnh được đánh giá, vị trí hẹp hoặc ở phình cảnh hoặc ở đoạn gần của ICA. Mảng xơ vữa loại hỗn hợp có chiếm 74,4%, xơ vữa vôi hoá chiếm 18,6%, xơ vữa mềm ít gặp nhất (7,0%). Có mối tương quan tuyến tính giữa mức độ hẹp theo phương pháp NASCET trên CTA và DECT sự tương quan này chặt chẽ với r = 0,996; p < 0,001 (Biểu đồ 1). Có sự phù hợp với mức độ rất tốt giữa hai phương thức chẩn đoán này trong đánh giá mức độ hẹp động mạch cảnh trong với hệ số Kappa = 0.812. Đáng chú ý là với mức hẹp từ 70-99% là mức có chỉ định can thiệp điều trị, CTA đánh giá quá mức độ hẹp này, 17 trường hợp (37,5%) hẹp so với 13 trường hợp (30,2%) hẹp trên DECT (Bảng 1). Mức độ hẹp trung bình động P h ầ n t ră m h ẹ p C TA Phần trăm hẹp DSCT III. KẾT QUẢ Nghiên cứu gồm có 27 bệnh nhân (BN), 23 nam và 4 nữ (tỷ lệ 5,75:1). Tuổi trung bình là 69 ±10 tuổi (45 - 85); trong đó có 21 BN (92,6%) có triệu chứng lâm sàng, gồm nhồi máu não nhẹ (44,4%) và thiếu máu não thoảng qua (48,1%). Các BN đều có một hay nhiều yếu tố nguy cơ kèm theo như tăng huyết áp, đái đường, rối loạn lipid máu; trong đó tăng huyết áp chiếm tỷ lệ cao nhất (85,2%). Biểu đồ 1. Phân tán điểm số NASCET của DECT với CTA th hiện mối quan hệ tuyến tính thuận (r = 0,996; p < 0,001) Tất cả các BN được đánh giá bằng DECT với chất lượng hình ảnh rất tốt (100%). Trong 27 BN có 16 trường hợp là mảng xơ vữa gây hẹp cả hai bên và đều ở đoạn phình cảnh, như vậy tổng có 43 động mạch cảnh được đánh giá, vị trí hẹp hoặc ở phình cảnh hoặc ở đoạn gần của ICA. Mảng xơ vữa loại hỗn hợp có chiếm 74,4%, xơ vữa vôi hoá chiếm 18,6%, xơ vữa mềm ít gặp nhất (7,0%). Có mối tương quan tuyến tính giữa mức độ hẹp theo phương phá NASCET trên CTA và DECT sự tương quan này chặt chẽ với r = 0,996; p < 0,001 (Biểu đồ 1). Có sự phù hợp với mức độ rất tốt giữa hai phương thức chẩn đoán này trong đánh giá mức độ h động mạch cản trong với hệ số Kappa = 0,812. Đáng chú ý là với mức hẹp từ 70 - 99% là mức có chỉ định can thiệp điều trị, CTA đánh giá quá mức độ hẹp này, 17 trường hợp (37,5%) hẹp so với 13 trường hợp (30,2%) hẹp trên DECT (Bảng 1). Mức độ hẹp trung bình động mạch cảnh đo trên hình ảnh CTA và DECT lần lượt là 63,3 ± 25,0% và 59,5 ± 24,4%. Tỷ lệ mức độ hẹp giữa hai nhóm này là khác biệt có ý nghĩa thống kê với p < 0,001, nhất là ở mảng xơ vữa có vôi hoá đơn thuần và hỗn hợp (Bảng 2). TẠP CHÍ NGHIÊN CỨU Y HỌC 5TCNCYH 142 (6) - 2021 Bảng 1. Độ phù hợp giữa hình ảnh CTA thường qui và DECT trong phân loại mức độ hẹp động mạch cảnh DECT CTA 1 - 29% 30 - 49% 50 - 69% 70 - 99% 100% Tổng (%) 1 - 29% 6 0 0 0 0 06 (14,0) 30 - 49% 0 6 0 0 0 06 (14,0) 50 - 69% 0 2 10 0 0 12 (27,9) 70 - 99% 0 0 4 13 0 17 (39,5) 100% 0 0 0 0 2 02 (04,6) Tổng (%) 06 (14,0) 08 (18,6) 14 (32,6) 13 (30,2) 02 (04,6) 43 (100) Kappa = 0,812 Bảng 2. So sánh mức độ hẹp trung bình của động mạch cảnh trên ảnh CTA và DECT theo loại xơ vữa Kỹ thuật Loại xơ vữa CTA DECT p Xơ vữa mềm (n = 3) 54,7 ± 02,5 53,7 ± 02,3 0,200 Xơ vữa hỗn hợp (n = 32) 70,3 ± 24,5 66,2 ± 24,1 0,000 Xơ vữa vôi hoá (n = 8) 38,8 ± 12,2 36,3 ± 12,3 0,011 Tổng (n = 43) 63,3 ± 25,0 59,5 ± 24,4 0,000 IV. BÀN LUẬN Chụp DECT được đặc trưng bởi sự thực hiện của 2 bộ dữ liệu ảnh ở 2 phổ tia X khác nhau. Có 2 cơ chế chính gây ra sự khác biệt về suy giảm tia X phụ thuộc vào vật liệu, đó là tán xạ compton và hiệu ứng quang điện. Loại thứ hai phụ thuộc nhiều vào mật độ nguyên tử của vật liệu được khảo sát, trong khi loại thứ nhất phụ thuộc nhiều hơn vào kích thước mô được chiếu xạ, chất lượng chùm tia và năng lượng chùm tia. Dựa trên những đặc điểm này, DECT cho phép phân biệt giữa các vật liệu khác nhau có số nguyên tử cao, chẳng hạn như iốt và canxi. Thuật toán ở đây áp dụng là loại bỏ vật liệu canxi và để lại một hỗn hợp vật liệu mô mềm và iốt. Điều này cho phép loại bỏ hoàn toàn vôi hoá và tránh lượng vôi hoá còn lại chồng lấp trong hình ảnh iốt của CTA. Một số nghiên cứu cho đến nay đều cho thấy tính hữu ích của chụp mạch DECT để mô tả các động mạch cảnh ngoài sọ có loại bỏ xương so với ảnh CTA thông thường.10,11,12 Trong các vị trí hẹp thường gặp, hẹp tại phình cảnh đứng đầu, theo sau đó là động mạch cảnh trong. Kết quả này phù hợp với xu hướng hình thành mảng tại chỗ chia đôi, nơi có tốc độ máu chảy cao và các dòng xoáy máu. Về tính chất của mảng xơ vữa, mảng xơ vữa hỗn hợp là thường gặp nhất.4 Những mảng xơ vữa TẠP CHÍ NGHIÊN CỨU Y HỌC 6 TCNCYH 142 (6) - 2021 có vôi hoá, đặc biệt là những mảng xơ vữa có vôi hoá nhiều ảnh hưởng rất lớn đến việc phân loại mức độ hẹp. Khi so sánh mức độ hẹp giữa CTA và DECT, nghiên cứu này cho thấy khác biệt giữa trước và sau khi loại bỏ vôi hoá, mức độ hẹp của CTA lớn hơn so với DECT xoá vôi hoá. Do hầu hết các động mạch cảnh trong nghiên cứu của chúng tôi đều có sự hiện diện của vôi hoá (93%), nên sẽ ảnh hưởng đến việc đo lường mức độ hẹp của lòng mạch. Những trường hợp vôi hóa lớn dạng vòng trong thành động mạch gây che lấp lòng mạch, trên CTA trên ảnh MIP có thể đánh giá quá mức độ hẹp (H2.A), nhưng với thuật toán của DECT, các mảng vôi hóa đã được loại bỏ một cách hiệu quả, dẫn đến giảm đáng kể hiện tượng tạo khối trong khi vẫn giữ được chất lượng hình ảnh, có thể nói tương tự như ảnh chụp mạch DSA (H2.B). Nghiên cứu của Mannil và cs13 cũng cho thấy DECT giúp loại bỏ các mảng bám vôi hóa thành mạch cảnh và do đó cải thiện việc định lượng hẹp động mạch cảnh tốt hơn so với sử dụng hình ảnh CTA thông thường. Ngay cả trong những trường hợp vôi hóa nhẹ, độ hẹp NASCET trung bình đo trên DECT vẫn thấp hơn 9% so với đo trên CTA thông thường. Tương tự, nghiên cứu Uotani và cs7 cho thấy tỷ lệ hẹp động mạch cảnh dương tính giả của DECT giảm so với CTA thông thường. So sánh với MRA với DECT, xác định mức độ hẹp ICA của MRA tương đương với DECT.2,4,14 Nhưng theo Korn và cs4 cho thấy MRA đánh giá xơ vữa vôi hoá kém hơn DECT và cho rằng do các mảng vôi hóa cung cấp thông tin quan trọng cho bác sĩ can thiệp hoặc bác sĩ phẫu thuật và cung cấp giá trị tiên lượng cho những bệnh nhân phân tầng nguy cơ bị hẹp không triệu chứng, vì vậy DECT nên được xem xét ở những bệnh nhân hẹp động mạch cảnh có xơ vữa vôi hóa lớn. So sánh DECT với chụp mạch DSA, nghiên cứu của Mannil đã chỉ không có sự khác biệt trong đánh giá hẹp giữa hai phương thức này.13 Nghiên cứu của Uotani và cs7 cũng chỉ ra mối tương quan chặt chẽ khi đối chiếu mức độ hẹp giữa ảnh DECT và ảnh DSA (r = 0,95) và đưa ra kết luận rằng với khả năng xoá mảng xơ vữa vôi hoá, DECT rất hữu ích trong việc đánh giá mức độ hẹp ở những động mạch cảnh có vôi hoá nhiều. Kỹ thuật này cũng có những hạn chế cần được nhắc đến là chất lượng hình ảnh không đủ có thể nhiễu gây đánh giá sai mức độ hẹp, ví dụ nhiễu ảnh do phục hình nha khoa bằng kim loại. Ngoài ra thuật toán loại bỏ canxi của DECT có thể loại bỏ một phần iốt cũng như do quá trình hiệu chuẩn của loại bỏ vật liệu cơ bản.13 Hạn chế của nghiên cứu là chúng tôi thu thập được một số lượng tương đối thấp và không có đối chứng với tiêu chuẩn vàng chụp mạch DSA. Tuy nhiên, nghiên cứu này đại diện cho bằng chứng với kết quả mạnh mẽ về một thuật toán loại bỏ canxi của DECT. Các suy luận chung về các hạn chế của thuật toán cần được xác nhận trong các nghiên cứu lớn hơn. V. KẾT LUẬN Nghiên cứu của chúng tôi góp phần làm sáng tỏ tính ứng dụng cao của kỹ thuật loại bỏ vôi hoá trên DECT trong chẩn đoán mức độ hẹp của động mạch cảnh ngoài sọ. Kỹ thuật này có thể khắc phục việc đánh giá quá mức mức độ hẹp CTA thường qui do hiện tượng chồng lấp các mảng vôi hóa. Lời cảm ơn Chúng tôi xin chân thành cảm ơn các đồng nghiệp khoa CĐHA và đơn vị đột quỵ, bệnh viện Saint Paul đã giúp đỡ chúng tôi hoàn thành nghiên cứu này. Xung đột lợi ích và tài chính: Không TẠP CHÍ NGHIÊN CỨU Y HỌC 7TCNCYH 142 (6) - 2021 TÀI LIỆU THAM KHẢO 1. Barrett KM, Brott TG. Stroke caused by extracranial disease. Circ Res. 2017; 120: 496–501. 2. Nederkoorn PJ, van der Graaf Y, Hunink MGM. Duplex ultrasound and magnetic resonance angiography compared with digital subtraction angiography in carotid artery stenosis. Stroke. 2003; 34(5):1324–32. 3. Josephson SA, Bryant SO, Mak HK, et al. Evaluation of carotid stenosis using CT angiography in the initial evaluation of stroke and TIA. Neurology. 2004; 63: 457–460. 4. Korn A, Bender B, Brodoefel H, et al. Grading of carotid artery stenosis in the presence of extensive calcifications: dual- energy CT angiography in comparison with contrast-enhanced MR angiography. CJCn. 2013; 25(1): 33-40. 5. Marks MP, Napel S, Jordan JE, et al. Diagnosis of carotid artery disease: preliminary experience with maximum-intensity- projectionspiral CT angiography. AJR Am J Roentgenol. 1993; 160: 1267–71. 6. Thomas C, Korn A, Krauss B, et al. Automatic bone and plaque removal using dual energy CT for head and neck angiography: feasibility and initial performance evaluation. UJEjoR. 2010; 76(1):61-67. 7. Uotani K, Watanabe Y, Higashi M, et al. Dual-energy CT head bone and hard plaque removal for quantification of calcified carotid stenosis: utility and comparison with digital subtraction angiography. JEr. 2009; 19(8): 2060-2065. 8. Naruto, N, Itoh, T, & Noguchi, K. Dual energy computed tomography for the head. Japanese Journal of Radiology. 2017; 36(2): 69–80. 9. Das M, Braunschweig T, Mühlenbruch G, et al. Carotid plaque analysis: comparison of dual-source computed tomography (CT) findings and histopathological correlation. 2009;38(1):14-19. 10. Morhard D, Fink C, Graser A, et al. Cervical and cranial computed tomographic angiography with automated bone removal: dual energy computed tomography versus standard computed tomography. Invest Radiol. 2009; 44: 293–297. 11. Lell MM, Kramer M, Klotz E, et al. Carotid computed tomography angiography with automated bone suppression: a comparative study between dual energy and bone subtraction techniques. Invest Radiol. 2009; 44:322–328. 12. Kaemmerer N, Brand M, Hammon M, et al. Dual-energy computed tomography angiography of the head and neck with single- source computed tomography: a new technical (Split Filter) approach for bone removal. Invest Radiol. 2016; 51: 618–623. 13. Mannil M, Ramachandran J, de Martini IV, et al. Modified dual-energy algorithm for calcified plaque removal: evaluation in carotid computed tomography angiography and comparison with digital subtraction angiography. SJIR. 2017; 52(11): 680-685. 14. Lv P, Lin J, Guo D, et al. Detection of carotid artery stenosis: a comparison between 2 unenhanced MRAs and dual-source CTA. American Journal of Neuroradiology. 2014; 35(12): 2360-2365. TẠP CHÍ NGHIÊN CỨU Y HỌC 8 TCNCYH 142 (6) - 2021 Summary DUAL ENERGY COMPUTED TOMOGRAPHY IN EVALUATION OF CERVICAL CAROTID CALCIFIED PLAQUE STENOSIS Dual Energy Computed Tomographic Angiography (DECT) with calcified plaque removal was compared with conventional CTA in the evaluation of the the degree of stenosis of the internal carotid artery (ICA). 43 stenosis ICA in 27 patients were assessed according to the North American Symptomatic Carotid Endarterectomy Trial (NASCET) criteria on both CTA and DECT techniques. There is a very good agreement between these two diagnostic methods in the evaluation of stenosis ICA with Kappa coefficient = 0.812. The average stenosis ICA measured on conventional CTA and DECT images were 63.3 ± 25.0% and 59.5 ± 24.4%, respectively (p < 0.001). Thus, DECT for calcified plaque removal facilitated the assessment of stenosis in all ICA and performed better than the conventional CTA. Keywords: Carotid stenosis, Calcified plaque, Dual energy CTA.
File đính kèm:
 cat_lop_vi_tinh_hai_muc_nang_luong_trong_danh_gia_hep_xo_vua.pdf
cat_lop_vi_tinh_hai_muc_nang_luong_trong_danh_gia_hep_xo_vua.pdf

