So sánh phương pháp bertrand và phương pháp chuẩn độ phức chất, ứng dụng xác định đường khử trong trái cây
Trong nghiên cứu này, chúng tôi thiết lập phƣơng pháp chuẩn độ phức chất để xác định đƣờng
khử trong một số loại trái cây. Kết quả này đƣợc so sánh với phƣơng pháp Bertrand. Một số yếu tố nhƣ
dung môi trích ly, thời gian trích ly, độ lặp, độ đúng và hiệu suất thu hồi của phƣơng pháp đã đƣợc khảo
sát. Mẫu phân tích so sánh đã đƣợc gởi đến Trung tâm kỹ thuật tiêu chuẩn đo lƣờng chất lƣợng 3
(QUATEST 3). Kết quả nhận đƣợc đã minh chứng cho độ đúng của phƣơng pháp. Phƣơng pháp chuẩn độ
phức chất này có nhiều ƣu điểm so với phƣơng pháp Bertrand nhƣ thời gian phân tích nhanh hơn, độ
chính xác cao hơn

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5

Trang 6
Bạn đang xem tài liệu "So sánh phương pháp bertrand và phương pháp chuẩn độ phức chất, ứng dụng xác định đường khử trong trái cây", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: So sánh phương pháp bertrand và phương pháp chuẩn độ phức chất, ứng dụng xác định đường khử trong trái cây

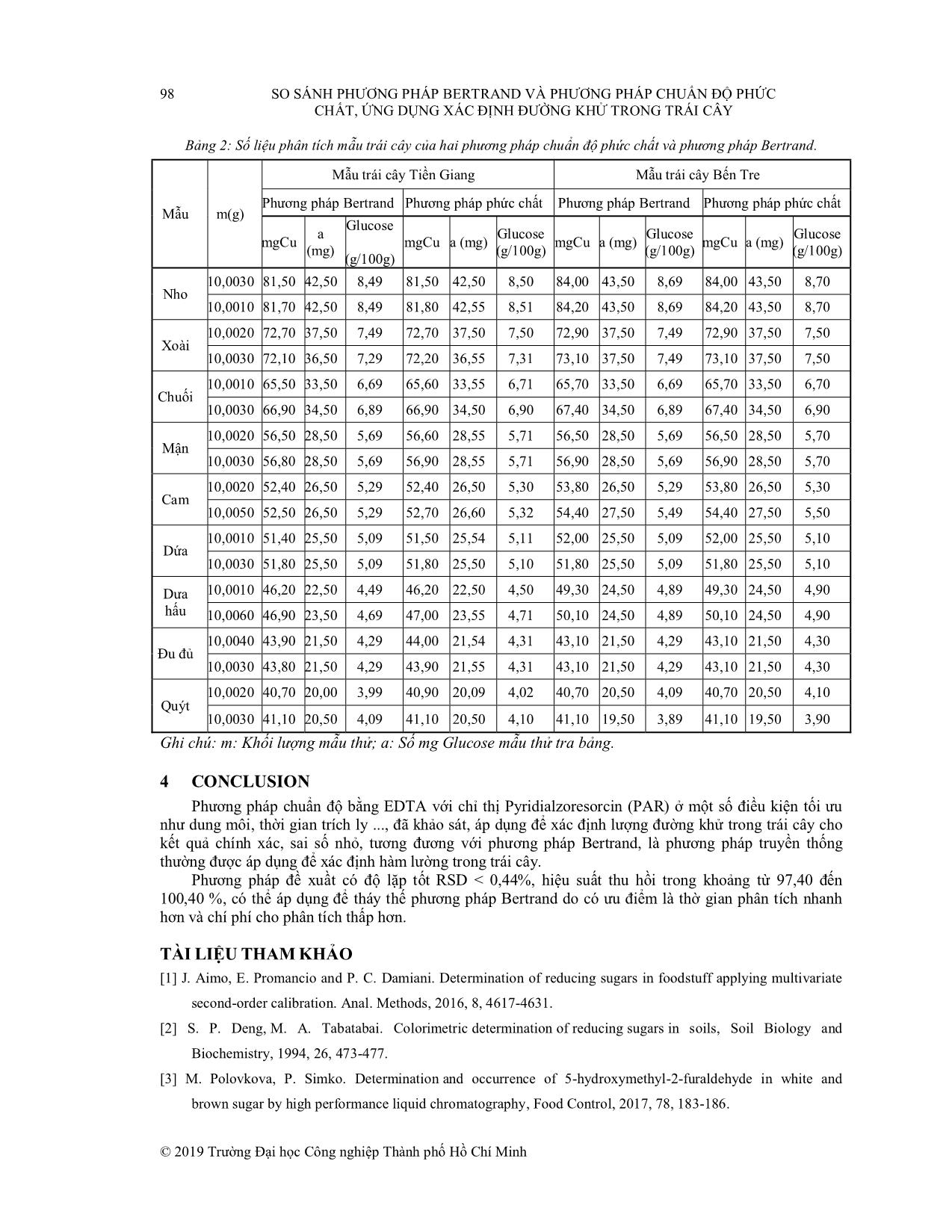
Tạp chí Khoa học và Công nghệ, Số 39B, 2019 © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY VAN TRONG NGUYEN Khoa công nghệ hóa học, Trường Đại học Công nghiệp Thành phố Hồ Chí Minh nguyenvantrong@iuh.edu.vn Tóm tắt. Trong nghiên cứu này, chúng tôi thiết lập phƣơng pháp chuẩn độ phức chất để xác định đƣờng khử trong một số loại trái cây. Kết quả này đƣợc so sánh với phƣơng pháp Bertrand. Một số yếu tố nhƣ dung môi trích ly, thời gian trích ly, độ lặp, độ đúng và hiệu suất thu hồi của phƣơng pháp đã đƣợc khảo sát. Mẫu phân tích so sánh đã đƣợc gởi đến Trung tâm kỹ thuật tiêu chuẩn đo lƣờng chất lƣợng 3 (QUATEST 3). Kết quả nhận đƣợc đã minh chứng cho độ đúng của phƣơng pháp. Phƣơng pháp chuẩn độ phức chất này có nhiều ƣu điểm so với phƣơng pháp Bertrand nhƣ thời gian phân tích nhanh hơn, độ chính xác cao hơn Từ khóa. Đƣờng khử; trái cây; phức chất; phƣơng pháp Bertrand. COMPARISION BETWEEN BERTRAND METHOD AND COMPLEX TITRATION, APPLYING TO DETERMINE SUGAR CONTENT IN FRUIT Abstract. In this study, a method of complex titration to determine sugar content in a variety of fruits was established and the results are compared with Bertrand method. A range of parameters including extracting solvent, time of extraction, repeatability and accuracy of the method were investigated. The fruit samples were sent to Quality Assurance and Testing Center 3 (QUATEST 3) for testing and it is proved a high correlation between these tests. This method was also providing more superior features including short analytical time, higher accuracy in comparison with Bertrand method. Keyword. Reduced sugar, complexes, Bertrand. 1 GIỚI THIỆU Đƣờng khử là các loại đƣờng có chứa nhóm aldehyde (-CHO) nhƣ đƣờng glucose, fructose, arabinose, maltose, lactose có công thức chung là C6H12O6 [1-2], đƣờng khử thƣờng có nhiều trong thực vật nhƣ củ cải đƣờng, các loại trái cây có vị ngọt. Trong công nghiệp đƣờng thƣờng đƣợc dùng làm trong sản xuất thực phẩm nhƣ bánh kẹo, nƣớc ngọt , ngoài ra chúng còn đƣợc sử dụng trong một số lĩnh vực công nghiệp khác [3-4]. Đƣờng có vai trò quan trọng đối với cơ thể con ngƣời, nó cung cấp năng lƣợng chính cho cơ thể, duy trì hoạt động chức năng thần kinh trung ƣơng, mỗi ngày một ngƣời cần 100-120 g đƣờng, đƣờng huyết phải ở mức bình thƣờng mới có thể duy trì chức năng của não bộ, đƣờng huyết giảm sẽ ảnh hƣởng tới chức năng não bộ và có thể dẫn đến bệnh hạ đƣờng huyết. Tuy nhiên, khi sử dụng đƣờng dƣ thừa đƣờng sẽ tích tụ trong gan làm gan nhiễm mỡ suy giảm chức năng gan là nguyên nhân làm xuất hiện các căn bệnh khác nhau trong đó có bệnh tiểu đƣờng [5]. Việt Nam là một nƣớc nhiệt đới, có nhiều loại trái cây nhƣ chuối, quýt, táo, xoài, nho mận, cam, dứa, đu đủ , đƣờng trong các loại trái cây chủ yếu là loại đƣờng fructose một loại đƣờng khử, việc xác định đánh giá hàm lƣợng của chúng có trong các loại trái cây trên nhằm mục đích khuyến cáo ngƣời tiêu dùng có ý thức về hàm lƣợng đƣờng khi sử dụng. Trƣớc đây để xác định đƣờng khử thƣờng sử dụng các phƣơng pháp truyền thống nhƣ Bertrand, Luff-Shoorl Đối với phƣơng pháp Bertrand [6-7], đƣờng khử phản ứng với dung dịch Felling A (CuSO4, H2SO4) và B (NaOH, KNaC4H4O6) trong môi trƣờng kiềm sinh ra một lƣợng Cu2O tƣơng ứng với lƣợng đƣờng khử, lọc và hòa tan lƣợng Cu2O bằng H2SO4 và chuẩn độ lƣợng Cu2O sinh ra bằng dung dịch KMnO4. Từ đó tính số miligam Cu sinh ra và tra bảng thực nghiệm của Bertrand [6] sẽ tìm đƣợc hàm lƣợng đƣờng khử. Phƣơng pháp này đơn giản, có độ chính xác cao, tuy nhiên mất nhiều thời gian và còn nhiều nhƣợc điểm nhƣ lƣợng Cu2O sinh ra phải đƣợc lọc, rửa kỹ tránh tiếp xúc với không khí. Để SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC 95 CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh khắc phục tình trạng trên, Luff-Shoorl phát triển phƣơng pháp Betrand, bằng cách sử dụng một lƣợng dung dịch Felling A có chứa lƣợng Cu2+ dƣ chính xác, sau đó xác định hàm lƣợng Cu2+ dƣ bằng phƣơng pháp chuẩn độ iod, từ đó tính ra hàm lƣợng đƣờng khử [8]. Gần đây, T. Kolusheva và cộng sự [8], đã xây dựng một phƣơng pháp xác định nhanh đƣờng khử trong tinh bột bằng phƣơng pháp chuẩn độ phức chất, kết quả của nghiên cứu cho thấy phƣơng pháp có độ chính xác cao với độ lệch chuẩn < 1%, khoảng nồng độ từ 10 g/L tới 200 g/L. Ngoài ra một số phƣơng pháp nhƣ quang phổ UV-VIS [1, 2, 9, 10], HPLC [3], điện hóa [11] cũng đƣợc sử dụng để xác định hàm lƣợng đƣờng thấp có trong một số loại trái cây. Các phƣơng pháp này sử dụng thiết bị, hóa chất và điều kiện phân tích tƣơng đối đắt tiền dẫn đến chi phí phân tích cao. Trong bài báo này chúng tôi công bố kết quả nghiên cứu cải tiến phƣơng pháp Bertrand. Kết quả phân tích đƣợc so sánh với phƣơng pháp Bertrand truyền thống. Hy vọng kết quả thu đƣợc sẽ đóng góp them một phƣơng pháp phân tích mới để xác định hàm lƣợng đƣờng trong trái cây ở nƣớc ta. Trong phƣơng pháp này, chúng tôi sử dụng một lƣợng Cu2+ trong dung dịch Felling A dƣ chính xác, sau khi đƣờng khử phản ứng với dung dịch Felling A và B sẽ tạo thành một lƣợng Cu2O tƣơng ứng. Ethylendiamine tetraacetic acid (EDTA) đã đƣợc sử dụng để chuẩn lƣợng Cu2+ còn dƣ sau khi lọc, từ đó tính ra số miligam Cu đã phản ứng, dựa vào bảng tra thực nghiệm sẽ tìm đƣợc hàm lƣợng đƣờng tƣơng ứng. Bằng cách này chúng tôi hy vọng sẽ thiết lập đƣợc phƣơng pháp phân tích hàm lƣợng đƣờng khử nhanh, chính xác và tiết kiệm chi phí. 2 THỰC NGHIỆM 2.1. Thiết bị và hóa chất Thiết bị, dụng cụ sử dụng trong nghiên cứu này gồm có cân phân tích có độ chính xác 4 số sau dấu phẩy, máy lắc, bếp điện, bộ lọc chân không. Một số loại thủy tinh nhƣ buret, pipet, erlen, bình định mức hãng Duran của Đức Hóa chất, ống chuẩn KMnO4 0,1 N và EDTA 0,05 M đƣợc mua từ hãng Merck của Đức, đƣờng chuẩn D-(+)-Glucose (> 99,5%) đƣợc mua từ hãng Sigma của Mỹ, các hóa chất khác có độ tinh khiết cao (P.A). Nƣớc cất đƣợc sử dụng là loại nƣớc cất hai lần, không ion. Dung dịch Felling A đƣợc chuẩn bị bằng cách hòa tan 34,6390 gam CuSO4.5H2O trong nƣớc và định mức tới vạch 500 mL bằng nƣớc cất Dung dịch Felling B đƣợc chuẩn bị bằng cách hòa tan 51,60 gam NaOH và 173,00 gam kali-natri tartrate (KNaC4H4O6.4H2O) rồi định mức thành 500 mL bằng nƣớc cất. Dung dịch đệm acetat (pH 5) đƣợc chuẩn bị nhƣ sau: Thêm cẩn thận 400 mL dung dịch có chứa 80 g NaOH vào 600 mL dung dịch CH3COOH (có chứa 140 mL dung dịch CH3COOH băng). Chỉ thị Pyridialzoresorcin (PAR): Trộn 0,2500 g PAR với 25,00 g KNO3 khan, nghiền và đựng trong chai sành bảo quản nơi khô ráo. Dung dịch Fe2(SO4)3 5 %: Hòa tan 50,00 g Fe2(SO4)3 tẩm bằng 20mL H2SO4 đậm đặc hòa tan hoàn toàn bằng nƣớc cất rồi định mức tới 1000mL. 2.2. Quy trình phân tích 2.2.1. Chuẩn bị mẫu Mẫu trái cây đƣợc thu thập từ hai tỉnh Tiền Giang và Bến Tre gồm các loại nhƣ chuối cau, quýt cái bè, táo ta, xoài cát Hòa Lộc, nho mận, cam, dứa, đu đủ . Trái cây đƣợc rửa sạch, lau khô và bảo quản trong tủ lạnh 5 0C. Trái cây đƣợc lột vỏ, bỏ hạt lấy phần ăn đƣợc từ 5 đến 10 trái tùy thuộc vào kích cỡ của trái, sao cho tổng khối lƣợng mẫu khoảng từ 100 đến 200 g đem xay nhiễn đồng nhất. Sau đó cân chính xác khoảng 10 g mẫu đã đƣợc xay nhiễn cho vào cốc có dung tích 250 mL, thêm 30 mL dung dịch trích ly, đun trên bếp cách thủy ở 80 0C trong 15 phút, lấy ra để nguội, lắng gạn lấy phần dung dịch cho vào bình định mức 500 mL. Lặp lại quá trình ly trích trên 3 lần, gộp tất cả các phần dung dịch thu đƣợc vào bình định mức 500 mL, thêm 1 mL kaliferocyanua 15 %, lắc đều và để yên 2 - 3 phút và 5 mL kẽm acetat 30 %, đậy nắp và lắc khoảng 10 phút, làm nguội và dùng nƣớc cất định mức đến vạch. Để yên 15 phút, lọc dung dịch rửa tạp bằng nƣớc cất nóng cho sạch, dung dịch này đƣợc đem đi xác định hàm lƣợng đƣờng. [12] 96 SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh 2.2.2. Quy trình phân tích Phương pháp Bertrand: Lấy 25 mL dung dịch mẫu sau lọc vào erlen 250 mL thêm 25 mL Felling A và 25 mL Felling B, lắc nhẹ và đun sôi 3 phút, lọc qua phễu thủy tinh xốp G4 với hệ thống hút chân không, giai đoạn này cần phải tránh Cu2O tiếp xúc với không khí và rửa sạch bằng nƣớc cất nóng sau cùng là cồn 90 0C. Sau đó hòa tan hoàn toàn kết tủa này bằng dung dịch 20 mL Fe2(SO4)3 5 %, thêm vào dung dịch 10 mL H2SO4 20%. Đun nóng dung dịch và chuẩn bằng KMnO4 0.1N đến khi dung dịch xuất hiện màu hồng nhạt bền vững trong 30 giây, ghi nhận thể tích KMnO4 tiêu tốn. Phương pháp chuẩn độ phức chất: Lấy 25 mL dung dịch mẫu sau lọc vào erlen 250 mL thêm 25 mL Felling A và 25 mL Felling B, lắc nhẹ và đun sôi 3 phút, lọc nhanh qua phễu thủy tinh xốp G4 với hệ thống hút chân không, giai đoạn này không phải quan tâm nhiều tới kết tủa Cu2O mà chúng ta cần rửa và gom toàn bộ nƣớc rửa và dung dịch lọc định mức thành 100 mL. Lấy 25 mL dung dịch này cho vào bình tam giác loại 100 mL, thêm vào bình 10 mL dung dịch đệm acetat (điều chỉnh pH khoảng 5 bằng CH3COOH), tiến hành chuẩn bằng EDTA 0,05 M với 0,1 g chỉ thị PAR đến khi dung dịch chuyển từ màu đỏ nho sang xanh lá, ghi nhận thể tích EDTA tiêu tốn. 2.2.3. Khảo sát dung môi và thời gian trích ly Trái mận đƣợc mua tại Tiền Giang đƣợc sử dụng trong nghiên cứu này. Sau khi xử lý mẫu đƣợc mô tả ở mục 2.2.1, hàm lƣợng đƣờng trong mận đƣợc xác định bằng phƣơng pháp chuẩn độ phức chất đƣợc nêu ở mục 2.2.2 chỉ thay đổi dung môi trích ly lần lƣợt là nƣớc cất nóng, HCl 10%, H2SO4 10 % và CH3COOH 10 %. Sau khi lựa chọn đƣợc dung môi trích ly thích hợp, chúng tôi tiếp tục khảo sát thời gian chiết tƣơng ứng là 3; 5; 10; 15; 20 và 25 phút. Trong suốt quá trình chiết chúng tôi duy trì đun cách thủy ở 80 0C. 2.2.4. Khảo sát độ lặp và độ đúng của phƣơng pháp Để khảo sát các yếu tố này, chúng tôi chọn 3 mẫu đại diện gồm chuối, quýt và táo đƣợc mua từ Bến Tre đem xử lý mẫu nhƣ phần 2.2.1. Chuẩn bị 12 mẫu cho mỗi loại trái cây, 6 mẫu tiến hành phân tích độ lặp, 6 mẫu còn lại thêm 5 mL dung dịch đƣờng chuẩn D-(+)-Glucose (1 mg/mL) để xác định hiệu suất thu hồi. 3 KẾT QUẢ VÀ THẢO LUẬN 3.1. Kết quả khảo sát dung môi và thời gian trích ly Đƣờng tồn tại trong mẫu trái cây rất khó có thể trích ly chúng ra khỏi nền mẫu, vì thế chúng tôi sử dụng một số loại dung môi nhƣ nƣớc cất nóng, HCl, H2SO4 hay CH3COOH để tìm đƣợc dung môi chiết thích hợp nhất. Kết quả cho thấy rằng với dung môi nƣớc cất nóng cho kết quả cao nhất với 5,9 (g Glucose/100g mận), với HCl 10 % là 4,8, với H2SO4 10 % là 5,1 và CH3COOH 10 % là 4,5 % (Hình 1). Dung môi trích ly là nƣớc cất đƣợc đun nóng ở 80 0C trên bếp cách thủy. Kết quả cho thấy chỉ sau 15 phút đƣờng trong mẫu đƣợc trích ly hoàn toàn (Hình 2). Hình 1: Biểu đồ thể hiện khả năng trích ly của dung môi với số gam Glucose/100g mận. Hình 2: Đồ thị thời gian trích ly (phút) với số gam Glucose/100g mận. 0 2 4 6 Nước cất nóng HCl 10% H2SO4 10% CH3COOH 10% H àm lư ợn g Gl uc os e (g /1 00 g) Dung môi trích ly 0 1 2 3 4 5 6 7 0 5 10 15 20 25 30 H àm lư ợn g Gl uc os e (g /1 00 g) Thời gian trích ly của nước cất nóng (phút) SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC 97 CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh Nhƣ vậy, dung dịch trích ly là nƣớc cất nóng và thời gian trích ly là 15 phút đun cách thủy ở 80 0C đƣợc lựa chọn cho các thí nghiệm tiếp theo. 3.2. So sánh giữa hai phƣơng pháp Đối với phƣơng pháp truyền thống Bertrand, khi lọc để tách kết tủa Cu2O cần phải tránh tiếp xúc với không khí, vì khi tiếp xúc Cu2O sẽ chuyển về CuO khi đó kết quả sẽ bị sai lệch, chí vì lý do trên việc lọc phải cẩn thận mất nhiều thời gian (2 giờ cho một mẫu) và phải có thiết bị lọc chân không dẫn đến không hiệu quả trong phân tích. Ngƣợc lại, đối với phƣơng pháp chuẩn độ nhanh hơn (1 giờ cho một mẫu), không cần lọc chân không mà kết quả vẫn có độ lặp, hiệu suất thu hồi từ 97,4 đến 100,4 % và kết quả chính xác tƣơng đƣơng với phƣơng pháp Bertrand. Để minh chứng cho điều này, chúng tôi tiến hành gởi mẫu tại Quatest 3. Kết quả đƣợc trình bày trong Bảng 1 cho thấy cả hai phƣơng pháp đều không sai khác nhau nhiều, có độ lặp tƣơng đồng với F(0,05; 5; 5) = 5,05 > Ftn cho cả 3 mẫu [5]. 3.3. Phân tích mẫu thử Chúng tôi lựa chọn 10 loại trái cây thông dụng đƣợc mua tại hai tỉnh Tiền Giang và Bến Tre. Đây là hai tỉnh có sản lƣợng trái cây nhiều nhất cả nƣớc; sau đó tiến hành phân tích bằng cả hai phƣơng pháp. Kết quả đƣợc thể hiện trong Bảng 2. Kết quả ở Bảng 2 cho thấy hàm lƣợng đƣờng trong nho cho kết quả cao nhất là 8,70 g và quýt thấp nhất là 4,0 g, kết quả này cũng phù hợp với kết quả tại Quatest 3 chứng nhận cũng nhƣ các kết quả nghiên cứu khác. [13]. Bảng 1: Số liệu so sánh giữa hai phương pháp chuẩn độ phức chất và phương pháp Bertrand. Mẫu m(g) V(mL) n Phƣơng pháp Bertrand Phƣơng pháp phức chất Hàm lƣợng glucose (g/100g) SD RSD a a+c H (%) a a+c H (%) Bertrand Phức chất Quatest 3 Ftn (g/100g) % Chuối 10,0012 5,0 6 33,83 38,73 98,00 33,88 38,79 98,20 6,70 6,79 6,80 1,0180 0,12 0,35 Quýt 10,0015 5,0 6 20,33 25,38 101,00 20,38 25,40 100,40 4,07 4,10 4,00 1,0240 0,09 0,44 Táo 10,0013 5,0 6 53,42 58,29 97,40 53,45 58,32 97,40 10,71 10,66 10,80 1,0731 0,15 0,28 Ghi chú: m: Khối lượng mẫu thử; V: Thể tích chuẩn D-(+)-Glucose 1mg/mL; n: Số lần thí nghiệm; a: Số mg Glucose mẫu thử tra theo bảng; a+c: Số mg Glucose mẫu thử + chuẩn tra theo bảng; H: Hiệu suất thu hồi của phương pháp; SD: Độ lệch chuẩn; RSD: Độ lệch chuẩn tương đối. 98 SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh Bảng 2: Số liệu phân tích mẫu trái cây của hai phương pháp chuẩn độ phức chất và phương pháp Bertrand. Mẫu m(g) Mẫu trái cây Tiền Giang Mẫu trái cây Bến Tre Phƣơng pháp Bertrand Phƣơng pháp phức chất Phƣơng pháp Bertrand Phƣơng pháp phức chất mgCu a (mg) Glucose (g/100g) mgCu a (mg) Glucose (g/100g) mgCu a (mg) Glucose (g/100g) mgCu a (mg) Glucose (g/100g) Nho 10,0030 81,50 42,50 8,49 81,50 42,50 8,50 84,00 43,50 8,69 84,00 43,50 8,70 10,0010 81,70 42,50 8,49 81,80 42,55 8,51 84,20 43,50 8,69 84,20 43,50 8,70 Xoài 10,0020 72,70 37,50 7,49 72,70 37,50 7,50 72,90 37,50 7,49 72,90 37,50 7,50 10,0030 72,10 36,50 7,29 72,20 36,55 7,31 73,10 37,50 7,49 73,10 37,50 7,50 Chuối 10,0010 65,50 33,50 6,69 65,60 33,55 6,71 65,70 33,50 6,69 65,70 33,50 6,70 10,0030 66,90 34,50 6,89 66,90 34,50 6,90 67,40 34,50 6,89 67,40 34,50 6,90 Mận 10,0020 56,50 28,50 5,69 56,60 28,55 5,71 56,50 28,50 5,69 56,50 28,50 5,70 10,0030 56,80 28,50 5,69 56,90 28,55 5,71 56,90 28,50 5,69 56,90 28,50 5,70 Cam 10,0020 52,40 26,50 5,29 52,40 26,50 5,30 53,80 26,50 5,29 53,80 26,50 5,30 10,0050 52,50 26,50 5,29 52,70 26,60 5,32 54,40 27,50 5,49 54,40 27,50 5,50 Dứa 10,0010 51,40 25,50 5,09 51,50 25,54 5,11 52,00 25,50 5,09 52,00 25,50 5,10 10,0030 51,80 25,50 5,09 51,80 25,50 5,10 51,80 25,50 5,09 51,80 25,50 5,10 Dƣa hấu 10,0010 46,20 22,50 4,49 46,20 22,50 4,50 49,30 24,50 4,89 49,30 24,50 4,90 10,0060 46,90 23,50 4,69 47,00 23,55 4,71 50,10 24,50 4,89 50,10 24,50 4,90 Đu đủ 10,0040 43,90 21,50 4,29 44,00 21,54 4,31 43,10 21,50 4,29 43,10 21,50 4,30 10,0030 43,80 21,50 4,29 43,90 21,55 4,31 43,10 21,50 4,29 43,10 21,50 4,30 Quýt 10,0020 40,70 20,00 3,99 40,90 20,09 4,02 40,70 20,50 4,09 40,70 20,50 4,10 10,0030 41,10 20,50 4,09 41,10 20,50 4,10 41,10 19,50 3,89 41,10 19,50 3,90 Ghi chú: m: Khối lượng mẫu thử; a: Số mg Glucose mẫu thử tra bảng. 4 CONCLUSION Phƣơng pháp chuẩn độ bằng EDTA với chỉ thị Pyridialzoresorcin (PAR) ở một số điều kiện tối ƣu nhƣ dung môi, thời gian trích ly ..., đã khảo sát, áp dụng để xác định lƣợng đƣờng khử trong trái cây cho kết quả chính xác, sai số nhỏ, tƣơng đƣơng với phƣơng pháp Bertrand, là phƣơng pháp truyền thống thƣờng đƣợc áp dụng để xác định hàm lƣờng trong trái cây. Phƣơng pháp đề xuầt có độ lặp tốt RSD < 0,44%, hiệu suất thu hồi trong khoảng từ 97,40 đến 100,40 %, có thể áp dụng để tháy thế phƣơng pháp Bertrand do có ƣu điểm là thờ gian phân tích nhanh hơn và chí phí cho phân tích thấp hơn. TÀI LIỆU THAM KHẢO [1] J. Aimo, E. Promancio and P. C. Damiani. Determination of reducing sugars in foodstuff applying multivariate second-order calibration. Anal. Methods, 2016, 8, 4617-4631. [2] S. P. Deng, M. A. Tabatabai. Colorimetric determination of reducing sugars in soils, Soil Biology and Biochemistry, 1994, 26, 473-477. [3] M. Polovkova, P. Simko. Determination and occurrence of 5-hydroxymethyl-2-furaldehyde in white and brown sugar by high performance liquid chromatography, Food Control, 2017, 78, 183-186. SO SÁNH PHƢƠNG PHÁP BERTRAND VÀ PHƢƠNG PHÁP CHUẨN ĐỘ PHỨC 99 CHẤT, ỨNG DỤNG XÁC ĐỊNH ĐƢỜNG KHỬ TRONG TRÁI CÂY © 2019 Trƣờng Đại học Công nghiệp Thành phố Hồ Chí Minh [4] J. F. Novales, et al. Shortwave-near infrared spectroscopy for determination of reducing sugar content during grape ripening, winemaking, and aging of white and red wines. Food Research International, 2009, 42, 285- 291. [5] Trần Cao Sơn. Sách thẩm định phƣơng pháp trong phân tích hóa học và vi sinh vật, Nhà xuất bản KH - KT Hà Nội. [6] Tiêu chuẩn Quốc gia, TCVN 5266:1990. Sản phẩm ong – Phƣơng pháp xác định đƣờng khử tự do. [7] Tiêu chuẩn Việt Nam, TCVN 4594:1988. Đồ hộp - Phƣơng pháp xác định đƣờng tổng số, đƣờng khử và tinh bột. [8] T. Kolusheva, A. Marinova. Fast complexonmetric method for analysis reducing sugars obtained during starch hydrolysis, Journal of University of Chemical Technology and Metallurgy, 2011, 46, 75-80. [9] B. Das, R. N. Sahoo, S. Pargal, et al. Quantitative monitoring of sucrose, reducing sugar and total sugar dynamics for phenotyping of water-deficit stress tolerance in rice through spectroscopy and chemometrics. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2018, 192, 41-51. [10] K. S. Naskan, et al. Spectrophotometric total reducing sugars assay based on cupric reduction. Talanta, 2016, 147, 162-168. [11] F. C. U. Santos, L. L. Paim, et al. Electrochemical determination of total reducing sugars from bioethanol production using glassy carbon electrode modified with graphene oxide containing copper nanoparticles. Fuel, 2016, 163, 112-121. [12] Hà Duyên Tƣ. Phân tích hóa học thực phẩm, Nhà xuất bản KH-KT Hà Nội, 2009. [13] https://thepaleodiet.com/fruits-and-sugars/ Ngày nhận bài: 02/07/2019 Ngày chấp nhận đăng: 03/10/2019
File đính kèm:
 so_sanh_phuong_phap_bertrand_va_phuong_phap_chuan_do_phuc_ch.pdf
so_sanh_phuong_phap_bertrand_va_phuong_phap_chuan_do_phuc_ch.pdf

