Nghiên cứu khả năng hấp phụ một số ion kim loại nặng trên đá ong tự nhiên và quặng apatit tự nhiên
This paper focus on Fe(III), Cr(VI), Mn(II), Ni(II) adsorption study results on natural laterite and
natural apatite ore. Some characteristics of the materials were investigated by SEM, BET, IR. Some
conditions that were effective to the removal of Fe(III), Cr(VI), Mn(II), Ni(II) using the materials such
as pH, materials size, contact time and initial concentration of the metal ions were systematically
studied. The optimum pH for removal Fe(III), Cr(VI), Mn(II), Ni(II) for both laterite and apatite ore
was 2.0, 2.5, 6.0, 6.0, respectively. The materials size was 0,1 0,2 mm. The optimum contact time for
removal Fe(III), Cr(VI), Mn(II), Ni(II) was 90 min, 120 min, 150 min and 150 min for laterite while it
was 120 min, 150 min, 150 min and 150 min for apatite ore, at room temperature (25 ± 2oC),
respectively. Maximum adsorption capacity for Fe(III), Cr(VI), Mn(II), Ni(II) on laterite was 2.72
mg/g; 4.57 mg/g; 1.68 mg/g and 4.34 mg/g while it was 3.02 mg/g; 3.50 mg/g; 2.65mg/g and 5.32
mg/g on apatite ore, respectively.

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5
Trang 6
Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Nghiên cứu khả năng hấp phụ một số ion kim loại nặng trên đá ong tự nhiên và quặng apatit tự nhiên

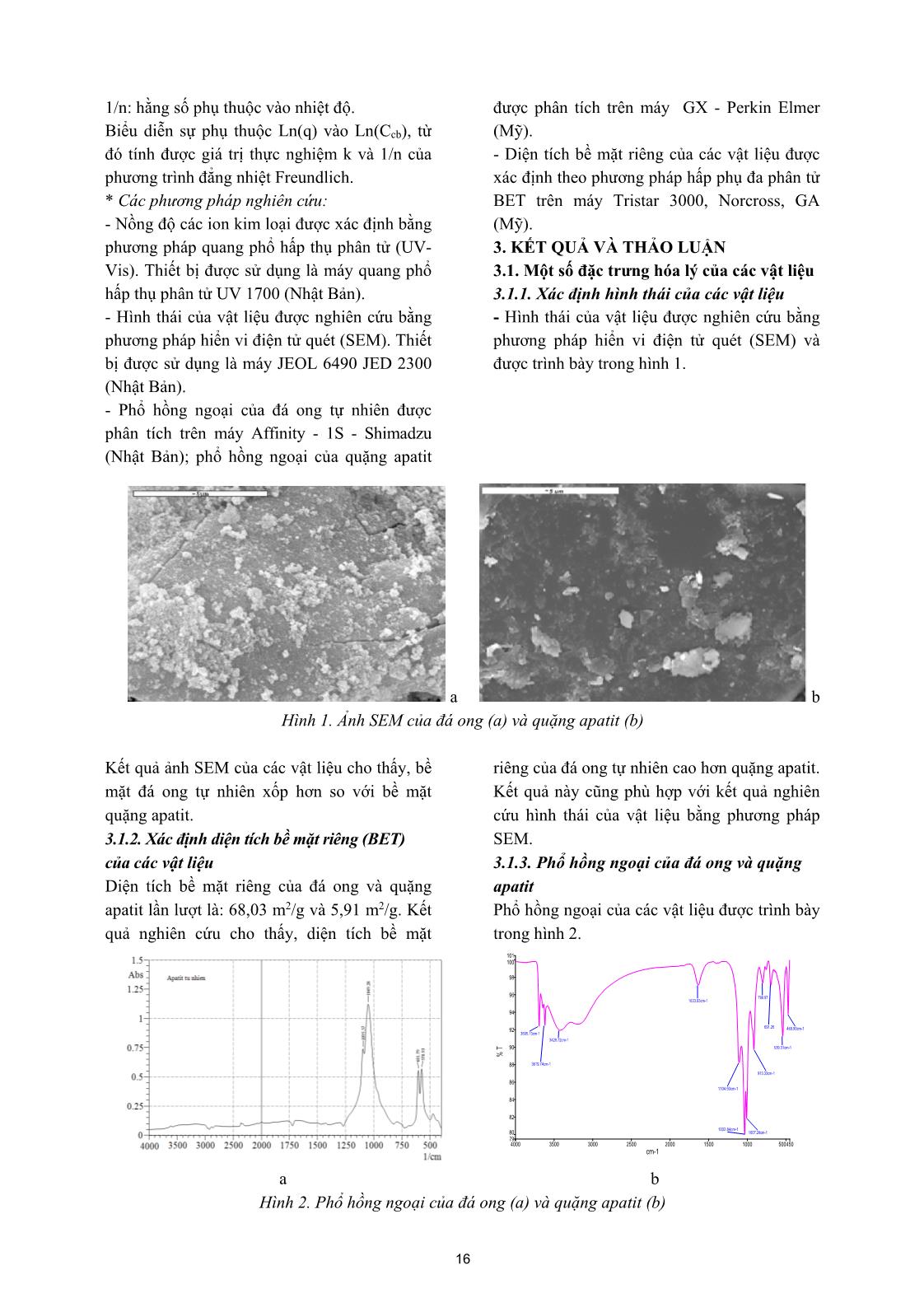
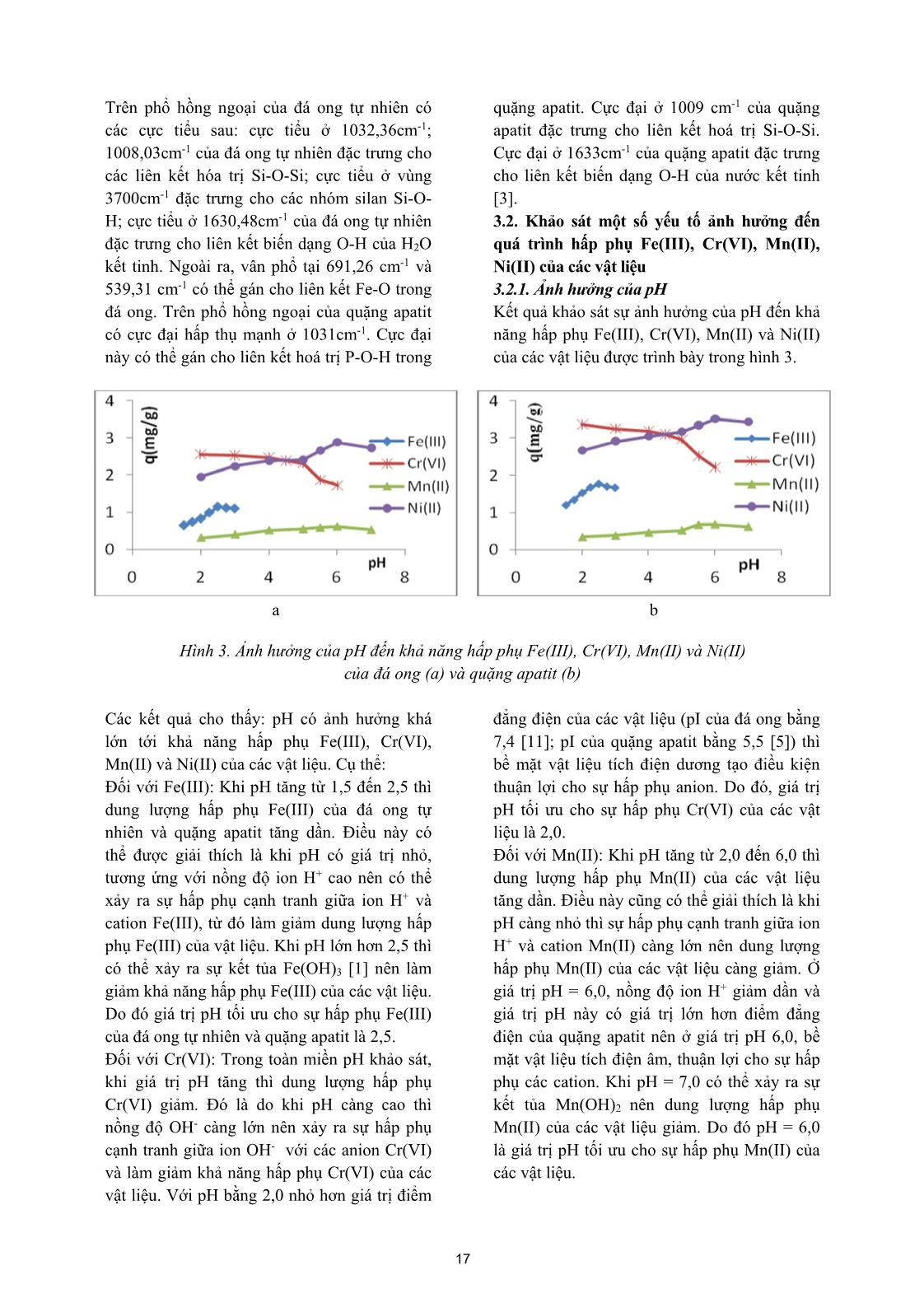
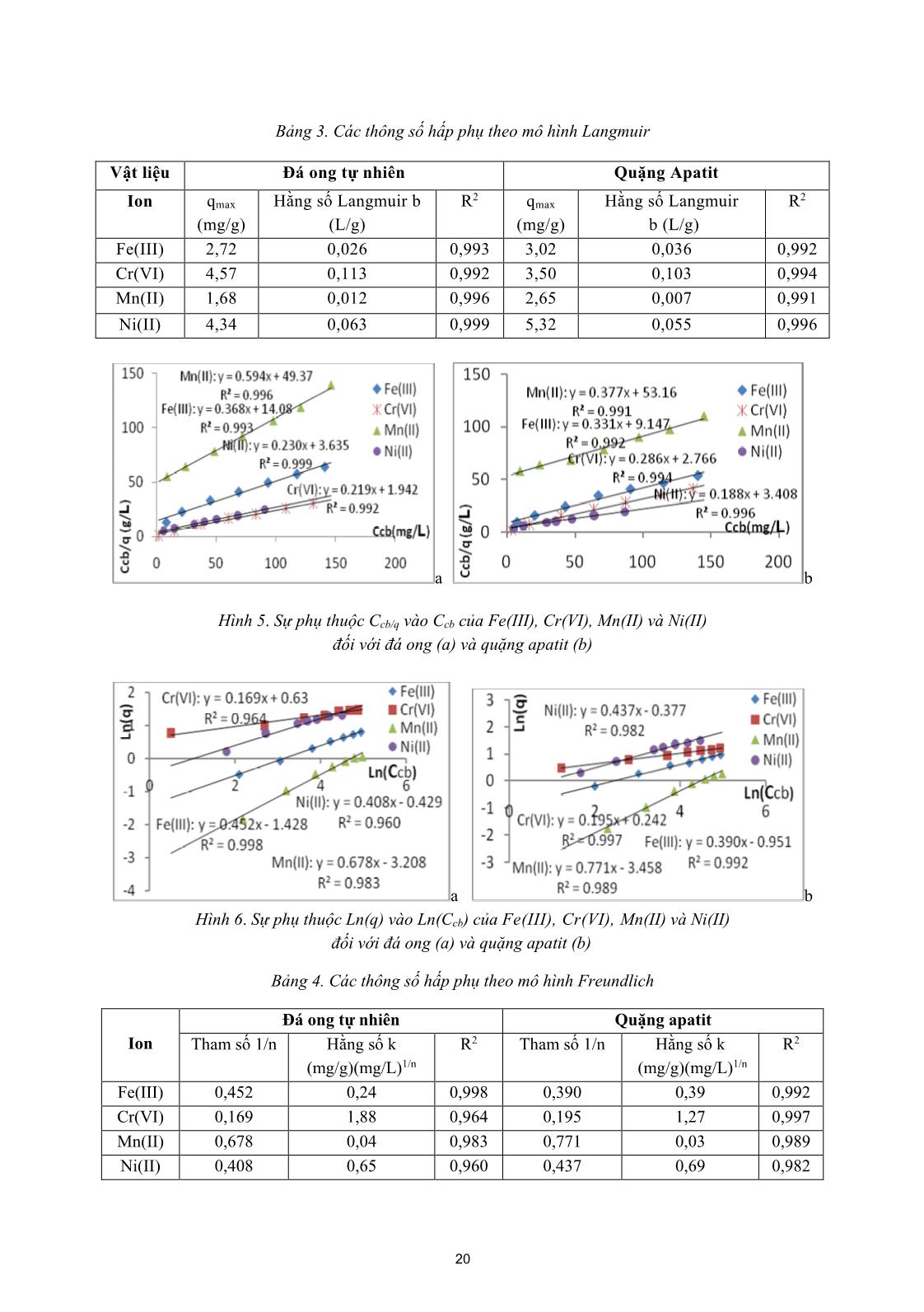
Tạp chí phân tích Hóa, Lý và Sinh học - Tập 25, Số 2/2020 NGHIÊN CỨU KHẢ NĂNG HẤP PHỤ MỘT SỐ ION KIM LOẠI NẶNG TRÊN ĐÁ ONG TỰ NHIÊN VÀ QUẶNG APATIT TỰ NHIÊN Đến toà soạn 20-11-2019 Ngô Thị Mai Việt, Dương Thị Tú Anh Khoa Hóa học – Trường Đại học Sư phạm Thái Nguyên SUMMARY STUDY ON ADSORPTION CAPACITY OF SOME HEAVY METAL IONS ON NATURAL LATERITE AND NATURAL APATITE ORE This paper focus on Fe(III), Cr(VI), Mn(II), Ni(II) adsorption study results on natural laterite and natural apatite ore. Some characteristics of the materials were investigated by SEM, BET, IR. Some conditions that were effective to the removal of Fe(III), Cr(VI), Mn(II), Ni(II) using the materials such as pH, materials size, contact time and initial concentration of the metal ions were systematically studied. The optimum pH for removal Fe(III), Cr(VI), Mn(II), Ni(II) for both laterite and apatite ore was 2.0, 2.5, 6.0, 6.0, respectively. The materials size was 0,1 0,2 mm. The optimum contact time for removal Fe(III), Cr(VI), Mn(II), Ni(II) was 90 min, 120 min, 150 min and 150 min for laterite while it was 120 min, 150 min, 150 min and 150 min for apatite ore, at room temperature (25 ± 2oC), respectively. Maximum adsorption capacity for Fe(III), Cr(VI), Mn(II), Ni(II) on laterite was 2.72 mg/g; 4.57 mg/g; 1.68 mg/g and 4.34 mg/g while it was 3.02 mg/g; 3.50 mg/g; 2.65mg/g and 5.32 mg/g on apatite ore, respectively. 1. MỞ ĐẦU Việc phát triển các ngành công nghiệp như công nghiệp mạ, công nghiệp khai khoáng hay luyện kim... đã góp phần phát triển kinh tế đất nước. Tuy vậy, mặt trái của quá trình phát triển này là sự ô nhiễm môi trường. Sự có mặt của các ion kim loại nặng trong các nguồn nước là một trong những nguyên nhân gây ảnh hưởng xấu đến sức khoẻ con người. Do đó, loại bỏ các ion kim loại nặng có trong các nguồn nước là hướng nghiên cứu được nhiều nhà khoa học quan tâm [4, 7-11, 13, 14]. Trong số các phương pháp được dùng để loại bỏ ion kim loại hiện nay (trao đổi ion, đồng kết tủa, hấp phụ...) thì hấp phụ vẫn là một phương pháp được dùng phổ biến nhất do tính ưu việt của nó (tính kinh tế, hiệu quả, thân thiện với môi trường, chất hấp phụ phong phú...). Mặc dù than hoạt tính và các nano oxit kim loại khá hiệu quả trong việc loại bỏ các ion kim loại nhưng giá thành của các vật liệu này tương đối cao. Vì vậy, các chất hấp phụ giá thành rẻ, có nguồn gốc hoàn toàn tự nhiên rất thích hợp đối với các nước đang phát triển. Bài báo này trình bày các kết quả nghiên cứu về sự hấp phụ Fe(III), Cr(VI), Mn(II), Ni(II) trên đá ong tự nhiên và quặng apatit tự nhiên, từ đó đánh giá khả năng hấp phụ các ion kim loại của các vật liệu này. 2. THỰC NGHIỆM 2.1. Hóa chất và thiết bị nghiên cứu Hóa chất: Các dung dịch chuẩn Fe(III), Cr(VI), Mn(II) và Ni(II) 1000 mg/L trong HNO3 1-2% của hãng Merck, Đức. Fe(NO3).9H2O 99%; K2CrO4 99,5%; Mn(NO3)2 50%, d = 1,51 g/mL; Ni(NO3)2.6H2O 99%; NH3 25 - 28%; HgSO4 98,5%; AgNO3 (ống chuẩn); (NH4)2S2O8 99%; 14 NaOH 96%; HNO3 65 ÷ 68%; Dung dịch brom bão hòa; Dimetylglyoxim; Axit sunfosalisilic; 1,5 – diphenylcacbazide; Cồn tuyệt đối. Tất cả hóa chất trên đều có độ tinh khiết PA. Thiết bị và dụng cụ nghiên cứu: Máy lắc Máy lắc HY – 4 Guo Hua Electrial Appliance (Trung Quốc); Máy đo pH 2 số Presisa 900 (Thụy Sĩ); Máy quang phổ hấp thụ phân tử UV 1700 (Shimadzu - Nhật Bản); Tủ sấy Jeio tech (Hàn Quốc); Cân điện tử 4 số Presicsa XT 120A (Thụy Sĩ); Bình định mức, cốc thủy tinh, pipet, bình tam giác, 2.2. Chuẩn bị nguyên liệu Đá ong tự nhiên được lấy tại huyện Thạch Thất – Hà Nội, quặng apatit được lấy tại huyện Cam Đường – Lào Cai. Sau khi thu thập, các vật liệu được rửa bằng nước máy, sau đó được rửa bằng nước cất và sấy khô ở 1000C. Nghiền vật liệu đến các kích thước hạt khác nhau. Bảo quản vật liệu trong lọ polyetylen sạch. 2.3. Quy trình thực nghiệm và các thí nghiệm nghiên cứu 2.3.1. Quy trình thực nghiệm Trong mỗi thí nghiệm hấp phụ: - Thể tích dung dịch ion kim loại: 25 mL với nồng độ xác định. - Lượng chất hấp phụ: 0,1 g - Thí nghiệm được tiến hành ở nhiệt độ phòng (25 ± 20C), sử dụng máy lắc với tốc độ 200 vòng/phút. 2.3.2. Các thí nghiệm nghiên cứu * Khảo sát một số yếu tố ảnh hưởng đến quá trình hấp phụ ion kim loại của vật liệu: + Ảnh hưởng của pH: pH thay đổi từ 1,5 ÷ 3,0 đối với Fe(III), từ 2,0 ÷ 6,0 đối với Cr(VI), từ 2,0 ÷ 7,0 đối với Mn(II) và Ni(II); nồng độ ban đầu của Fe(III), Cr(VI), Mn(II) và Ni(II) tương ứng là: 50,52 mg/L; 51,25 mg/L; 49,86 mg/L; 51,76 mg/L; thời gian hấp phụ: 150 phút. + Ảnh hưởng của thời gian: Sử dụng giá trị pH đã tối ưu; nồng độ ban đầu của Fe(III), Cr(VI), Mn(II) và Ni(II) tương ứng là: 51,23 mg/L; 49,82 mg/L; 50,67 mg/L; 51,93 mg/L; thời gian hấp phụ thay đổi từ 10 ÷ 180 phút. + Ảnh hưởng của kích thước hạt vật liệu: Sử dụng giá trị pH và thời gian đã tối ưu; nồng độ ban đầu của Fe(III), Cr(VI), Mn(II) và Ni(II) tương ứng là: 49,98 mg/L; 51,32 mg/L; 48,32 mg/L; 49,15 mg/L; kích thước hạt vật liệu thay đổi như sau: 0,1 0,2 mm; 0,2 0,6 mm; 0,6 0,8 mm. + Ảnh hưởng của nồng độ ban đầu: sử dụng giá trị pH, thời gian và kích thước hạt vật liệu tối ưu đã xác định ở các thí nghiệm trước; nồng độ ban đầu thay đổi từ 10,57 đến 149,93 mg/L đối với Fe(III); 10,25 đến 148,94 mg/L đối với Cr(VI); 9,48 đến 150,27 mg/L đối với Mn(II); 10,99 đến 105,12 mg/L đối với Ni(II). Các thí nghiệm được tiến hành ở nhiệt độ phòng (25 ± 20C). Hiệu suất hấp phụ được tính theo công thức: .100 C CCH o to % (1) Trong đó: H: hiệu suất hấp phụ (%) Co, Ct: nồng độ ban đầu và nồng độ tại thời điểm t của dung dịch ion kim loại (mg/L). - Dung lượng hấp phụ cực đại được xác định dựa vào phương trình hấp phụ đẳng nhiệt Langmuir dạng tuyến tính: bq 1C q 1 q C max cb max cb (2) Trong đó: q, qmax: dung lượng hấp phụ và dung lượng ... 8,03 m2/g và 5,91 m2/g. Kết quả nghiên cứu cho thấy, diện tích bề mặt riêng của đá ong tự nhiên cao hơn quặng apatit. Kết quả này cũng phù hợp với kết quả nghiên cứu hình thái của vật liệu bằng phương pháp SEM. 3.1.3. Phổ hồng ngoại của đá ong và quặng apatit Phổ hồng ngoại của các vật liệu được trình bày trong hình 2. 4000 4503500 3000 2500 2000 1500 1000 500 101 79 80 82 84 86 88 90 92 94 96 98 100 cm-1 % T 1032.84cm-1 1007.28cm-1 1104.50cm-1 913.33cm-1 539.31cm-1 3429.72cm-1 3695.13cm-1 3619.74cm-1 469.90cm-1 1633.93cm-1 798.97 691.26 a b Hình 2. Phổ hồng ngoại của đá ong (a) và quặng apatit (b) 16 Trên phổ hồng ngoại của đá ong tự nhiên có các cực tiểu sau: cực tiểu ở 1032,36cm-1; 1008,03cm-1 của đá ong tự nhiên đặc trưng cho các liên kết hóa trị Si-O-Si; cực tiểu ở vùng 3700cm-1 đặc trưng cho các nhóm silan Si-O- H; cực tiểu ở 1630,48cm-1 của đá ong tự nhiên đặc trưng cho liên kết biến dạng O-H của H2O kết tinh. Ngoài ra, vân phổ tại 691,26 cm-1 và 539,31 cm-1 có thể gán cho liên kết Fe-O trong đá ong. Trên phổ hồng ngoại của quặng apatit có cực đại hấp thụ mạnh ở 1031cm-1. Cực đại này có thể gán cho liên kết hoá trị P-O-H trong quặng apatit. Cực đại ở 1009 cm-1 của quặng apatit đặc trưng cho liên kết hoá trị Si-O-Si. Cực đại ở 1633cm-1 của quặng apatit đặc trưng cho liên kết biến dạng O-H của nước kết tinh [3]. 3.2. Khảo sát một số yếu tố ảnh hưởng đến quá trình hấp phụ Fe(III), Cr(VI), Mn(II), Ni(II) của các vật liệu 3.2.1. Ảnh hưởng của pH Kết quả khảo sát sự ảnh hưởng của pH đến khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của các vật liệu được trình bày trong hình 3. a b Hình 3. Ảnh hưởng của pH đến khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của đá ong (a) và quặng apatit (b) Các kết quả cho thấy: pH có ảnh hưởng khá lớn tới khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của các vật liệu. Cụ thể: Đối với Fe(III): Khi pH tăng từ 1,5 đến 2,5 thì dung lượng hấp phụ Fe(III) của đá ong tự nhiên và quặng apatit tăng dần. Điều này có thể được giải thích là khi pH có giá trị nhỏ, tương ứng với nồng độ ion H+ cao nên có thể xảy ra sự hấp phụ cạnh tranh giữa ion H+ và cation Fe(III), từ đó làm giảm dung lượng hấp phụ Fe(III) của vật liệu. Khi pH lớn hơn 2,5 thì có thể xảy ra sự kết tủa Fe(OH)3 [1] nên làm giảm khả năng hấp phụ Fe(III) của các vật liệu. Do đó giá trị pH tối ưu cho sự hấp phụ Fe(III) của đá ong tự nhiên và quặng apatit là 2,5. Đối với Cr(VI): Trong toàn miền pH khảo sát, khi giá trị pH tăng thì dung lượng hấp phụ Cr(VI) giảm. Đó là do khi pH càng cao thì nồng độ OH- càng lớn nên xảy ra sự hấp phụ cạnh tranh giữa ion OH- với các anion Cr(VI) và làm giảm khả năng hấp phụ Cr(VI) của các vật liệu. Với pH bằng 2,0 nhỏ hơn giá trị điểm đẳng điện của các vật liệu (pI của đá ong bằng 7,4 [11]; pI của quặng apatit bằng 5,5 [5]) thì bề mặt vật liệu tích điện dương tạo điều kiện thuận lợi cho sự hấp phụ anion. Do đó, giá trị pH tối ưu cho sự hấp phụ Cr(VI) của các vật liệu là 2,0. Đối với Mn(II): Khi pH tăng từ 2,0 đến 6,0 thì dung lượng hấp phụ Mn(II) của các vật liệu tăng dần. Điều này cũng có thể giải thích là khi pH càng nhỏ thì sự hấp phụ cạnh tranh giữa ion H+ và cation Mn(II) càng lớn nên dung lượng hấp phụ Mn(II) của các vật liệu càng giảm. Ở giá trị pH = 6,0, nồng độ ion H+ giảm dần và giá trị pH này có giá trị lớn hơn điểm đẳng điện của quặng apatit nên ở giá trị pH 6,0, bề mặt vật liệu tích điện âm, thuận lợi cho sự hấp phụ các cation. Khi pH = 7,0 có thể xảy ra sự kết tủa Mn(OH)2 nên dung lượng hấp phụ Mn(II) của các vật liệu giảm. Do đó pH = 6,0 là giá trị pH tối ưu cho sự hấp phụ Mn(II) của các vật liệu. 17 Đối với Ni(II): Sự ảnh hưởng của pH đối với sự hấp phụ Ni(II) của các vật liệu được giải thích tương tự như sự hấp phụ Mn(II). Các kết quả khảo sát cho thấy, giá trị pH tối ưu cho sự hấp phụ Ni(II) của đá ong và quặng apatit là 6,0. Như vậy, giá trị pH tối ưu cho sự hấp phụ Fe(III), Cr(VI), Mn(II), Ni(II) trên cả hai vật liệu lần lượt là: pH 2,0; 2,5; 6,0 và 6,0. Điều kiện pH tối ưu này sẽ được sử dụng cho các nghiên cứu tiếp theo. 3.2.2. Ảnh hưởng của thời gian Kết quả nghiên cứu sự ảnh hưởng của thời gian đến dung lượng hấp phụ các ion kim loại của vật liệu được trình bày ở hình 4. a b Hình 4. Ảnh hưởng của thời gian đến khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của đá ong (a) và quặng apatit (b) Các kết quả thực nghiệm cho, thấy dung lượng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của vật liệu hấp phụ tăng khi thời gian tiếp xúc của VLHP với ion kim loại tăng. Trong khoảng thời gian đầu, dung lượng hấp phụ các ion kim loại của các vật liệu tăng nhanh sau đó tăng chậm dần và đạt trạng thái cân bằng. Cụ thể, thời gian đạt cân bằng đối với Ni(II), Fe(III), Cr(VI) và Mn(II) của đá ong tự nhiên lần lượt là 90 phút, 120 phút, 150 phút và 150 phút; của quặng apatit lần lượt là 120 phút, 150 phút, 150 phút và 150 phút. Đây là thông số thời gian chúng tôi sẽ chọn để làm các thí nghiệm tiếp theo. 3.2.3. Ảnh hưởng của kích thước hạt vật liệu Khảo sát sự ảnh hưởng của kích thước hạt vật liệu đến khả năng hấp phụ các ion kim loại, chúng tôi thu được các kết quả trong bảng 1. Bảng 1. Ảnh hưởng của kích thước hạt vật liệu đến khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) Nồng độ ban đầu (mg/L) Kích thước vật liệu d (mm) Đá ong Quặng apatit Ccb (mg/L) q (mg/g) H (%) Ccb (mg/L) q (mg/g) H (%) Fe(III) C0 = 48,98 0,1 0,2 44,34 1,16 9,47 41,98 1,75 14,29 0,2 0,6 45,26 0,93 7,59 42,86 1,53 12,49 0,6 0,8 45,50 0,87 7,10 43,50 1,37 11,18 Cr(VI) C0 = 51,32 0,1 0,2 41,00 2,58 20,11 37,76 3,39 26,42 0,2 0,6 41,96 2,34 18,23 38,84 3,12 24,32 0,6 0,8 43,52 1,95 15,20 39,96 2,84 22,12 Mn(II) C0 = 48,32 0,1 0,2 46,80 0,63 5,11 46,52 0,70 5,68 0,2 0,6 47,40 0,48 3,89 47,28 0,51 4,14 0,6 0,8 48,04 0,32 2,60 47,80 0,38 3,08 Ni(II) C0 = 49,15 0,1 0,2 37,55 2,90 23,60 35,03 3,53 28,73 0,2 0,6 40,31 2,21 17,99 35,63 3,38 27,51 0,6 0,8 41,67 1,87 15,22 37,39 2,94 23,93 18 Kết quả thực nghiệm cho thấy, khi kích thước hạt vật liệu tăng thì dung lượng hấp phụ và hiệu suất hấp phụ của Fe(III), Cr(VI), Mn(II) và Ni(II) giảm. Đó là do khi kích thước hạt vật liệu hấp phụ càng lớn thì diện tích bề mặt riêng càng nhỏ nên sự hấp phụ càng kém. Với kết quả nghiên cứu này, chúng tôi chọn kích thước hạt vật liệu từ 0,1 0,2 mm cho các thí nghiệm tiếp theo. 3.2.4. Ảnh hưởng của nồng độ đầu Tiến hành khảo sát sự ảnh hưởng của nồng độ đầu Fe(III), Cr(VI), Mn(II) và Ni(II) đến khả năng hấp phụ của các vật liệu, chúng tôi thu được kết quả trong bảng 2. Bảng 2. Ảnh hưởng của nồng độ đầu đến khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của vật liệu Ion Đá ong tự nhiên Quặng apatit Co ( mg/L) Ccb (mg/L) q (mg/g) Ccb/q ( mg/L) Co ( mg/L) Ccb (mg/L) q (mg/g) Ccb/q ( mg/L) Fe(III) 10,57 8,09 0,62 13,05 10,62 7,38 0,81 9,11 24,89 21,17 0,93 22,76 25,76 20,52 1,31 15,66 50,32 44,92 1,35 33,27 50,15 43,03 1,78 24,17 75,46 68,78 1,67 41,19 75,17 67,37 1,95 34,55 100,94 93,42 1,88 49,69 99,94 91,02 2,23 40,82 125,86 117,66 2,05 57,40 125,19 115,31 2,47 46,68 149,93 141,09 2,21 63,84 151,03 140,55 2,62 53,65 Cr(VI) 10,25 1,65 2,15 0,77 9,87 3,35 1,63 2,06 25,46 14,66 2,70 5,43 24,93 16,21 2,18 7,44 50,83 37,31 3,38 11,04 50,12 39,88 2,56 15,58 74,91 60,27 3,66 16,47 75,67 64,03 2,91 22,00 100,12 83,56 4,14 20,18 99,82 87,42 3,10 28,20 125,67 108,59 4,27 25,43 125,86 113,06 3,20 35,33 148,94 131,54 4,35 30,24 150,47 137,07 3,35 40,92 9,48 8,84 0,16 55,25 10,58 9,90 0,17 58,24 25,88 24,36 0,38 64,11 25,88 24,36 0,38 64,11 Mn(II) 50,97 48,49 0,62 78,21 49,97 47,21 0,69 68,42 75,06 71,94 0,78 92,23 75,06 71,42 0,91 78,48 101,50 97,82 0,92 106,33 101,50 97,18 1,08 89,98 124,80 120,72 1,02 118,35 124,80 119,88 1,23 97,46 150,27 146,07 1,05 139,11 150,32 145,04 1,32 109,88 10,99 6,07 1,23 4,94 10,65 5,25 1,35 3,89 Ni(II) 23,74 15,14 2,15 7,04 20,33 12,13 2,05 5,92 43,19 31,75 2,86 11,10 41,90 29,22 3,17 9,22 52,50 40,18 3,08 13,05 50,24 36,20 3,51 10,31 63,35 50,27 3,27 15,37 63,62 47,94 3,92 12,23 82,34 67,94 3,60 18,87 80,30 64,10 4,05 15,83 105,12 90,40 3,68 24,57 104,28 86,40 4,47 19,32 Từ các kết quả thu được, chúng tôi tiến hành xây dựng phương trình Langmuir và phương trình Freundlich. Kết quả khảo sát là một trong những cơ sở ban đầu cho phép nhận định cơ chế hấp phụ các ion Fe(III), Cr(VI), Mn(II) và Ni(II) trên đá ong tự nhiên và quặng apatit. Các kết quả được trình bày trong các bảng 3, 4 và các hình 5, 6 dưới đây. 19 Bảng 3. Các thông số hấp phụ theo mô hình Langmuir Vật liệu Đá ong tự nhiên Quặng Apatit Ion qmax (mg/g) Hằng số Langmuir b (L/g) R2 qmax (mg/g) Hằng số Langmuir b (L/g) R2 Fe(III) 2,72 0,026 0,993 3,02 0,036 0,992 Cr(VI) 4,57 0,113 0,992 3,50 0,103 0,994 Mn(II) 1,68 0,012 0,996 2,65 0,007 0,991 Ni(II) 4,34 0,063 0,999 5,32 0,055 0,996 a b Hình 5. Sự phụ thuộc Ccb/q vào Ccb của Fe(III), Cr(VI), Mn(II) và Ni(II) đối với đá ong (a) và quặng apatit (b) a b Hình 6. Sự phụ thuộc Ln(q) vào Ln(Ccb) của Fe(III), Cr(VI), Mn(II) và Ni(II) đối với đá ong (a) và quặng apatit (b) Bảng 4. Các thông số hấp phụ theo mô hình Freundlich Ion Đá ong tự nhiên Quặng apatit Tham số 1/n Hằng số k (mg/g)(mg/L)1/n R2 Tham số 1/n Hằng số k (mg/g)(mg/L)1/n R2 Fe(III) 0,452 0,24 0,998 0,390 0,39 0,992 Cr(VI) 0,169 1,88 0,964 0,195 1,27 0,997 Mn(II) 0,678 0,04 0,983 0,771 0,03 0,989 Ni(II) 0,408 0,65 0,960 0,437 0,69 0,982 20 Nhận xét: Các kết quả nghiên cứu cho phép nhận định rằng, sự hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) trên các vật liệu hấp phụ tuân theo mô hình đẳng nhiệt Langmuir (R2 > 0,99) và Freundlich (R2 > 0,96). Như vậy, bước đầu có thể giả thiết rằng sự hấp phụ các ion Fe(III), Cr(VI), Mn(II), Ni(II) trên các vật liệu xảy ra theo cơ chế hấp phụ vật lý và hấp phụ hoá học. 3.3. Đánh giá khả năng hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) của các vật liệu Kết quả nghiên cứu về mô hình hấp phụ đẳng nhiệt Langmuir cho thấy: Dung lượng hấp phụ cực đại của các ion trên đá ong tăng theo thứ tự: Mn(II), Fe(III), Ni(II), Cr(VI). Kết quả này có thể giải thích dựa vào giá trị điểm đẳng điện của đá ong, giá trị pH tối ưu khi tiến hành hấp phụ các ion trên đá ong, cũng như bán kính ion hiđrat hoá của các ion kim loại [6]. Kết quả nghiên cứu cũng chỉ ra rằng, dung lượng hấp phụ của các ion Fe(III), Mn(II), Ni(II) trên quặng apatit lớn hơn đá ong tự nhiên và tăng theo thứ tự Mn(II), Fe(III), Ni(II). Dung lượng hấp phụ Cr(VI) của đá ong tự nhiên cao hơn quặng apatit. Điều này có thể giải thích là do quặng apatit có chứa tâm hấp phụ dạng PO43-, HPO42- nên thuận lợi cho sự hấp phụ các cation hơn các anion. Tuy diện tích bề mặt riêng của đá ong lớn hơn quặng apatit nhưng dung lượng hấp phụ của hầu hết các ion khảo sát trên đá ong lại nhỏ hơn trên quặng apatit. Kết hợp với các kết quả nghiên cứu mô hình đẳng nhiệt hấp phụ; kết quả nghiên cứu về phổ hồng ngoại, điểm đẳng điện, diện tích bề mặt riêng của các vật liệu cho thấy, sự hấp phụ các ion Fe(III), Cr(VI), Mn(II) và Ni(II) trên các vật liệu tuân theo cả hai cơ chế hấp phụ vật lý và hấp phụ hoá học. So với một số vật liệu có nguồn gốc tự nhiên khác, nhận thấy dung lượng hấp phụ Ni(II) của đá ong và quặng apatit cao hơn một số zeolite tự nhiên là clinoptilolite và charbazite philipsite [2]; dung lượng hấp phụ Cr(VI) của đá ong và quặng apatit lớn hơn của bentonite tự nhiên [10]. Đối với mô hình đẳng nhiệt Freundlich, các giá trị 1/n của quá trình hấp phụ Fe(III), Cr(VI), Ni(II) trên đá ong tự nhiên và quặng apatit đều nhỏ hơn 0,5 chứng tỏ sự hấp phụ Fe(III), Cr(VI), Ni(II) trên các vật liệu là dễ dàng. Do giá trị 1/n lớn hơn 0,5 nên quá trình hấp phụ Mn(II) trên các vật liệu là khó khăn [12]. 4. KẾT LUẬN 1. Đã nghiên cứu các đặc trưng hóa lí của đá ong tự nhiên và quặng apatit tự nhiên bằng các phương pháp SEM, BET, IR. 2. Đã nghiên cứu các điều kiện tối ưu cho phép hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) trên các vật liệu. Cụ thể: pH tốt nhất cho sự hấp phụ Cr(VI), Fe(III), Mn(II) và Ni(II) trên các vật liệu lần lượt là 2,0; 2,5; 6,0 và 6,0. Thời gian đạt cân bằng hấp phụ đối với Ni(II), Fe(III), Cr(VI) và Mn(II) của đá ong tự nhiên lần lượt là 90 phút, 120 phút, 150 phút và 150 phút; của quặng apatit lần lượt là 120 phút, 150 phút, 150 phút và 150 phút. Kích thước hạt vật liệu từ 0,1 0,2 mm. 3. Sự hấp phụ Fe(III), Cr(VI), Mn(II) và Ni(II) trên các vật liệu tuân theo mô hình đẳng nhiệt Langmuir và Freundlich. Dung lượng hấp phụ Fe(III), Cr(VI), Mn(II), Ni(II) cực đại trên đá ong tự nhiên lần lượt là: 2,72 mg/g; 4,57 mg/g; 1,68 mg/g và 4,34 mg/g. Dung lượng hấp phụ Fe(III), Cr(VI), Mn(II), Ni(II) cực đại trên quặng apatit lần lượt là: 3,02 mg/g; 3,50 mg/g; 2,65mg/g và 5,32 mg/g. Sự hấp phụ Fe(III), Cr(VI), Ni(II) trên đá ong tự nhiên và quặng apatit là thuận lợi trong khi đó sự hấp phụ Mn(II) trên các vật liệu là khó khăn. TÀI LIỆU THAM KHẢO 1. Nguyễn Tinh Dung (2009), Hóa học phân tích, Phần II, Các phản ứng trong dung dịch, NXB ĐHSP. 2. Đặng Xuân Tập (2002), Nghiên cứu khả năng hấp phụ của một số khoáng tự nhiên, tổng hợp và ứng dụng của chúng, Luận án Tiến sỹ Hóa học, ĐH Bách Khoa Hà Nội. 3. Nguyễn Đình Triệu (2006), Các phương pháp vật lý ứng dụng trong hóa học, NXB ĐHQG Hà Nội. 4. Ngô Thị Mai Việt, Nguyễn Thị Hằng, Phạm Thị Quỳnh, Nghiêm Thị Hương, Ngô Thành Trung (2019), Tách loại amoni, Mn(II) trong nước sử dụng cột hấp phụ đá ong biến 21
File đính kèm:
 nghien_cuu_kha_nang_hap_phu_mot_so_ion_kim_loai_nang_tren_da.pdf
nghien_cuu_kha_nang_hap_phu_mot_so_ion_kim_loai_nang_tren_da.pdf

