Nghiên cứu bào chế viên nén Acid alpha lipoic 300 mg
(i) Bước đầu đánh giá được ảnh hưởng
của một số yếu tố thuộc công thức bào chế đến khả
năng khắc phục hiện tượng dính chày cối trong quá
trình dập viên và độ hòa tan (ĐHT) của viên nén acid
alpha lipoic (ALA) 300 mg; (ii) Bào chế được viên nén
ALA 300 mg đạt tiêu chuẩn ĐHT theo Dược điển Mỹ
(USP) 41 ở quy mô phòng thí nghiệm. Phương pháp
nghiên cứu: Bào chế viên nén ALA bằng phương
pháp tạo hạt ướt và đánh giá ảnh hưởng của một số
yếu tố bằng thực nghiệm. Kết quả: Công thức viên
nén ALA 300 mg tìm được gồm: ALA: 300 mg, Avicel
PH-102: 120 mg, natri stearyl fumarat (NSF): 19,1
mg, Aerosil 200: 19,1 mg, talc: 9,6 mg, dinatri edetat
(EDTA): 1mg, hydroxypropyl cellulose (HPC): 12,2
mg, natri croscarmellose (NCC): 25 mg, menthol: 12
mg, poloxamer: 6 mg, calci carbonat: 20 mg, calci
hydrophosphat (DCP): 160,7 mg, ethanol 30% điều
chỉnh đến pH 8,0: 300 mg. Viên không dính chày cối
trong quá trình dập viên ở quy mô 1000 viên/mẻ và
đạt tiêu chuẩn ĐHT theo USP 41

Trang 1

Trang 2

Trang 3
Trang 4
Trang 5
Tóm tắt nội dung tài liệu: Nghiên cứu bào chế viên nén Acid alpha lipoic 300 mg

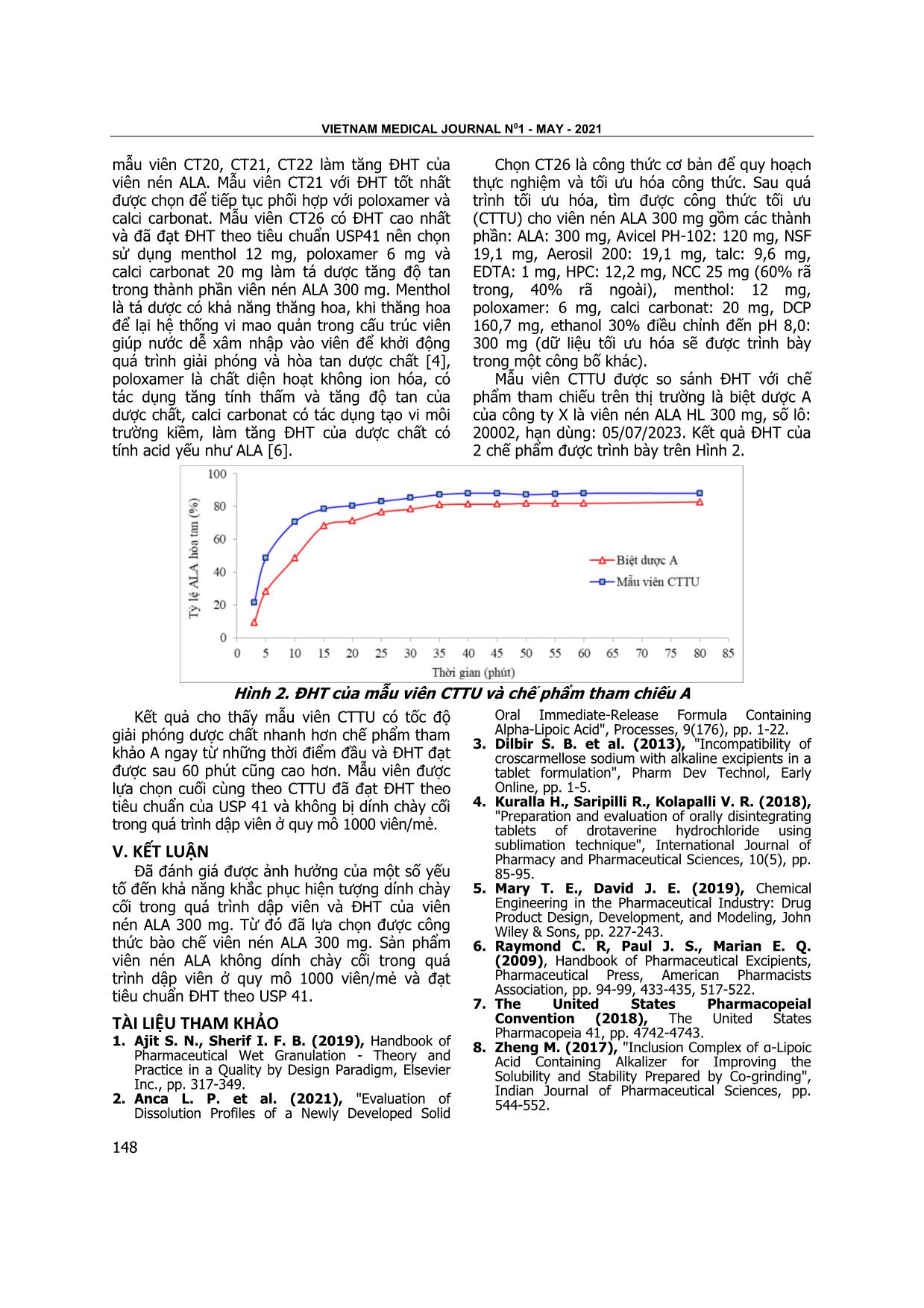
vietnam medical journal n01 - MAY - 2021 144 5. Võ Trương Như Ngọc, Trương Mạnh Dũng, Tống Minh Sơn, Trịnh Thị Thái Hà (2014). Nhận xét chuẩn tân cổ điển ở một nhóm sinh viên 18-25 có khuôn mặt trên ảnh kỹ thuật số chuẩn hóa. Tạp Chí Y Học Thực Hành, 3, 24-27. 6. Trần Tuấn Anh, Võ Trương Như Ngọc (2013). Đặc điểm hình thái khuôn mặt ở một nhóm người Việt độ tuổi từ 18-25 tại trường Cao Đẳng Y tế Bình Dương. Tạp Chí Y Học Việt Nam, 2, 66–75. 7. Võ Trương Như Ngọc, Trương Mạnh Dũng, Tống Minh Sơn, Trịnh Thị Thái Hà (2014), Nhận xét chuẩn tân cổ điển ở một nhóm sinh viên 18-25 tuổi có khuôn mặt hài hòa trên ảnh kỹ thuật số chuẩn hóa, Tạp chí Y Học Thực Hành, số 2 (906), trang 131-136. 8. Võ Trương Như Ngọc, Nguyễn Đức Nghĩa (2014), Mối tương quan giữa các kích thước khuôn mặt trên ảnh chuẩn hóa ở một nhóm học sinh PTTH- Trường Chu Văn An Hà Nội năm 2012, Tạp chí Y Học Thực Hành, số 2 (906), trang 140-144. NGHIÊN CỨU BÀO CHẾ VIÊN NÉN ACID ALPHA LIPOIC 300 MG Trần Văn Vinh1, Nguyễn Văn Giang1, Phạm Văn Hùng1 Đàm Thanh Xuân1, Nguyễn Thị Thanh Duyên1 TÓM TẮT35 Mục tiêu: (i) Bước đầu đánh giá được ảnh hưởng của một số yếu tố thuộc công thức bào chế đến khả năng khắc phục hiện tượng dính chày cối trong quá trình dập viên và độ hòa tan (ĐHT) của viên nén acid alpha lipoic (ALA) 300 mg; (ii) Bào chế được viên nén ALA 300 mg đạt tiêu chuẩn ĐHT theo Dược điển Mỹ (USP) 41 ở quy mô phòng thí nghiệm. Phương pháp nghiên cứu: Bào chế viên nén ALA bằng phương pháp tạo hạt ướt và đánh giá ảnh hưởng của một số yếu tố bằng thực nghiệm. Kết quả: Công thức viên nén ALA 300 mg tìm được gồm: ALA: 300 mg, Avicel PH-102: 120 mg, natri stearyl fumarat (NSF): 19,1 mg, Aerosil 200: 19,1 mg, talc: 9,6 mg, dinatri edetat (EDTA): 1mg, hydroxypropyl cellulose (HPC): 12,2 mg, natri croscarmellose (NCC): 25 mg, menthol: 12 mg, poloxamer: 6 mg, calci carbonat: 20 mg, calci hydrophosphat (DCP): 160,7 mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg. Viên không dính chày cối trong quá trình dập viên ở quy mô 1000 viên/mẻ và đạt tiêu chuẩn ĐHT theo USP 41. Từ khóa: Acid alpha lipoic (ALA), độ hòa tan (ĐHT), dính chày cối, viên nén. SUMMARY FORMULATION OF ALPHA LIPOIC ACID TABLET 300 MG Objectives: (i) Initially evaluating the effects of some formula factors on alpha lipoic acid (ALA) tablets’ sticking phenomenon during compaction process and tablets’ dissolution; (ii) Preparing 300 mg ALA tablets meeting the USP 41 requirement for dissolution test on a laboratory scale. Method: Tablets were prepared by wet-granulation method, evaluate the effects of some factors by experiments. Result: The selected fomula of ALA tablet contained: ALA: 300 mg, Avicel PH-102: 120 mg, sodium stearyl 1Trường Đại học Dược Hà Nội Chịu trách nhiệm chính: Nguyễn Thị Thanh Duyên Email: duyenntt@hup.edu.vn Ngày nhận bài: 2.3.2021 Ngày phản biện khoa học: 22.4.2021 Ngày duyệt bài: 29.4.2021 fumarate (NSF): 19,1 mg, Aerosil 200: 19,1 mg, talcum: 9,6 mg, disodium edetate (EDTA): 1 mg, hydroxypropyl cellulose (HPC): 12,2 mg, sodium croscarmellose (NCC): 25 mg, menthol: 12 mg, poloxamer: 6 mg, calcium carbonate: 20 mg, calcium hydrogen phosphate (DCP): 160,7 mg, ethanol 30% to pH 8,0: 300mg. The selected formula were successfully prepared on a scale of 1000 tablets without punch sticking and met the USP 41 requirement for dissolution test. Keywords: Acid alpha lipoic (ALA), dissolution, punch sticking, tablet. I. ĐẶT VẤN ĐỀ Acid alpha lipoic (ALA) là dược chất có tác dụng chống oxy hóa, thường được chỉ định để điều trị các tổn thương gây ra bởi quá trình oxy hóa và tái tạo các chất chống oxy hóa nội sinh [2]. Tuy nhiên, việc sản xuất và bảo quản dạng thuốc viên nén chứa ALA gặp nhiều khó khăn do dược chất có nhiệt độ nóng chảy thấp (ở 60oC), ít tan trong nước, kém ổn định với nhiệt và ánh sáng, viên nén dễ bị dính chày trong quá trình dập viên, khả năng tự polyme hóa của ALA còn có thể làm cho viên nén ALA giảm hàm lượng (HL) và ĐHT sau một thời gian sản xuất [2], [8]. Do vậy, nghiên cứu này được thực hiện với các mục tiêu: (i) Bước đầu đánh giá được ảnh hưởng của một số yếu tố thuộc công thức bào chế đến khả năng khắc phục hiện tượng dính chày cối trong quá trình dập viên và ĐHT của viên; (ii) Bào chế được viên nén ALA 300 mg đạt tiêu chuẩn ĐHT theo USP 41 ở quy mô phòng thí nghiệm. II. NGUYÊN LIỆU VÀ PHƯƠNG PHÁP 2.1. Nguyên liệu Dược chất: ALA (Trung Quốc - TQ) và một số tá dược khác như: tinh bột sắn (TQ), Avicel PH- 102 (Đài Loan), DCP (TQ), hydroxypropyl methylcellulose (HPMC) E5 (Singapore), HPC (Singapore), natri starch glycolat (NSG) (TQ), TẠP CHÍ Y häc viÖt nam tẬP 502 - th¸ng 5 - sè 1 - 2021 145 NCC (TQ), crospovidon (Singapore), magnesi stearat (TQ), talc (TQ), Aerosil 200 (TQ), polyethylen glycol (PEG) 6000 (TQ), NSF (TQ), EDTA (TQ), menthol (TQ), poloxamer (Mỹ) 2.2. Thiết bị. Máy nhào Caleva mini mixer (Anh), tủ sấy Memmert (Đức), máy dập viên quay tròn Shaki LP2 (TQ), máy thử ĐHT Erweka DT 600 (Đức), hệ thống sắc ký lỏng hiệu năng cao (HPLC) Shimadzu (Nhật Bản) và một số thiết bị, dụng cụ thí nghiệm khác. 2.3. Phương pháp nghiên cứu 2.3.1. Phương pháp bào chế. Viên nén ALA 300 mg được bào chế bằng phương pháp tạo hạt ướt, công thức cơ bản mỗi viên gồm: ALA 300 mg, tá dược độn, tá dược dính, tá dược rã, tá dược trơn, tá dược tăng ĐHT, tá dược tăng độ ổn định. Các giai đoạn bào chế: Rây ALA và các tá dược trơn qua rây số 125, các tá dược còn lại qua rây số 250. Cân các thành phần theo công thức. Trộn hỗn hợp bột kép gồm ALA và các tá dược độn, rã trong. Pha dung dịch tá dược dính lỏng gồm tá dược dính, chất điều chỉnh pH, chất tăng độ ổn định, chất tăng ĐHT trong dung môi. Nhào ẩm hỗn hợp bột kép với dung dịch tá dược dính. Xát hạt qua rây số 1000. Sấy hạt ở 40ºC đến khi độ ẩm của hạt đạt 1 ... 75 vòng/phút. Định lượng ALA trong môi trường hòa tan bằng phương pháp HPLC với điều kiện tương tự phần “Định lượng ALA trong các mẫu nghiên cứu”. Yêu cầu: không ít hơn 70% ALA hòa tan sau 60 phút [7]. Ngoài ra, viên nén ALA còn được đánh giá các chỉ tiêu: Tính chất, độ cứng. III. KẾT QUẢ NGHIÊN CỨU VÀ BÀN LUẬN Từ một số nghiên cứu tiền công thức trước đó và qua tham khảo tài liệu, công thức cơ bản của viên nén ALA được chọn gồm: ALA: 300 mg, Avicel PH-102: 120 mg, MgS: 15 mg, Aerosil 200: 20 mg, EDTA: 1 mg, dung môi pha tá dược dính là nước tinh khiết và ethanol ở các tỷ lệ khác nhau được điều chỉnh đến pH 8,0, tinh bột sắn vừa đủ 680 mg. 3.1. Ảnh hưởng của tá dược dính Bào chế các mẫu viên nén ALA theo công thức cơ bản, thay đổi loại tá dược dính. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên ALA được trình bày ở Bảng 1 và Hình 1. Bảng 1. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA sử dụng loại tá dược dính khác nhau Công thức Tá dược dính cho 1 viên Dung môi pha tá dược dính cho 1 viên Hình thức ĐHT (TB±SD, %, n=3) 1 HPMC E5: 15 mg Ethanol 96%: 300 mg Cốm trơn chảy kém, viên rỗ mặt do dính chày 9,67 ± 0,23 2 HPMC E5: 15 mg Nước tinh khiết: 300 mg Hạt chắc, trơn chảy tốt, viên nhẵn 52,23 ± 0,00 3 HPMC E5: 15 mg Ethanol 30%: 300 mg 53,57 ± 0,26 4 HPC: 15 mg 55,80 ± 0,25 5 PEG 6000: 30 mg Cốm trơn chảy kém, viên không đạt độ cứng 62,20 ± 0,09 Mẫu viên CT1 sử dụng tá dược dính là HPMC E5 5% trong ethanol 96%, cốm thu được không chắc, dễ vỡ, tạo nhiều bột mịn, có hiện tượng dính chày trong quá trình dập viên (Hình 1). Mẫu viên CT2 sử dụng tá dược dính là HPMC E5 5% trong nước, cốm tạo ra chắc, viên không bị dính chày. Mẫu viên CT3 sử dụng HPMC E5 5% trong ethanol 30% làm tá dược dính, cốm tạo ra chắc, bề mặt viên nhẵn, viên có ĐHT tốt hơn mẫu viên CT2. Trong ethanol 96%, HPMC E5 không hòa tan hoàn toàn mà chỉ tồn tại ở trạng thái phân tán trong môi trường lỏng nên quá trình tạo liên kết giữa các tiểu phân chưa hoàn thiện, vì vậy hạt CT1 bở, dễ vỡ, làm tăng diện tích tiếp xúc của dược chất với bề mặt chày, dẫn tới dính chày. Mẫu viên CT2 sử dụng nước làm dung môi vietnam medical journal n01 - MAY - 2021 146 pha tá dược dính, HPMC E5 trương nở và hòa tan hoàn toàn, tạo dung dịch polyme có độ nhớt cao hơn, đóng vai trò cầu nối lỏng liên kết các tiểu phân tốt và triệt để hơn, kích thước hạt tạo ra đều, gần cầu, diện tích tiếp xúc với bề mặt chày thấp hơn, viên không dính chày khi dập. Khi sử dụng ethanol 30%, lượng nước trong dung môi đủ để HPMC E5 trương nở và hòa tan, do đó chất lượng của hạt và viên vẫn đạt tương tự CT2, đồng thời một phần dược chất được hòa tan trong ethanol, phần dược chất này khi được làm khô có thể tồn tại ở trạng thái vô định hình hoặc trạng thái tinh thể có kích thước tiểu phân nhỏ hơn tinh thể nguyên liệu ban đầu, giúp tăng tốc độ hòa tan dược chất, vì vậy mẫu viên CT3 có ĐHT tốt hơn mẫu viên CT2, do đó chọn ethanol 30% làm dung môi pha tá dược dính để nghiên cứu tiếp. Mẫu viên CT5 dùng PEG 6000 làm tá dược dính, viên bị dính chày. PEG 6000 có nhiệt độ nóng chảy thấp (khoảng 55-63ºC), ma sát trong quá trình dập viên có thể khiến PEG 6000 chảy lỏng, làm cho hiện tượng dính chày nghiêm trọng hơn [6]. CT4 dùng HPC làm tá dược dính, cốm trơn chảy tốt, bề mặt viên nhẵn (Hình 1), viên có ĐHT tốt hơn so với dùng tá dược dính HPMC E5, do đó lựa chọn HPC 5% trong ethanol 30% làm tá dược dính. So với HPMC E5, HPC là tá dược dính mạnh, có thể tạo liên kết tốt giữa các tiểu phân rắn, hạt tạo ra chắc và đều hơn, làm giảm diện tích tiếp xúc của dược chất với bề mặt chày, giảm dính chày trong quá trình dập viên, thích hợp với các dược chất chiếm tỷ lệ lớn trong viên và chịu nén kém như ALA trong nghiên cứu này [1]. Hình 1. Hình ảnh bề mặt mẫu viên CT1 (trái) và CT4 (phải) 3.2. Ảnh hưởng của tá dược độn. Bào chế các mẫu viên nén ALA với loại tá dược độn khác nhau. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA được trình bày ở Bảng 2. Bảng 2. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA sử dụng loại tá dược độn khác nhau Công thức Tá dược độn Hình thức ĐHT (TB±SD, %, n=3) 4 Tinh bột Hạt chắc, trơn chảy tốt, viên nhẵn, đẹp 55,80 ± 0,25 6 DCP 61,49 ± 0,73 7 Avicel PH-102 Viên rỗ mặt 30,88 ± 0,50 Ghi chú: Thành phần cố định mỗi viên: ALA: 300 mg, Avicel PH-102: 120mg, MgS: 15mg, Aerosil 200: 20mg, EDTA: 1mg, HPC: 15mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg, tá dược độn vừa đủ 680 mg. Mẫu viên CT4 và CT6 sử dụng tá dược độn lần lượt là tinh bột và DCP, cốm tạo thành chắc, trơn chảy tốt, bề mặt viên nhẵn, không dính chày. DCP là tá dược có tính biến dạng gãy vỡ khi chịu lực nén, sự gãy vỡ của các tiểu phân DCP làm tăng diện tích bề mặt của tá dược này, tăng khả năng che phủ tiểu phân dược chất, giảm tính kết dính của dược chất với bề mặt chày, tăng lực liên kết liên tiểu phân, tăng sức bền cho viên. Avicel PH-102 lại có tính biến dạng dẻo khi chịu lực nén, có thể vì đó mà mẫu viên CT7 vẫn bị dính chày [5]. Mẫu viên CT6 ngoài khả năng chống dính tốt còn cho ĐHT cao nhất, có thể do tính base của DCP đã tạo vi môi trường pH thuận lợi cho sự hòa tan của ALA [6], do đó DCP được chọn làm tá dược độn để nghiên cứu tiếp. 3.3. Ảnh hưởng của tá dược trơn. Bào chế các mẫu viên ALA với các loại tá dược trơn khác nhau. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên được trình bày ở Bảng 3. Bảng 3. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA sử dụng loại tá dược trơn khác nhau Công thức Tá dược trơn cho 1 viên Hình thức ĐHT (TB±SD, %, n=3) 6 MgS: 15 mg, A: 20 mg Bề mặt viên nhẵn, chắc 61,49 ± 0,73 8 MgS: 15 mg, NLS: 20 mg Bề mặt viên rỗ 67,57 ± 0,57 9 MgS: 10 mg, A: 10 mg, NLS: 15 mg 68,30 ± 2,62 10 NSF: 15, A: 20 mg Bề mặt viên nhẵn, chắc 62,66 ± 2,40 11 NSF: 14 mg, A: 14 mg, talc: 7mg 64,08 ± 0,50 12 NSF: 20 mg, A: 10 mg, talc: 5 mg 62,96 ± 0,40 TẠP CHÍ Y häc viÖt nam tẬP 502 - th¸ng 5 - sè 1 - 2021 147 Ghi chú: A: Aerosil 200. Thành phần cố định mỗi viên: ALA: 300 mg, Avicel PH-102: 120 mg, EDTA: 1 mg, HPC: 15 mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg, DCP vừa đủ 680 mg. Kết quả cho thấy các mẫu viên có sử dụng NLS làm tá dược trơn (CT8, CT9) cho ĐHT cao hơn các công thức còn lại do NLS là một chất diện hoạt, có tác dụng gây thấm bề mặt tiểu phân dược chất sơ nước và tăng độ tan của dược chất, tuy nhiên các viên dập về sau có xu hướng dính chày. Các mẫu viên còn lại (CT6, CT10, CT11, CT12) có khả năng chống dính tốt hơn, bề mặt viên nhẵn. Mẫu viên CT11 cho ĐHT tốt nhất nên được chọn để tiếp tục nghiên cứu. 3.4. Ảnh hưởng của tá dược siêu rã Bào chế các mẫu viên nén ALA kết hợp thêm với các loại tá dược siêu rã (TDSR) khác nhau, kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên được trình bày ở Bảng 4. Bảng 4. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA sử dụng loại tá dược siêu rã khác nhau Công thức Tá dược siêu rã cho 1 viên Hình thức ĐHT (TB±SD, %, n=3) 11 Không dùng TDSR Bề mặt viên nhẵn, viên không dính chày trong suốt quá trình dập 64,08 ± 0,50 13 NSG (20 mg RT, 20 mg RN) 66,31 ± 0,96 14 Crosspovidon (20 mg RT, 20 mg RN) 67,30 ± 0,90 15 NCC (20 mg RT, 20 mg RN) 69,33 ± 0,85 16 NCC (16 mg RT, 24 mg RN) 69,72 ± 0,79 17 NCC (24 mg RT, 16 mg RN) 71,30 ± 0,25 18 NCC (12 mg RT, 28 mg RN) 69,04 ± 0,10 19 NCC (28 mg RT, 12 mg RN) 68,19 ± 0,13 Ghi chú: RT: rã trong, RN: rã ngoài. Thành phần cố định mỗi viên: ALA: 300 mg, Avicel PH- 102: 120 mg, NSF 14mg, Aerosil 200: 14 mg, talc: 7 mg, EDTA: 1 mg, HPC: 15 mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg, DCP vừa đủ 680 mg. Các mẫu viên CT13, CT14, CT15 sử dụng 3 loại TDSR khác nhau với cùng tỷ lệ phối hợp rã trong:rã ngoài (1:1), mẫu viên CT15 sử dụng NCC cho ĐHT cao nhất. Khi tiếp tục thay đổi tỷ lệ phối hợp rã trong:rã ngoài (mẫu viên CT16 đến CT19), mẫu viên CT17 với tỷ lệ rã trong:rã ngoài (24:16) cho ĐHT cao nhất. Điều này có thể do việc phối hợp cả tá dược rã trong và rã ngoài giúp đẩy nhanh cả hai quá trình rã từ viên thành hạt và từ hạt thành bột nên có hiệu quả tốt nhất trong việc tăng ĐHT. CT17 được chọn để khảo sát tiếp. Giá trị pH 8,0 của tá dược dính vừa phù hợp với độ tan, độ ổn định của ALA (như kết quả nghiên cứu tiền công thức), vừa phù hợp với độ ổn định của TDSR được chọn. Trong môi trường pH > 9,0, NCC sẽ bị thủy phân các liên kết chéo giữa các chuỗi polyme, tạo thành dạng polyme tan trong nước, lúc này mất khả năng rã mà trái lại còn hình thành lớp hàng rào gel nhớt làm giảm ĐHT của viên [3]. 3.5. Ảnh hưởng của tá dược làm tăng ĐHT. Bào chế các mẫu viên nén ALA kết hợp thêm với các loại tá dược tăng ĐHT khác nhau. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên được trình bày ở Bảng 5. Bảng 5. Kết quả đánh giá một số chỉ tiêu chất lượng của các mẫu viên nén ALA sử dụng loại tá dược tăng ĐHT khác nhau Công thức Tá dược tăng ĐHT cho 1 viên Hình thức Độ rã (TB±SD, phút, n=3) ĐHT (TB±SD, %, n=3) 17 Không dùng Bề mặt viên nhẵn, viên không dính chày 6,30 ± 0,40 71,30 ± 0,25 20 M: 6 mg 7,37 ± 0,38 76,03 ± 0,10 21 M: 12 mg 5,20 ± 0,10 81,26 ± 0,56 22 M: 18 mg 4,20 ± 0,12 80,47 ± 0,47 23 M: 12 mg, P: 3 mg 5,47 ± 0,25 80,19 ± 0,91 24 M: 12 mg, P: 6 mg 4,30 ± 0,56 82,55 ± 0,53 25 M: 12 mg, P: 12 mg 6,00 ± 0,36 82,01 ± 0,20 26 M: 12 mg, P: 6 mg, C: 20 mg 3,80 ± 0,20 85,16 ± 0,48 Ghi chú: M: menthol, P: poloxamer, C: calci carbonat. Thành phần cố định mỗi viên: ALA: 300 mg, Avicel PH-102: 120 mg, NSF 14 mg, Aerosil 200: 14 mg, talc: 7 mg, EDTA: 1 mg, HPC: 15 mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg, NCC: 40 mg (24 mg rã trong, 16 mg rã ngoài), DCP vừa đủ 680mg. Kết quả cho thấy, việc sử dụng menthol ở các vietnam medical journal n01 - MAY - 2021 148 mẫu viên CT20, CT21, CT22 làm tăng ĐHT của viên nén ALA. Mẫu viên CT21 với ĐHT tốt nhất được chọn để tiếp tục phối hợp với poloxamer và calci carbonat. Mẫu viên CT26 có ĐHT cao nhất và đã đạt ĐHT theo tiêu chuẩn USP41 nên chọn sử dụng menthol 12 mg, poloxamer 6 mg và calci carbonat 20 mg làm tá dược tăng độ tan trong thành phần viên nén ALA 300 mg. Menthol là tá dược có khả năng thăng hoa, khi thăng hoa để lại hệ thống vi mao quản trong cấu trúc viên giúp nước dễ xâm nhập vào viên để khởi động quá trình giải phóng và hòa tan dược chất [4], poloxamer là chất diện hoạt không ion hóa, có tác dụng tăng tính thấm và tăng độ tan của dược chất, calci carbonat có tác dụng tạo vi môi trường kiềm, làm tăng ĐHT của dược chất có tính acid yếu như ALA [6]. Chọn CT26 là công thức cơ bản để quy hoạch thực nghiệm và tối ưu hóa công thức. Sau quá trình tối ưu hóa, tìm được công thức tối ưu (CTTU) cho viên nén ALA 300 mg gồm các thành phần: ALA: 300 mg, Avicel PH-102: 120 mg, NSF 19,1 mg, Aerosil 200: 19,1 mg, talc: 9,6 mg, EDTA: 1 mg, HPC: 12,2 mg, NCC 25 mg (60% rã trong, 40% rã ngoài), menthol: 12 mg, poloxamer: 6 mg, calci carbonat: 20 mg, DCP 160,7 mg, ethanol 30% điều chỉnh đến pH 8,0: 300 mg (dữ liệu tối ưu hóa sẽ được trình bày trong một công bố khác). Mẫu viên CTTU được so sánh ĐHT với chế phẩm tham chiếu trên thị trường là biệt dược A của công ty X là viên nén ALA HL 300 mg, số lô: 20002, hạn dùng: 05/07/2023. Kết quả ĐHT của 2 chế phẩm được trình bày trên Hình 2. Hình 2. ĐHT của mẫu viên CTTU và chế phẩm tham chiếu A Kết quả cho thấy mẫu viên CTTU có tốc độ giải phóng dược chất nhanh hơn chế phẩm tham khảo A ngay từ những thời điểm đầu và ĐHT đạt được sau 60 phút cũng cao hơn. Mẫu viên được lựa chọn cuối cùng theo CTTU đã đạt ĐHT theo tiêu chuẩn của USP 41 và không bị dính chày cối trong quá trình dập viên ở quy mô 1000 viên/mẻ. V. KẾT LUẬN Đã đánh giá được ảnh hưởng của một số yếu tố đến khả năng khắc phục hiện tượng dính chày cối trong quá trình dập viên và ĐHT của viên nén ALA 300 mg. Từ đó đã lựa chọn được công thức bào chế viên nén ALA 300 mg. Sản phẩm viên nén ALA không dính chày cối trong quá trình dập viên ở quy mô 1000 viên/mẻ và đạt tiêu chuẩn ĐHT theo USP 41. TÀI LIỆU THAM KHẢO 1. Ajit S. N., Sherif I. F. B. (2019), Handbook of Pharmaceutical Wet Granulation - Theory and Practice in a Quality by Design Paradigm, Elsevier Inc., pp. 317-349. 2. Anca L. P. et al. (2021), "Evaluation of Dissolution Profiles of a Newly Developed Solid Oral Immediate-Release Formula Containing Alpha-Lipoic Acid", Processes, 9(176), pp. 1-22. 3. Dilbir S. B. et al. (2013), "Incompatibility of croscarmellose sodium with alkaline excipients in a tablet formulation", Pharm Dev Technol, Early Online, pp. 1-5. 4. Kuralla H., Saripilli R., Kolapalli V. R. (2018), "Preparation and evaluation of orally disintegrating tablets of drotaverine hydrochloride using sublimation technique", International Journal of Pharmacy and Pharmaceutical Sciences, 10(5), pp. 85-95. 5. Mary T. E., David J. E. (2019), Chemical Engineering in the Pharmaceutical Industry: Drug Product Design, Development, and Modeling, John Wiley & Sons, pp. 227-243. 6. Raymond C. R, Paul J. S., Marian E. Q. (2009), Handbook of Pharmaceutical Excipients, Pharmaceutical Press, American Pharmacists Association, pp. 94-99, 433-435, 517-522. 7. The United States Pharmacopeial Convention (2018), The United States Pharmacopeia 41, pp. 4742-4743. 8. Zheng M. (2017), "Inclusion Complex of α-Lipoic Acid Containing Alkalizer for Improving the Solubility and Stability Prepared by Co-grinding", Indian Journal of Pharmaceutical Sciences, pp. 544-552.
File đính kèm:
 nghien_cuu_bao_che_vien_nen_acid_alpha_lipoic_300_mg.pdf
nghien_cuu_bao_che_vien_nen_acid_alpha_lipoic_300_mg.pdf

