Các giải pháp kỹ thuật kiểm soát bệnh hoại tử gan tụy cấp trên tôm chân trắng (litopenaeus vannamei) nuôi thâm canh quy mô trang trại ở đồng bằng sông Cửu Long
Bệnh hoại tử gan tụy cấp (AHPND) do vi khuẩn Vibrio parahaemolyticus là nguyên nhân gây tôm
chết hàng loạt ở ĐBSCL. Mục tiêu của nghiên cứu này là tìm các giải pháp kỹ thuật để kiểm soát
dịch bệnh AHPND. Nghiên cứu được thực hiện trên 11 ao trong thời gian nuôi 88-98 ngày. Các thí
nghiệm tập trung hạn chế mật độ V. parahaemolyticus trong nước bằng chất diệt khuẩn và bổ sung
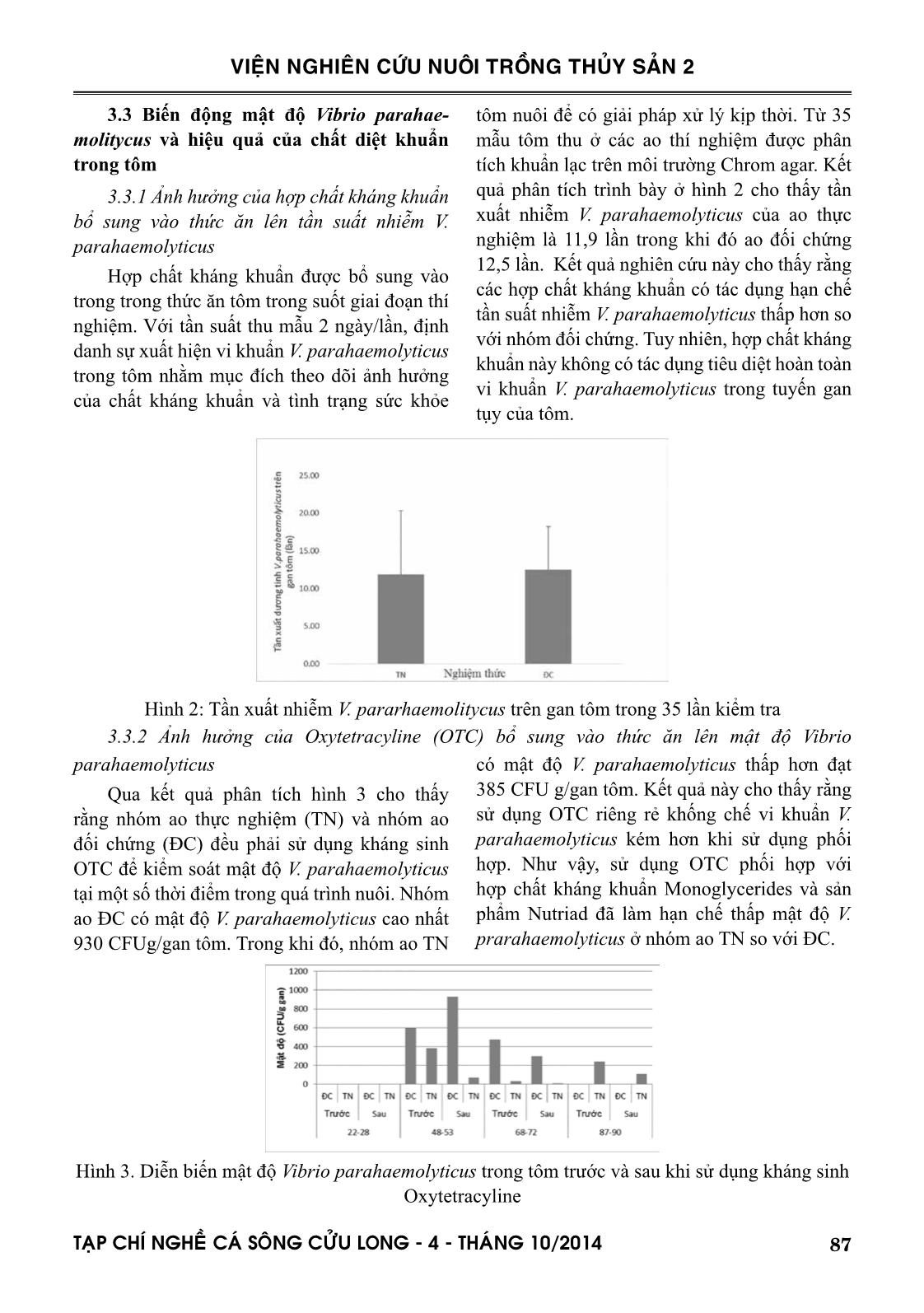
chế phẩm vi sinh và trong tôm bằng các hợp chất kháng khuẩn (Monoglycerides, sản phẩm của Nutriad) và kháng sinh Oxytetracyline 10g/kg bổ sung trong thức ăn trong quá trình nuôi. Kết quả cho
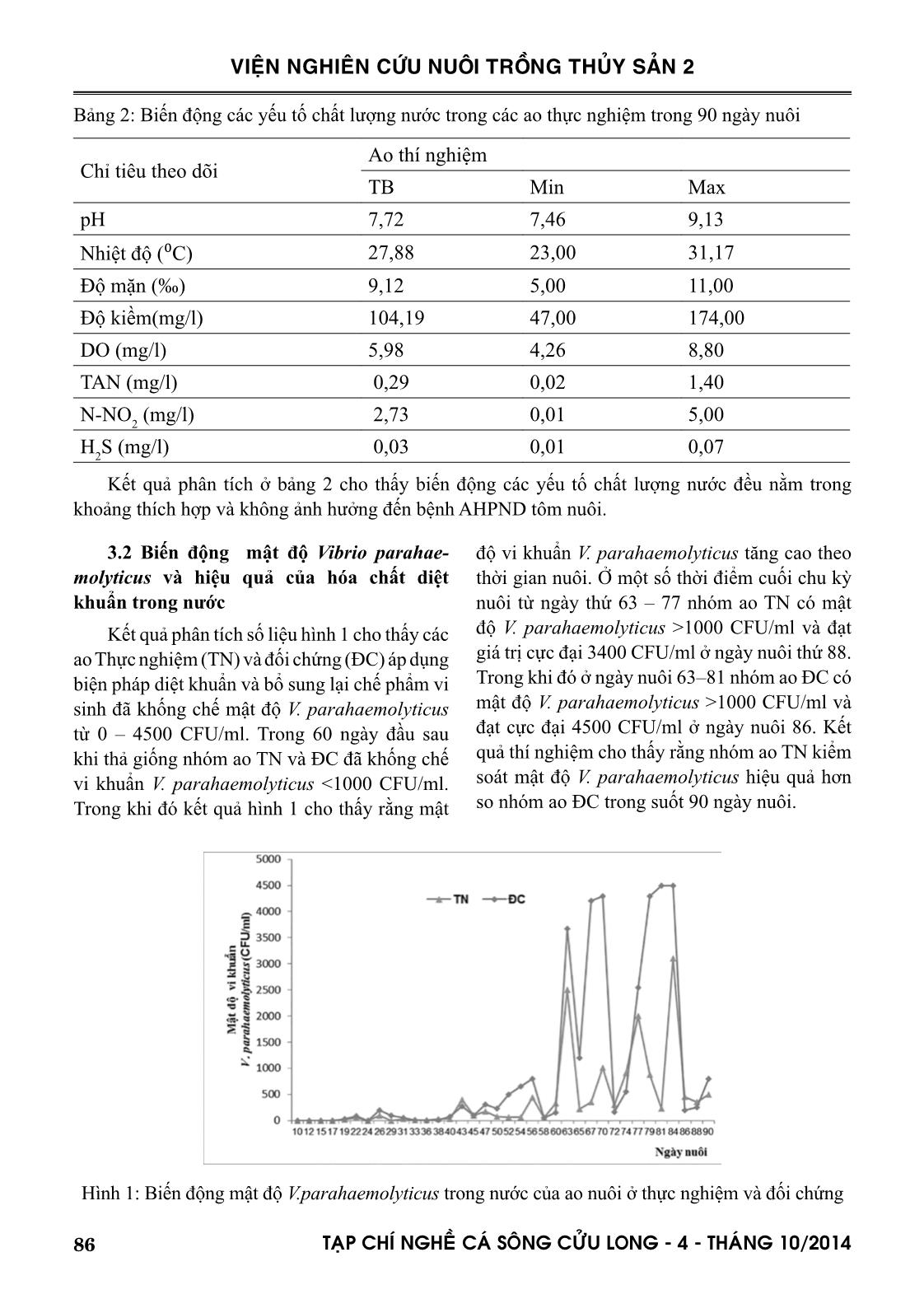
thấy, hai nghiệm thức thí nghiệm khống chế mật độ V. parahaemolyticus trong nước từ 0 – 4.500
CFU/ml. Nhóm ao sử dụng các hợp chất kháng khuẩn kết hợp với Oxytetracyline liều 10g/kg thức
ăn bổ sung trong thức ăn giúp hạn chế mật độ V. parahaemolyticus có ý nghĩa so đối chứng. Kết quả
nghiên cứu cho thấy tỷ lệ sống của tôm ở nhóm ao thực nghiệm đạt lần lượt 87,53 ± 7,5 (%); FCR:
1,46 ± 0,14, năng suất: 12,38 ± 1,31 tấn/ha. Ngược lại, nhóm ao đối chứng tỷ lệ sống: 60,69 ± 34,50
(%), FCR: 1,65 ± 0,55 và năng suất: 9,39 ± 4,47 tấn/ha. Bước đầu cho thấy giải pháp bổ sung các
chất kháng khuẩn, kháng sinh trong thức ăn, diệt khuẩn và chế phẩm vi sinh trong nước kiểm soát
được bệnh AHPND ở điều kiện sản xuất.

Trang 1

Trang 2

Trang 3
Trang 4
Trang 5

Trang 6

Trang 7

Trang 8

Trang 9
Tóm tắt nội dung tài liệu: Các giải pháp kỹ thuật kiểm soát bệnh hoại tử gan tụy cấp trên tôm chân trắng (litopenaeus vannamei) nuôi thâm canh quy mô trang trại ở đồng bằng sông Cửu Long

83TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 1 Phòng Nguồn lợi và Khai thác Thủy sản Nội địa, Viện Nghiên cứu Nuôi trồng Thủy sản 2 * Email: [email protected] 2 Trung tâm Quốc gia Quan trắc Cảnh báo Môi trường & Phòng ngừa Dịch bệnh Thủy sản Khu vực Nam bộ, Viện Nghiên cứu Nuôi trồng Thủy sản 2. 3 Viện Nghiên cứu Nuôi trồng Thủy sản 2. CÁC GIẢI PHÁP KỸ THUẬT KIỂM SOÁT BỆNH HOẠI TỬ GAN TỤY CẤP TRÊN TÔM CHÂN TRẮNG (Litopenaeus vannamei) NUÔI THÂM CANH QUY MÔ TRANG TRẠI Ở ĐỒNG BẰNG SÔNG CỬU LONG Nguyễn Văn Phụng1*, Lê Hồng Phước2, Nguyễn Văn Hảo3 TÓM TẮT Bệnh hoại tử gan tụy cấp (AHPND) do vi khuẩn Vibrio parahaemolyticus là nguyên nhân gây tôm chết hàng loạt ở ĐBSCL. Mục tiêu của nghiên cứu này là tìm các giải pháp kỹ thuật để kiểm soát dịch bệnh AHPND. Nghiên cứu được thực hiện trên 11 ao trong thời gian nuôi 88-98 ngày. Các thí nghiệm tập trung hạn chế mật độ V. parahaemolyticus trong nước bằng chất diệt khuẩn và bổ sung chế phẩm vi sinh và trong tôm bằng các hợp chất kháng khuẩn (Monoglycerides, sản phẩm của Nu- triad) và kháng sinh Oxytetracyline 10g/kg bổ sung trong thức ăn trong quá trình nuôi. Kết quả cho thấy, hai nghiệm thức thí nghiệm khống chế mật độ V. parahaemolyticus trong nước từ 0 – 4.500 CFU/ml. Nhóm ao sử dụng các hợp chất kháng khuẩn kết hợp với Oxytetracyline liều 10g/kg thức ăn bổ sung trong thức ăn giúp hạn chế mật độ V. parahaemolyticus có ý nghĩa so đối chứng. Kết quả nghiên cứu cho thấy tỷ lệ sống của tôm ở nhóm ao thực nghiệm đạt lần lượt 87,53 ± 7,5 (%); FCR: 1,46 ± 0,14, năng suất: 12,38 ± 1,31 tấn/ha. Ngược lại, nhóm ao đối chứng tỷ lệ sống: 60,69 ± 34,50 (%), FCR: 1,65 ± 0,55 và năng suất: 9,39 ± 4,47 tấn/ha. Bước đầu cho thấy giải pháp bổ sung các chất kháng khuẩn, kháng sinh trong thức ăn, diệt khuẩn và chế phẩm vi sinh trong nước kiểm soát được bệnh AHPND ở điều kiện sản xuất. Từ khóa: Vibrio parahaemolyticus, tôm chân trắng, monoglyceries, Nutriad, Kiên Giang I. ĐẶT VẤN ĐỀ Tình hình dịch bệnh tôm đang diễn ra và thiệt hại nặng về kinh tế đến người nuôi tôm ở các tỉnh ven biển Đồng bằng sông Cửu Long. Nguyên nhân tôm chết được xác định do bệnh hoại tử gan tụy cấp từ năm 2010 đến nay (Lê Hồng Phước và ctv., 2012). Theo kết quả thống kê của Tổng cục Thủy sản (2012), cả nước có khoảng 100.776 ha diện tích tôm nước lợ bị thiệt hại do dịch bệnh. Trong đó, có 91.174 ha nuôi tôm sú và 7.068 ha tôm thẻ chân trắng bị thiệt hại do bệnh hoại tử gan tụy cấp tính và đốm trắng. Các tỉnh bị thiệt hại nhiều nhất là Sóc Trăng: 23.371 ha, Bạc Liêu: 16.919 ha, Trà Vinh: 12.224 ha, và Bến Tre: 2.237 ha. Trước tình hình đó, các cơ quan nghiên cứu trong và ngoài nước tập trung nghiên cứu tác nhân gây ra hội chứng hoại tử gan tụy cấp EMS/AHPNS. Lightner và ctv., (2012) cho rằng tác nhân gây hội chứng hoại tử gan tụy có thể là độc tố (từ môi trường nuôi, thức ăn hoặc từ vi khuẩn). Mới đây, Lộc và ctv., (2013) đã công bố tác nhân gây bùng nổ dịch hội chứng hoại tử gan tụy cấp (EMS/AHPNS) gây ra bởi vi khuẩn 84 TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 Vibrio parahaemolyticus có khả năng sản sinh độc tố gây nên tổn thương gan tụy của tôm. Kết quả này rất quan trọng vì nó giúp thu hẹp hướng nghiên cứu, hỗ trợ chuẩn đoán bệnh cũng như cảnh báo nguy cơ dịch bệnh khi có vi khuẩn này hiện diện. Hiện nay, chưa có công trình nào công bố về biện pháp phòng chống bệnh hoại tử gan tụy cấp một cách hữu hiệu. Mục đích của nghiên cứu này là nhằm xác định các giải pháp kỹ thuật tổng hợp để giải quyết hiệu quả về kĩ thuật để có thể áp dụng rộng rãi vào sản xuất hiện nay góp phần phát triển bền vững nghề nuôi tôm. II. VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU 2.1 Vật liệu nghiên cứu Tất cả 11 ao nuôi được lót bạt bờ, có diện tích từ 1000 – 3000 m2. Trong đó 7 ao diện tích 3000 m2 và 4 ao diện tích 1000 m2. Mật độ thả giống 86-106 con/m2. Độ sâu mực nước trước khi thả giống là 1,4m. Hệ thống quạt nước lắp đặt theo hệ thống trục dài tổng công suất 6 – 12HP/ao. Ao 3000 m2 lắp đặt 4 hệ thống quạt, mỗi hệ thống có 12 cánh, tổng 12HP. Ao 1000 m2 được lắp đặt 10 cánh quạt tổng công suất 6HP. Hệ thống quạt nước hoạt động 24h/ngày. Tôm PL 12 sạch bệnh có nguồn gốc từ công ty cổ phần thủy sản Trung Sơn. Thí nghiệm được thực hiện từ tháng 08 đến tháng 12 năm 2013 tại Công ty Cổ phần Trung Sơn (Ấp Ngã Tư, xã Dương Hòa, Kiên Lương, Kiên Giang). 2.2 Phương pháp bố trí thí nghiệm Trong nghiên cứu này, giải pháp kỹ thuật tầm soát vi khuẩn Vibrio parahaemolyticus trong nước và trong tôm được tiến hành với tần suất 2 ngày/lần. Dựa trên kết quả tầm soát này để xây dựng các biện pháp kỹ thuật xử lý kịp thời nhằm hạn chế bệnh AHPND ở mức thấp nhất. Thí nghiệm được bố trí làm hai nghiệm thức: - Nhóm ao thực nghiệm (TN): sử dụng các hợp chất kháng khuẩn bổ sung vào thức ăn. Hợp chất kháng khuẩn gồm hai chất: monoglyceri- des có nguồn gốc từ acid béo và sản phẩm của Nutriat có nguồn gốc từ thảo dược. Nhóm các ao TN được bố trí trên 7 ao nuôi có diện tích 3000 m2/ao. - Nhóm ao đối chứng (ĐC): không sử dụng các hợp chất kháng khuẩn Monoglycerides và sản phẩm Nutriad bổ sung vào thức ăn. Nhóm các ao ĐC được bố trí 4 ao diện tích 1000 m2/ao. Nhóm ao ĐC và TN quản lý môi trường nước thông qua việc tầm soát vi khuẩn V. pa- rahaemolyticus. Mật độ V. parahaemolyticus ≥ 1000 CFU/ml được xử lý bằng hóa chất diệt khuẩn và 24 giờ có bổ sung chế phẩm vi sinh ngọai lai. Ngược lại, mật độ V. parahaemolyti- cus <1000 CFU/ml được xử lý bằng chế phẩm vi sinh định kỳ 7 ngày/lần. Trong tôm, khi tầm soát trong tuyến gan tụy phát hiện có V. pa- rahaemolyticus thì sử dụng Oxytetracyline (OTC) cho ăn với liều 10g/kg thức ăn. Loại thức ăn thương mại được sử dụng trong thí nghiệm có protein 30 – 35%. Tháng thứ nhất, lư ... Diễn biến mật độ Vibrio parahaemolyticus trong tôm trước và sau khi sử dụng kháng sinh Oxytetracyline 88 TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 3.4 Đánh giá tăng trưởng và năng suất tôm Kết quả phân tích bảng 3 cho thấy ở nhóm ao thực nghiệm (TN) có năng suất đạt cao nhất 12376,3 ± 1307,3 tấn/ha. Tuy nhiên, khác biệt không có ý nghĩa thống kê so với nhóm ao đối chứng (ĐC) 9393,2 ± 4465,5 tấn/ha. Nhóm ao TN và ao ĐC có tốc độ tăng trưởng, hệ số thức ăn (FCR) và trọng lượng thu hoạch khác biệt không có ý nghĩa trong thống kê. Tuy nhiên, tỷ lệ sống và thời gian nuôi khác biệt có ý nghĩa thống kê (P<0,05) so với nghiệm thức đối chứng. Bảng 3. Năng suất và tăng trưởng của tôm trong ao thí nghiệm Thông số Đơn vị TN ĐC Trọng lượng thu hoạch g/con 14,66±2a 15,09±1,34a Thời gian nuôi Ngày 95,10±4,22a 89,00±0,0b Hệ số thức ăn (FCR) g/g 1,46±0,14a 1,65±0,55a Năng suất kg/ha 12376,3±1307,3a 9393,2a ±4465,5 Tỷ lệ sống % 87,53 ± 7,50a 60,69±34,5b Tốc độ tăng trưởng g/con 0,15 ±0,02a 0,17 ±0,02a Ký hiệu các chữ cái trên trên cùng một hàng ngang khác nhau thể hiện sự khác biệt có ý nghĩa thống kê (p<0,05) IV. THẢO LUẬN Giải pháp kỹ thuật chính trong nghiên cứu này là sử dụng biện pháp tầm soát mật độ Vibrio parahaemolyticus với tần xuất 2 ngày/lần trong suốt chu kỳ nuôi. Dựa vào kết quả tầm soát này, chúng tôi có cơ sở khoa học để áp dụng các biện pháp kỹ thuật can thiệp trực tiếp tại ao nuôi nhằm giảm mật độ V. parahamolyticus trong nước ở ngưỡng thấp nhất <1000 CFU/ml. Kết quả hình 1 cho thấy rằng biến động mật độ V. parahaemolyticus đều phụ thuộc vào tác động kỹ thuật can thiệp tại từng thời điểm của quá trình nuôi. Kết quả tầm soát vi khuẩn cũng cho thấy rằng càng về cuối chu kỳ nuôi (sau 60 ngày nuôi) hàm lượng hữu cơ trong nước tăng, lúc này ở hai nhóm ao thực nghiệm (TN) và đối chứng (ĐC) có mật độ V. parahaemolyticus tăng cao >1000 CFU/ml. Tại các thời điểm này chúng tôi áp dụng biện pháp diệt khuẩn và 24h bổ sung lại chế phẩm vi sinh đã làm giảm thấp đáng kể mật độ V. parahaemolyticus. Như vậy, sử dụng giải pháp tầm soát và can thiệp đúng thời điểm bằng hóa chất diệt khuẩn và bổ sung chế phẩm vi sinh đã khống chế mật độ V. parahaemolyticus từ 0 – 4500 CFU/ml ở nhóm ao TN và ĐC. Kết quả cho thấy với mật độ trên không thấy sự xuất hiện bệnh AHPND trong điều kiện sản xuất. Trong khi đó kết quả nghiên cứu nghiên cứu của Tran và ctv., (2013) lây nhiễm bằng cách ngâm vào dịch vi khuẩn V. parahaemolyticus với mật độ tế bào 106 - 108 cfu/ml, sau 4 ngày lây nhiễm, kết quả cho thấy 100% tôm chết với biểu hiện bệnh hoại tử gan cấp tính. Hợp chất Monoglyceride được biết như là một chất kháng khuẩn và kháng virus được sử dụng trong dược phẩm ở người và thuốc thú y. Hợp chất này được xem như là một chất dự phòng thay thế cho thuốc kháng sinh. Trong khi đó, sản phẩm Nutriad là hợp chất chiết xuất từ thực vật, được lựa chọn nhờ đặc tính kháng khuẩn và diệt khuẩn, chống vi khuẩn gây hại trong môi trường thí nghiệm. Hợp chất này cũng được chứng minh có khả năng ức chế vi khuẩn phát tín hiệu Quorum Sensing ở nồng độ thấp hơn nồng độ ức chế, cho phép kiểm soát hiệu quả hệ vi sinh vật đường ruột theo hướng có lợi hơn (Coutteau và ctv., 2010). Bệnh AH- PND gây ra do tác nhân chính là vi khuẩn V. parahaemolyticus (Loc và ctv., 2013). Do đó, biện pháp tầm soát trong tuyến gan tụy tôm là 89TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 cần thiết để phát hiện sớm vi khuẩn V. para- haemolyticus, nghiên cứu đã áp dụng hợp chất kháng khuẩn Monoglycerides và sản phẩm của Nutriad bổ sung vào thức ăn sau khi tôm được 1 ngày tuổi và đến cuối chu kỳ nuôi. Kết quả hình 2 cho thấy tần xuất nhiễm V.parahaemolyticus giữa nhóm ao thực nghiệm và ao đối chứng thể hiện không rõ ràng. Tuy nhiên, khi quan sát trên tôm nuôi nhận thấy rằng nhóm ao thực nghiệm sử dụng hợp chất kháng khuẩn có màu sắc gan tụy tốt hơn so với ao đối chứng. Như vậy, các hợp chất kháng khuẩn chỉ có tác dụng kiềm chế sự phát triển vi khuẩn V. Parahaemolyticus. Tuy nhiên, không có tác dụng diệt vi khuẩn V. pa- rahaemolyticus hoàn toàn trong tuyến gan tụy của tôm. Kháng sinh là những chất có khả năng tiêu diệt vi khuẩn hay kìm hãm sự phát triển của vi khuẩn một cách đặc hiệu. Một số loại kháng sinh phổ biến như: oxytetracyline, florfenicol, sarafloxacine và enrofloxacine để sử dụng điều trị bệnh trong nuôi trồng thủy sản (Soto-Rodri- guez và ctv., 2006). Oxytetracyline, kháng sinh sử dụng rộng rãi trong nuôi tôm và cá, được sử dụng ức chế vi khuẩn Vibrio (Reed và ctv., 2006). Nghiên cứu này sử dụng oxytetracyline (OTC) nhằm tiêu diệt vi khuẩn V. parahae- molyticus trên tôm. Với nồng độ OTC 10g/kg thức ăn sử dụng 5 ngày liên tục. Kết quả kiểm tra mật độ vi khuẩn V. parahaemolyticus trên gan tôm ở nhóm ao đối chứng (ĐC) cao hơn 2-3 lần so với nhóm thực nghiệm (TN). Nhóm ao TN sử dụng phối hợp với kháng sinh OTC đã làm giảm mật độ V. parahaemolyticus thấp hơn so với nhóm ao ĐC lần lượt tại các thời điểm 48-53 ngày, 68-72 và 87-90 ngày nuôi. Một vài kết quả nghiên cứu gần đây của các tác giả Morales-Covarrubias, M.S. ctv., (2012) sử dụng florfenicol (FF) liều 1.000g/kg thức ăn và oxytetracycline (OTC) liều 6.070 g/kg thức ăn diệt vi khuẩn NHPB hiệu quả cao trên tôm chân trắng. Theo nghiên cứu Chanratchakool và ctv., (1991); Frelier và ctv., (1993) cho rằng bổ sung OTC liều 3-5g/kg thức ăn để điều trị bệnh NHP trên tôm sú. Trong nghiên cứu này, bổ sung kháng sinh OTC 10g/kg thức ăn ở nhóm ao đối chứng có độ mẫn cảm vi khuẩn V. para- haemolyticus thấp hơn khi dùng phối hợp với các hợp chất kháng khuẩn. Kết quả tăng trưởng và năng suất tôm ở nhóm ao thực nghiệm (TN) và đối chứng (ĐC) cho thấy rằng tốc độ tăng trưởng, FCR và năng suất khác biệt không có ý nghĩa về mặt thống kê. Tuy nhiên, năng suất và tỷ lệ sống ở nhóm ao TN cao hơn so với đối chứng. Đồng thời FCR thấp hơn so với đối chứng. Như vậy, việc sử dụng hợp chất kháng khuẩn không ảnh hưởng đến tốc độ tăng trưởng tôm và tăng năng suất và tỷ lệ sống, đồng thời làm giảm thấp FCR trong nghiên cứu thí nghiệm. Theo tác giả Hermsen., (2014) nghiên cứu cho thấy hợp chất Monoglyceride có khả năng kháng bệnh cao, tỷ lệ sống giữa nghiệm thức sử dụng monogly- ceride trên 80%. Nghiên cứu của Coutteau và ctv., (2010) bổ sung hợp chất kháng khuẩn của Nutriad thúc đẩy tôm tăng trưởng ở điều kiện phòng thí nghiệm; tăng 20% tăng trọng hàng tuần và cải thiện 4% tỉ lệ chuyển đổi thức ăn. Tương tự như kết quả của hai tác giả (Coutteau; Hermsen), nghiên cứu này sử dụng các hợp chất kháng khuẩn Monoglycerides và sản phẩm Nut- riad bổ sung trong thức ăn trong thí nghiệm cho thấy tăng năng suất, tỷ lệ sống tôm nuôi và giảm FCR so với nhóm ao đối chứng. V. KẾT LUẬN 5.1 Kết luận Thí nghiệm cho thấy rằng các giải pháp kỹ thuật kiểm soát bệnh AHPND dựa trên biện pháp tầm soát định kỳ 2 ngày/lần đã khống chế mật độ Vibrio parahaemolyticus <4500 CFU/ml trong nước và tôm nuôi <1000 CFU/g gan tôm. Bước đầu cho thấy giải pháp bổ sung các hóa chất diệt khuẩn, chế phẩm vi sinh trong nước và hợp chất kháng khuẩn, kháng sinh Oxyte- tracyline trong thức ăn kiểm soát được bệnh AHPND ở điều kiện sản xuất. 90 TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 5.2 Đề nghị Để hạn chế bệnh AHPND trên tôm chân trắng cần phải tầm soát mật độ Vibrio paraha- emolyticus trong nước và trong tôm để có giải pháp khống chế bằng chất diệt khuẩn và kết hợp với vi sinh. Oxytetracyline có thể sử dụng với liều lượng thích hợp khi tôm nhiễm mầm bệnh, không nên sử dụng kháng sinh định kỳ. Cần nghiên cứu thêm cơ sở khoa học của việc ứng dụng chất diệt khuẩn và sử dụng vi sinh. Trong tương lai gần, cần nghiên cứu thử nghiệm vài chất kháng khuẩn khác thay thế kháng sinh để tăng chất lượng tôm thương phẩm. CẢM ƠN Nghiên cứu này được thực hiện từ đề tài “Nghiên cứu đề xuất mô hình nuôi tôm sú và tôm thẻ chân trắng phòng chống hội chứng chết sớm” thuộc chương trình Dịch bệnh tôm khẩn cấp, Bộ Nông Nghiệp đã tài trợ kinh phí cho nghiên cứu này. Tác giả chân thành cảm ơn đến Công ty cổ phần thủy sản Trung Sơn đã hợp tác trong nghiên cứu này. TÀI LIỆU THAM KHẢO Tài liệu tiếng Việt Lê Hồng Phước, Lê Hữu Tài và Nguyễn Văn Hảo, 2012. Diễn biến của hội chứng hoại tử gan tụy trong ao nuôi tôm thâm canh ở huyện Trần Đề, Tỉnh Sóc Trăng. Báo cáo khoa học. 268-277. Nguyễn Thị Ngọc Tĩnh, Văn Thị Thúy, Nguyễn Văn Chắc, 2013. Phân lập và khảo sát đặc tính pro- biotic của các chủng Bacillus spp. Từ môi trường ao nuôi cá tra tại tỉnh Đồng Tháp. Tạp chí nghề cá sông Cửu long -2-tháng 11-2013. Tài liệu tiếng Anh Balcazar, J.L., de Blas, I., Ruiz-Zarzuela, I., Cun- ningham, D., Vendrell, D., Muzquiz, J.L., 2006. The role of probiotics in aquaculture. Veterinary Microbiology 114, 173–186. Charatchkool, P., Limsuwan, C.,1991. Accumulation of oxytetracycline in tiger shrimp Penaeus monodon (Fabricius). Thai Fisher Gazette. 44: 31-33. Coutteau, P., PhD thesis, 2013. Novel additive to reduce economic impact of disease on shrimp production. International Aqufeed, 29-32. Defoirdt, T., Halet, D., Sorgeloos, P., Bossier, P., Verstraete, W., 2006. Short chain fatty acids protect gnotobiotic Artemia franciscana from pathogenic Vibrio campbellii. Aquaculture 261: 804-808. Eleraky, N.Z., Potgieter, L.N., Kennedy, M.A., 2002. Virucidal efficacy of 4 new disinfectants. J Am Anim Hosp Assoc 38(3): 231–234. Frelier, P.F., Loy, J.F., Kruppenbach, B.,1993. Trans- mission of Necrotizing Hepatopancreatitis in Penaeus vannamei. J. Invert. Pathol. 61:44-48. Hermsen, D., 2014. Development of 1-Monoglycerides Against AHPN. Global aquaculture advocate. 18-21. Loc Tran, Linda Nunan, Rita, M., Redman, Leone, L., Mohney, Carlos R., Pantoja, Kevin Fitzsimmons, Donald, V., Lightner., 2013. Determination of the infectious nature of the agent of acute hepatopancreatic necrosis syndrome affecting penaeid shrimp. Dis Aquat Org.Vol. 105: 45–55. doi: 10.3354/dao02621. Lightner, D.V., Redman, R.M., Pantoja, C.R., Noble, B.L., Loc Tran., 2012. Early Mortality Syndrome. Global aquaculture advocate 2/2012, p40. Morales-Covarrubias, M.S., 2012. Necrotising hepatobacterium (NHPB) infection in Penaeus vannamei with florfenicol and oxytetracycline: a comparative experimental study Revista Científica, vol. XXII, núm. 1, enero-febrero, 2012, pp. 72-80, Universidad del Zulia Venezuela. Reed, L. A.; Siewicki., Shah, J.C., 2006. The biopharma- ceutics and oral bioavailability of two forms of oxytetracy- cline to the white shrimp, Litopenaeus setiferus. Aquac. 258: 42-54. Soto-Rodríguez, S., Armenta, M., & Gomez-Gil, B., 2006. Effects of enrofloxacin and florfenicol on survival and bacterial population in an experimental infection with luminescent Vibrio campbellii in shrimp larvae of Litopenaeus vannamei. Aquaculture,vol.255, pp.48-54. Vaseeharan and P. Ramasam, 2003. Control of pathogenic Vibrio spp. by Bacillus subtilis BT23, a possible probiotic treatment for black tiger shrimp Penaeus monodon. The Society for Applied Microbiology, Letters in Applied Microbiology, 36, 83–87. Wutzler, P., Sauerbrei, A., 2000. Virucidal efficacy of a combi- nation of 0.2% peracetic acid and 80% (v/v) ethanol (PAA-ethanol) as a potential hand disinfectant. J Hosp Infect 46(4):304–8 91TAÏP CHÍ NGHEÀ CAÙ SOÂNG CÖÛU LONG - 4 - THAÙNG 10/2014 VIỆN NGHIÊN CỨU NUÔI TRỒNG THỦY SẢN 2 TECHNICAL SOLUTIONS TO CONTROL ACUTE EPATOPANCREATIC NECROSIS DISEASE OF WHITE LEG SHRIMP (Litopenaeus vannamei) IN INTENSIVE FARMING IN MEKONG DELTA Nguyen Van Phung1*, Le Hong Phuoc2, Nguyen Van Hao3 ABSTRACT The Acute Hepatopancreatic Necrosis Disease (AHPND) caused by Vibrio parahaemolyticus has been happened a mass mortality of shrimp culture in the Mekong Delta, Vietnam. The aim of this re- search is to find out effective technical solutions which can be reduced the AHPND. This study was conducted on 11 grow out ponds within 88-98 days of culture. Experiments carried out to reduce V. parahaemolyticus density in water colume and hetopancreas of L. vannamei by disinfectants com- bining probiotic, and Monoglycerides and Nutriad’s products and Oxytetracyline in oral feeding during culture period respectively. The results showed that applying the disinfectants combining probiotic controlled V. parahaemolyticus density about 0 – 4.500 cfu/ml in water colume. The ex- periments that used Monoglycerides and Nutriad’s products combining with 10g of Oxytetracyline per 1kg shrimp helped to decrease the V. parahaemolyticus density in hetopancreas of shrimp sig- nificantly. The results recorded that average of survival rate 87.53 ± 7.5 (%), FCR 1.46 ± 0.14 and yield reached 12.38 ± 1.30 ton/ha, while those control treatment average of survival rate 60.69 ± 34.50 (%), FCR 1.65 ± 0.55 , yeild reached 9.39 ± 4.46 ton/ha. Preliminary results presented that using anti-microbials and antibiotics in oral feed, and using disinfectants combining probiotic in water can to control the AHPND in shrimp farming. Keywords: Vibrio parahaemolyticus, white shrimp, monoglyceries, Nutriad, Kien Giang Người phản biện: ThS. Nguyễn Nhứt Ngày nhận bài: 10/8/2014 Ngày thông qua phản biện: 28/8/2014 Ngày duyệt đăng: 05/9/2014 1 Inland Fisheries Resources & Capture Division, Research Institure for Aquaculture No.2. * Email: [email protected] 2 Southern Monitoring Center for Aquaculture Environment and Epidemic, Research Institute for Aquaculture No.2. 3 Research Institute for Aquaculture No.2.
File đính kèm:
 cac_giai_phap_ky_thuat_kiem_soat_benh_hoai_tu_gan_tuy_cap_tr.pdf
cac_giai_phap_ky_thuat_kiem_soat_benh_hoai_tu_gan_tuy_cap_tr.pdf

