Bài giảng Hóa đại cương - Chương 11: Dung dịch lỏng - Huỳnh Kỳ Phương Hạ
KHÁI NIỆM VỀ DUNG DỊCH
Định nghĩa
• Dung dịch là hệ đồng thể gồm chất tan (chiếm phần
nhỏ) và dung môi (chiếm phần lớn), thành phần của
dung dịch có thể thay đổi trong giới hạn rộng.
•
• Dung dịch có thể ở pha khí, lỏng hay rắn.
• Mỗi chất trong dung dịch được gọi là cấu tử.
• Dung môi là chất dùng để hòa tan chất tan.

Trang 1

Trang 2

Trang 3
Trang 4

Trang 5

Trang 6
Trang 7

Trang 8

Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa đại cương - Chương 11: Dung dịch lỏng - Huỳnh Kỳ Phương Hạ", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa đại cương - Chương 11: Dung dịch lỏng - Huỳnh Kỳ Phương Hạ

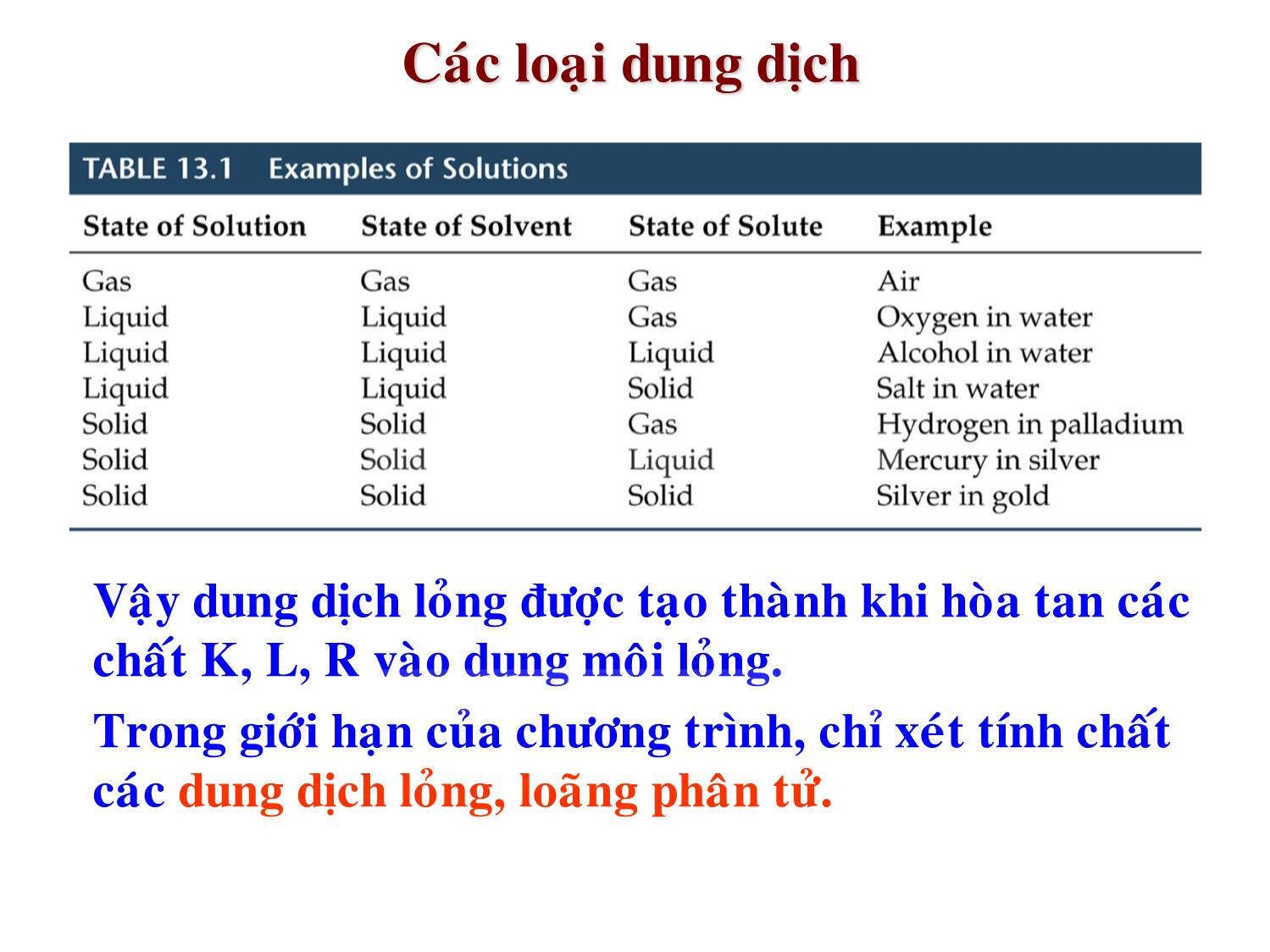
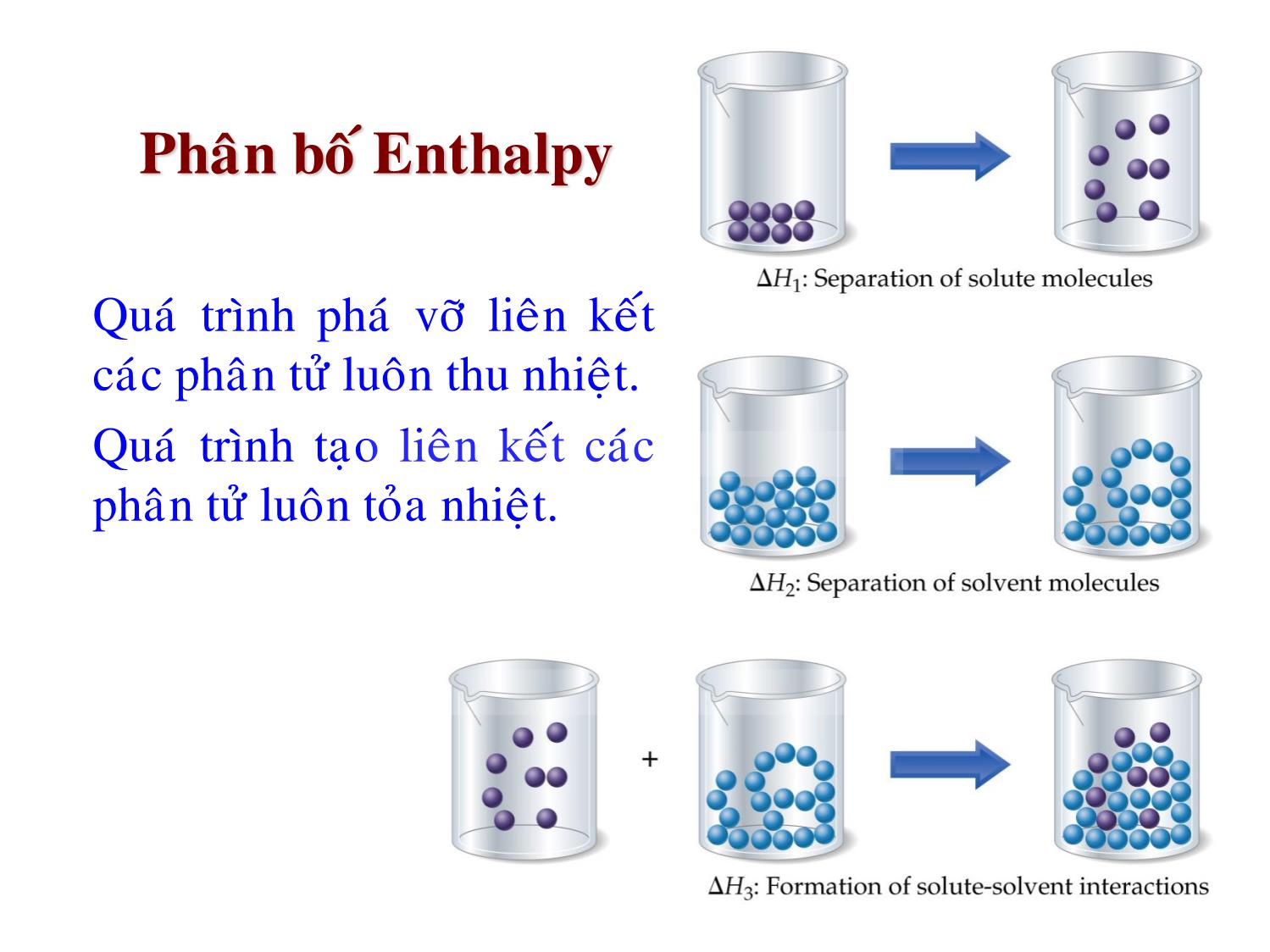
Chương 11 DUNG DỊCH LỎNG • Định nghĩa • Dung dịch là hệ đồng thể gồm chất tan (chiếm phần nhỏ) và dung môi (chiếm phần lớn), thành phần của dung dịch có thể thay đổi trong giới hạn rộng. • • Dung dịch có thể ở pha khí, lỏng hay rắn. • Mỗi chất trong dung dịch được gọi là cấu tử. • Dung môi là chất dùng để hòa tan chất tan. KHÁI NIỆM VỀ DUNG DỊCH Tùy thuộc kích thước hạt của chất phân ta có: • Huyền phù: Hệ dị thể gồm ít nhất 1 cấu tử có kích thước lớn hơn 1μm, lớn hơn hệ keo. • • Hệ keo: Hệ dị thể có các hạt phân tán có kích thước từ 1 đến 1000 nm. – Nguồn: (and suspension) • • (Nhũ tương: Hệ các hạt chất lỏng không tan trong dung môi lỏng) Các loại dung dịch • Vậy dung dịch lỏng được tạo thành khi hòa tan các chất K, L, R vào dung môi lỏng. • Trong giới hạn của chương trình, chỉ xét tính chất các dung dịch lỏng, loãng phân tử. • Xét quá trình hòa tan của NaCl vào nước: • Liên kết hydro của nước phải bị phá vỡ. • NaCl phân ly thành Na+và Cl-. • Lực lưỡng cực-ion được thiết lập: • Na+ -OH 2 và Cl - +H 2 O. • Sự tương tác giữa chất tan và dung môi gọi là sự solvat hóa (solvation). –Nếu dung môi là nước ta gọi là sự hydrat hóa. Sự tạo thành dung dịch • Có 3 loại (bước) năng lượng khi tạo thành dung dịch: – Năng lượng tách phân tử chất tan ( H 1 ). – Năng lượng tách các phân tử dung môi (H 2 ). – Năng lượng tạo thành liên kết giữa các phân tử chất tan – dung môi ( H 3 ). • Enthalpy của cả quá trình hòa tan là: H hoà tan = H 1 + H 2 + H 3 . • H hòa tan có thể âm hoặc dương phụ thuộc vào lực nội phân tử các quá trình. Sự thay đổi năng lượng khi tạo thành dung dịch Phân bố Enthalpy • Quá trình phá vỡ liên kết các phân tử luôn thu nhiệt. • Quá trình tạo liên kết các phân tử luôn tỏa nhiệt. • Để xác định H ht dương hay âm, ta xem xét độ mạnh của liên kết phân tử chất tan-chất tan và chất tan- dung môi: • H 1 và H 2 đều dương. • H 3 luôn âm. • Nếu H 3 > H 1 + H 2 thì quá trình hòa tan tỏa nhiệt (ví dụ hòa tan NH 4 NO 3 vào nước có Hht = + 26.4 kJ/mol). • Nếu H 3 < H 1 + H 2 thì quá trình hòa tan tỏa nhiệt (ví dụ hòa tan NaOH vào nước có Hht = -44.48 kJ/mol). Tính chất enthalpy của dung dịch • Qui luật: Chất phân cực hòa tan trong dung môi phân cực, chất không phân cực hòa tan trong dung môi không phân cực (độ phân cực càng gần độ tan càng lớn). Nếu H ht quá dương thì không tạo thành dung dịch. • NaCl trong xăng: lực ion-lưỡng cực yếu vì xăng là chất không cực. Do đó lực ion-lưỡng cực không đủ bù với lực phân ly ion. • Nước trong octane: Nước có liên kết Hydro mạnh. Không có lực hút giữa nước và octane để bù vào lực liên kết hydro. Quá trình hòa tan Phần khối lượng, ppm (parts per million) và ppb (parts per billion ). Definitions: CÁC LOẠI NỒNG ĐỘ DUNG DỊCH 100 solution of mass total solutionin component of mass component of % mass 6 10 solution of mass total solutionin component of mass component of ppm 9 10 solution of mass total solutionin component of mass component of ppb Nồng độ phần mol (N) solution of moles total solutionin A of moles N A solution of liters solute moles C M Nồng độ mol (C M , mol/lit) ),1(1N i solutionofcomponentsallni solvent of kg solute moles m C Nồng độ molan (C m , mol/kg dung môi) • Hòa tan: chất tan + dung môi dung dịch. • Kết tinh: dung dịch chất tan + dung môi. • Sự bão hòa: Khi cân bằng hòa tan – kết tinh thiết lập. • Độ tan: Lượng chất tan cần thiết để tạo dung dịch bão hòa ở điều kiện xác định (g chất tan/ 100g dung môi). • Ví dụ: Độ tan của NaCl trong 100 ml H 2 O ở 100 o C là 35.9g. Độ tan và Dung dịch bão hòa Cân bằng động Dung dịch bão hòa Tương tác Chất tan – Dung môi Áp suất: Độ tan của khí ảnh hưởng bởi áp suất. CÁC YẾU TỐ ẢNH HƯỞNG ĐẾN ĐỘ TAN • Định luật Henry: Nếu S k là độ tan của chất khí A, k là hằng số, P k là áp suất riêng phần của A: • – Hằng số Henry, phụ thuộc bản chất quá trình, đơn vị là l.atm/mol, atm/(N A ) hoặc Pa.m 3 /mol. • Một số giá trị của k: – Oxygen (O 2 ) : 769.2 l.atm/mol – Carbon dioxide (CO 2 ) : 29.4 l.atm/mol – Hydrogen (H 2 ) : 1282.1 l.atm/mol kk kPS Equation: Dimension: O2 769.23 1.3 E-3 4.259 E4 H2 1282.05 7.8 E-4 7.099 E4 CO2 29.41 3.4 E-2 0.163 E4 N2 1639.34 6.1 E-4 9.077 E4 He 2702.7 3.7 E-4 14.97 E4 Ne 2222.22 4.5 E-4 12.30 E4 Ar 714.28 1.4 E-3 3.955 E4 CO 1052.63 9.5 E-4 5.828 E4 Ảnh hưởng của nhiệt độ • Áp suất hơi của mỗi cấu tử i trong dung dịch loãng phụ thuộc vào áp suất riêng và phần mol của nó trong dung dịch. • Nhắc lại định luật Dalton trong hỗn hợp khí: Định luật Raoult 0 iii PNP total PNP AA • P0 i là áp suất hơi của cấu tử tinh khiết. • Ni là phần mol của cấu tử i trong dung dịch. 0 ii i solution PNP •Định luật Raoult không đúng khi lực hút dung môi – dung môi và chất tan – chất tan lớn hơn lực hút chất tan – dung môi trong dung dịch. • Tại điểm sôi của chất lỏng tinh khiết, áp suất hơi của dung dịch sẽ < 1atm . Do đó, cần nhiệt độ cao hơn để đạt áp suất hơi 1 atm cho dung dịch ( T S ). Ta có: • K S là hằng số, phụ thuộc bản chất dung môi. ĐỘ TĂNG NHIỆT ĐỘ SÔI mSS CKT ĐỘ HẠ NHIỆT ĐỘ ĐÔNG ĐẶC Độ hạ nhiệt độ đông đặc được định nghĩa: T đ = K đ .C m Bảng K đ và K s cho dưới đây của một số dung môi. Solvent Boiling Point (°C) Kb (°C/(mol kg -1)) Freezing Point (°C) Kf (°C/(mol kg -1)) Aniline 184.3 3.69 –5.96 –5.87 Acetic Acid 118.1 3.07 16.6 –3.90 Benzene 80.1 2.65 5.5 –4.90 Carbon Disulfide 46.2 2.34 –111.5 –3.83 Carbon Tetrachloride 76.8 4.88 –22.8 –29.8 Chloroform 61.2 3.88 –63.5 –4.90 Cyclohexane 80.74 2.79 6.55 –20.2 Diethyl Ether 34.5 2.16 –116.2 –1.79 Ethanol 78.4 1.19 –114.6 –1.99 Formic acid 101.0 2.4 8.0 –2.77 Nitrobenzene 210.8 5.24 5.7 –7.00 Phenol 181.75 3.60 43.0 –7.27 Water 100.00 (exact) 0.52 0.0 –1.86 • Là sự di chuyển của dung môi từ dung dịch có nồng độ cao đến dung dịch có nồng độ thấp thông qua màng bán thẩm. • Màng bán thẩm: Chỉ cho một số cấu tử của dung dịch đi qua. Ví dụ màng tế bào. • Màng bán thẩm có thể cho cấu tử chuyển qua theo 2 hướng. • Khi dung môi chuyển động qua màng, mức dung dịch mất cân bằng. Sự thẩm thấu • Áp suất thẩm thấu, , là áp suất cần thiết để chống lại sự thẩm thấu: • Quá trình thẩm thấu là quá trình tự xảy ra. Áp suất thẩm thấu (Định luật van’t Hoff) RTC RT V n nRTV M
File đính kèm:
 bai_giang_hoa_dai_cuong_chuong_11_dung_dich_long_huynh_ky_ph.pdf
bai_giang_hoa_dai_cuong_chuong_11_dung_dich_long_huynh_ky_ph.pdf

