Bài giảng Hóa đại cương: Cân bằng hóa học - Nguyễn Minh Kha
Nhận xét về trạng thái cân bằng hoá học
Trạng thái cbhh là trạng thái cân bằng động.
Trạng thái cân bằng ứng với Gpư= 0 . (A’=0)
Dấu hiệu của trạng thái cân bằng hoá học:
Tính bất biến theo thời gian
Tính linh động
Tính hai chiều

Trang 1
Trang 2

Trang 3
Trang 4

Trang 5

Trang 6

Trang 7

Trang 8

Trang 9
Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa đại cương: Cân bằng hóa học - Nguyễn Minh Kha", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa đại cương: Cân bằng hóa học - Nguyễn Minh Kha

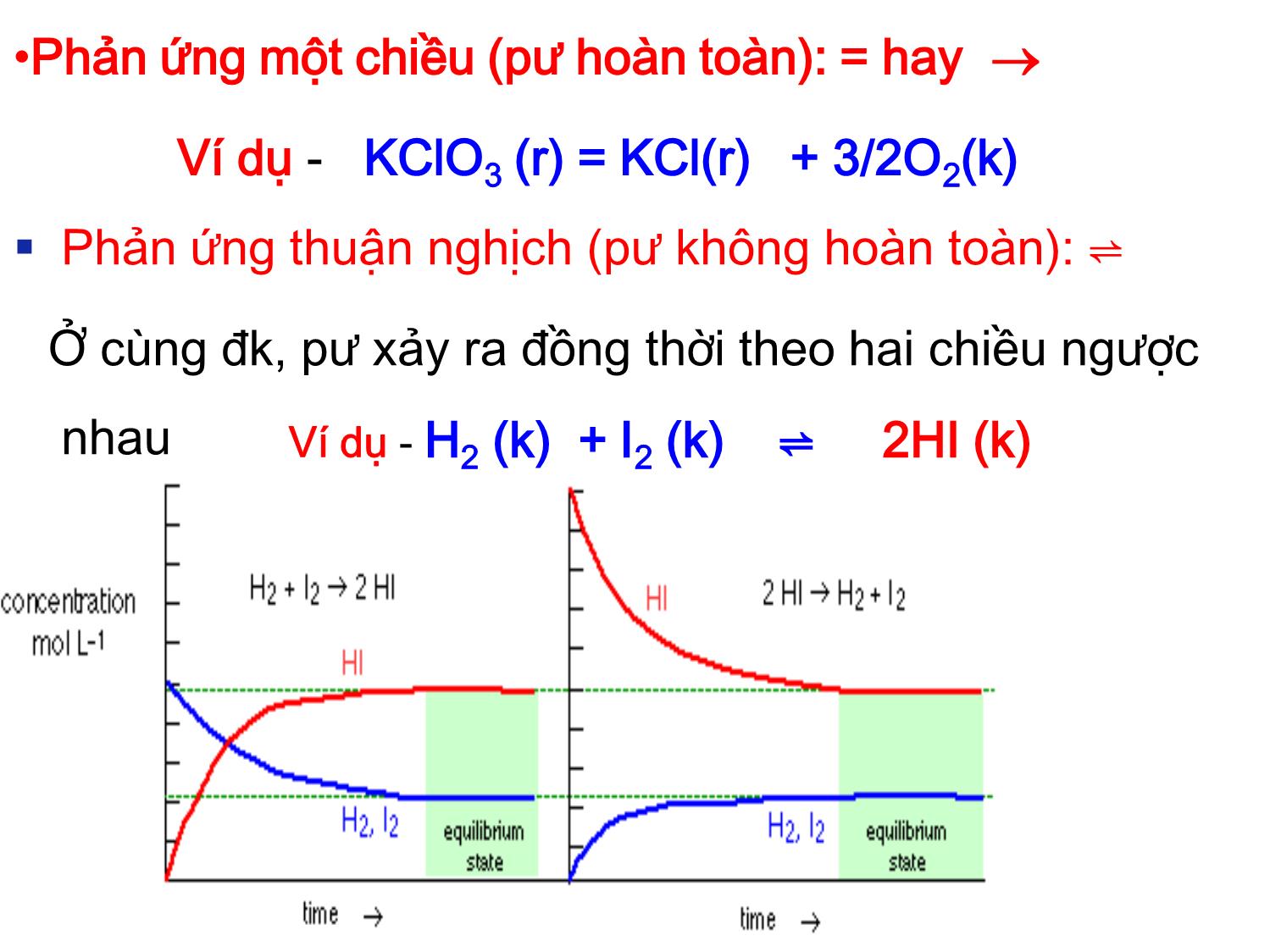
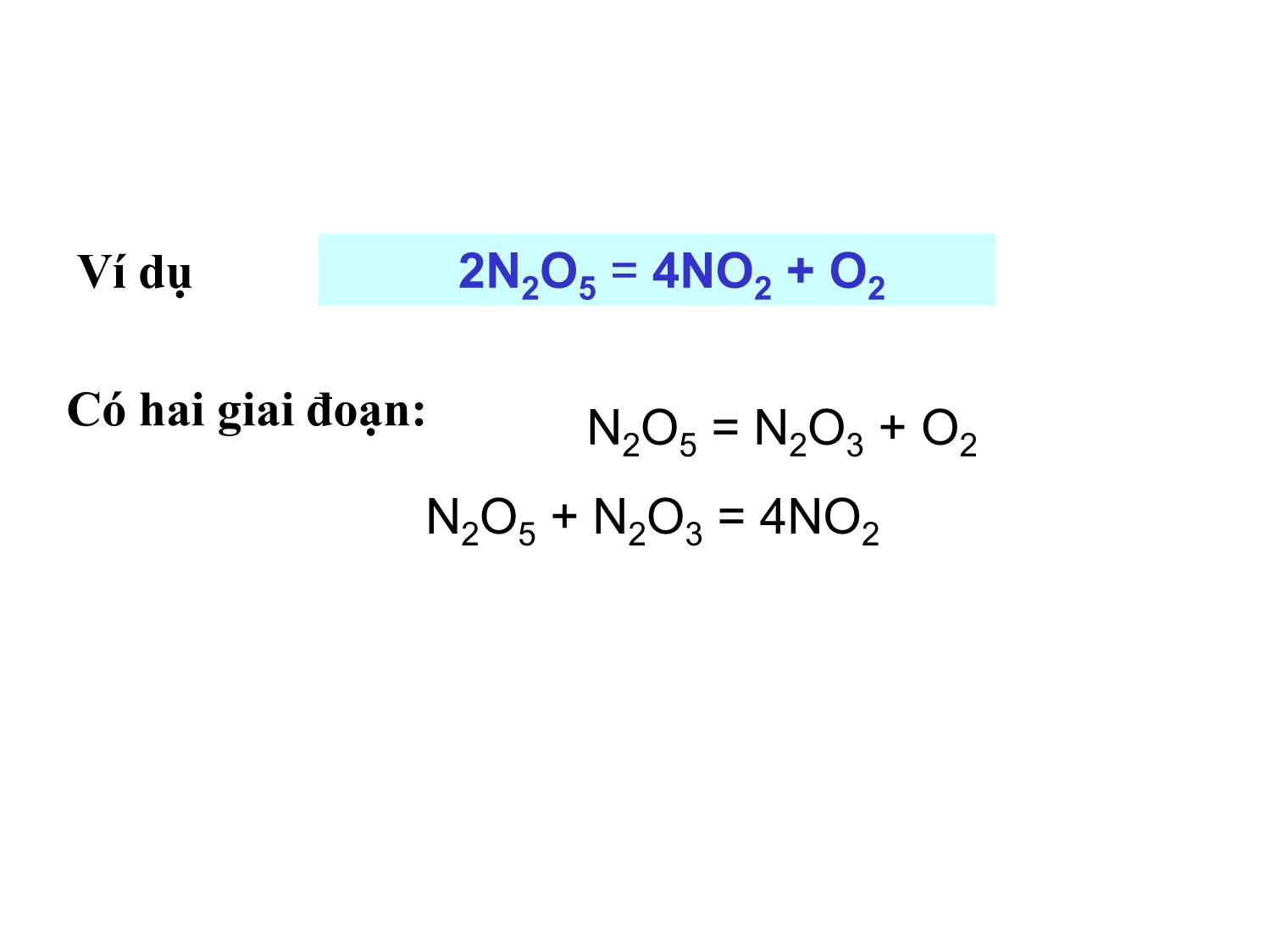
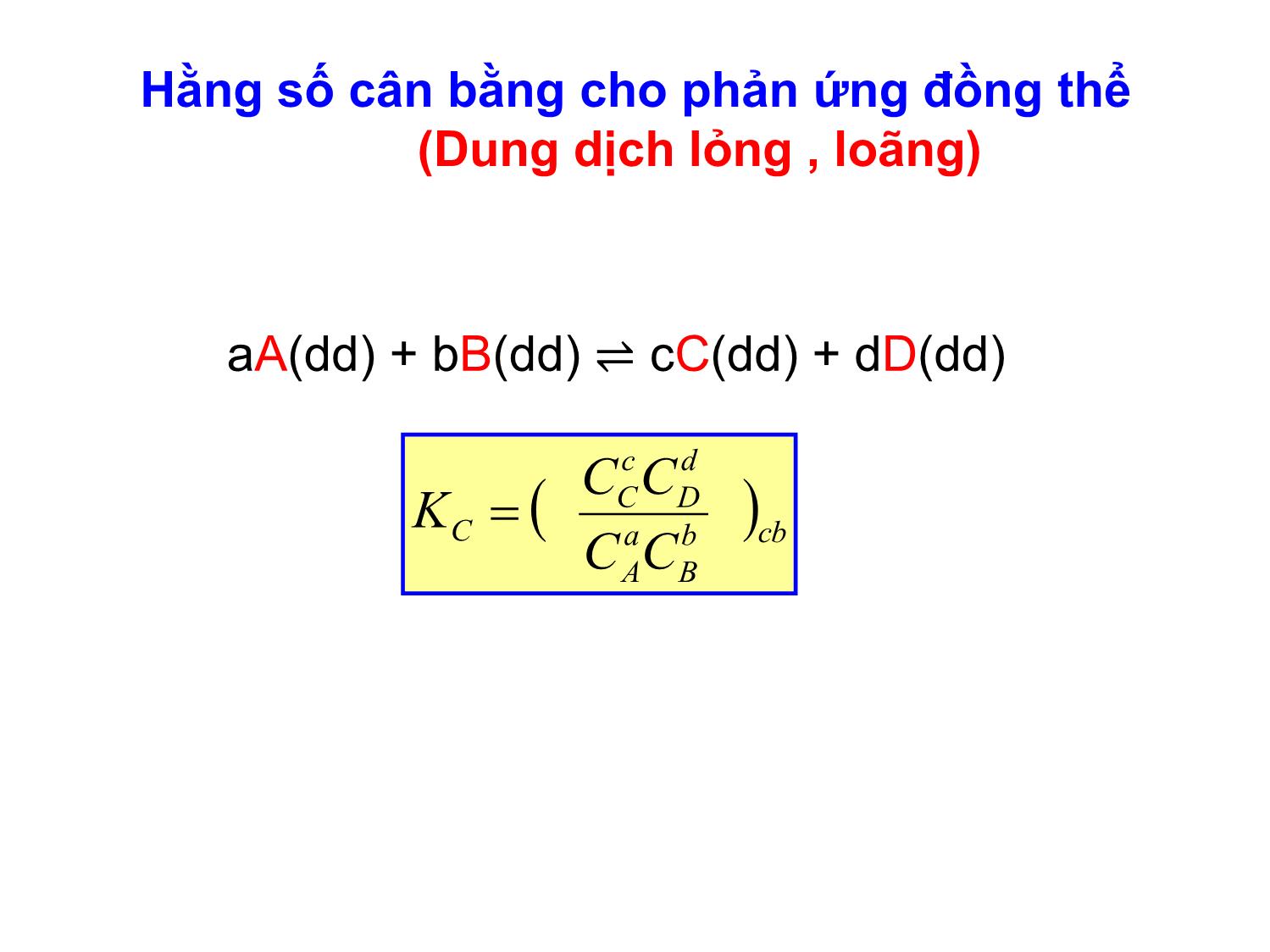
Chương VI CÂN BẰNG HÓA HỌC Giảng viên: ThS. Nguyễn Minh Kha Phản ứng thuận nghịch (pư không hoàn toàn): ⇌ Ở cùng đk, pư xảy ra đồng thời theo hai chiều ngược nhau Ví dụ - H2 (k) + I2 (k) ⇌ 2HI (k) •Phản ứng một chiều (pư hoàn toàn): = hay Ví dụ - KClO3 (r) = KCl(r) + 3/2O2(k) Phản ứng đồng thể - pư trong thể tích 1 pha HCl(dd) + NaOH(dd) = NaCl (dd) + H2O(l) Phản ứng dị thể -pư diễn ra trên bề mặt phân chia pha Zn (r) + 2HCl (dd) = ZnCl2(dd) + H2(k) Phản ứng đơn giản - pư diễn ra qua 1 giai đoạn (1 tác dụng cơ bản) Ví dụ: H2(k) + I2(k) = 2HI (k) Phản ứng phức tạp – pư diễn ra qua nhiều giai đoạn ( nhiều tác dụng cơ bản) Các giai đoạn : nối tiếp , song song, thuận nghịch 2N2O5 = 4NO2 + O2 N2O5 = N2O3 + O2 N2O5 + N2O3 = 4NO2 Ví dụ Có hai giai đoạn: Định luật tác dụng khối lượng (M.Guldberg và P. Waage ) Ở nhiệt độ không đổi, pư đồng thể, đơn giản: aA + bB = cC + dD Tốc độ phản ứng : v = k.CaA.C b B Định luật tác dụng khối lượng của Guldberg- waage nghiệm đúng cho các pư đơn giản và cho từng tác dụng cơ bản của pư phức tạp. Cân bằng hóa học b B a Att CCkv d D c Cnn CCkv vt = vn 0 v vt vn Phản ứng của hệ khí lý tưởng (pư đơn giản ): aA (k) + bB(k) ⇌ cC(k) + dD(k) = 0 C0A C 0 B 0 0 (mol/l ) CA CB Cc CD vt = vn (CA)cb=const (CB)cb=const (Cc)cb=const (CD)cb =const G=0 (PA)cb=const (PB)cb=const (PC)cb=const (PD)cb =const cb Nhận xét về trạng thái cân bằng hoá học Trạng thái cbhh là trạng thái cân bằng động. Trạng thái cân bằng ứng với Gpư= 0 . (A’=0) Dấu hiệu của trạng thái cân bằng hoá học: Tính bất biến theo thời gian Tính linh động Tính hai chiều. Hệ khí lý tưởng aA(k) + bB(k) ⇌ cC(k) + dD(k) (pư đơn giản ) Khi trạng thái đạt cân bằng: vt = vn K – hằng số ở nhiệt độ xác định: hằng số cân bằng. cb d Dcb c Cncb b Bcb a At C.C.kC.C.k cbb B a A d D c C n t C CC CC k k K badc cbb B a A d D c C cbb B a A d D c C cbb B a A d D c C p RT CC CC RTCRTC RTCRTC pp pp K nCp RTKK Hằng số cân bằng cho phản ứng đồng thể Xác định K 2 NOCl(K) 2 NO(k) + Cl2(k) [NOCl] [NO] [Cl2] Ban đầu 2.00 0 0 Phản ứng +0.33 Cân bằng K [NO]2[Cl2 ] [NOCl]2 K [NO]2[Cl2 ] [NOCl]2 = (0.66)2(0.33) (1.34)2 = 0.080 - 0.66 +0.66 1.34 0.66 0.33 Hằng số cân bằng cho phản ứng đồng thể (Dung dịch lỏng , loãng) aA(dd) + bB(dd) ⇌ cC(dd) + dD(dd) cbb B a A d D c C C CC CC K Phản ứng dị pha CaCO3(r) ⇌ CaO(r) + CO2(k) RTKK cP cbCOc 2CK cb CaCO COCaO p 3 2 p pp K cbCO CaO CaCO pp 2 3 p p p KK Trong biểu thức của hằng số cân bằng K không xuất hiện các thành phần sau: chất rắn nguyên chất, chất lỏng nguyên chất, dung môi. Mg(OH)2(r) ⇌ Mg 2+(dd) + 2OH-(dd) K = [Mg2+]cb .[OH -]2cb = T Mg(OH)2 - Tích số tan CH3COOH(dd) + H2O ⇌ CH3COO - (dd) + H3O + COOHCH COOCHOH K 3 33 a OHNH OHNH K 4 4 b Hằng số điện ly của axit NH4OH (dd) ⇌ NH4 + (dd) + OH-(dd) Hằng số điện ly của baze CH3COONa (dd) + 2H2O ⇌ CH3COOH(dd)+NaOH(dd) CH3COO- (dd) + 2H2O ⇌ CH3COOH (dd) + OH- (dd) COOCH OHCOOHCH Kt 3 3 Hằng số thuỷ phân Viết biểu thức hằng số cân bằng S(r) + O2(k) SO2(k) cb O SO p P P K 2 2 cb O SO C C C K 2 2 KP = KC S(r) + O2(k) SO2(k) K1 = [SO2] / [O2] SO2(k) +1/2 O2(k) SO3(k)K2 = [SO3] / [SO2][O2] 1/2 S(r) + 3/2 O2(k) SO3(k) K3 = ???? Thay đổi hệ số tỉ lượng S(r) + 3/2 O2(k) SO3(k) 2 S(r) + 3 O2(k) 2 SO3(k) 2 3 2 3 1 cb cb O SO K 32 2 3 2 cb cb O SO K K2 = K1 2 Đổi chiều phản ứng S(r) + O2(k) SO2(k) SO2(k) S(r) + O2(k) Kthuận = 1/Knghịch cb cb O SO K 2 2 1 12 2 2 1 KSO O K cb cb Quan hệ giữa hằng số cân bằng và G Phản ứng dị pha : aA + bB ⇌ cC + dD K Q RTQRTGG TT lnln 0 ba dc BA DC Q cb ba dc cb BA DC QK Chất khí lý tưởng [] → P (atm)/P0(1atm) Dung dịch loãng [] → C (mol/l)/C0(1mol/l) Rắn nc, lỏng nc, dung môi (H2O) → 1 Quan hệ giữa hằng số cân bằng và G PHẢN ỨNG ĐỒNG THỂ Khí lý tưởng aA + bB ⇌ cC + dD c c P P P 0 Tb B a A d D c C0 TT K Q lnRT K Q lnRTQlnRTG pp pp lnRTGG Khi phản ứng đạt trạng thái cân bằng: GT = 0 p cb b B a A d D c C T KRT pp pp RTG lnln0 Dungdịch lỏng,loãng c c c 0 Tb B a A d D c C0 TT K Q lnRTQlnRTG CC CC lnRTGG Khi phản ứng đạt trạng thái cân bằng: GT = 0 C cb b B a A d D c C T KRT CC CC RTG lnln0 Kp = f(bc pư, T) Kp f(C) KQ lnRTGT Nếu Q < K → G < 0 → phản ứng xảy ra theo chiều thuận Nếu Q > K → G > 0 → phản ứng xảy ra theo chiều nghịch Nếu Q = K → G = 0 → hệ đạt trạng thái cân bằng Ví dụ : Tính hằng số cân bằng của phản ứng: 2 NO2(k) ↔ N2O4(k) ở 298K khi biết Giải: KJvàkJH pu /6,176S 040,58 0 298pu 0 298 NHẬN XÉT về Kp và Kc Là hằng số ở nhiệt độ nhất định, chỉ phụ thuộc vào bản chất pư và nhiệt độ, chứ không phụ thuộc vào nồng độ hoặc áp suất riêng phần của chất pư Phụ thuộc vào cách thiết lập các hệ số trong ptpư. Hằng số cân bằng Kp ,Kc không có thứ nguyên. Hằng số cân bằng không phụ thuộc vào chất xúc tácHằng số cân bằng có giá trị càng lớn thì hiệu suất pư càng cao. Quan hệ của Kp với nhiệt độ và nhiệt phản ứng ooo STHG p o KRTG ln 0 2 0 2ln R S RT H K 0 1 0 1ln R S RT H K 21 0 1 2 11ln TTR H K K Ví dụ NO(k) + ½ O2(k) ⇌ NO2(k) Tính Kp ở 325 0C? Biết: H0 = -56,484kJ và Kp = 1,3.10 6 ở 250C Nguyên lý chuyển dịch cân bằng Le Chatelier Phát biểu: Một hệ đang ở trạng thái cân bằng mà ta thay đổi một trong các thông số trạng thái của hệ (nồng độ, nhiệt độ, áp suất) thì cân bằng sẽ dịch chuyển theo chiều có tác dụng chống lại sự thay đổi đó. Henri LeChâtelier (1850-1936) n =0 áp suất chung không ảnh hưởng đến trạng thái cân bằng. N2(k) + 3H2(k) ⇌ 2NH3(k) ; H<0 [N2] ↑ [NH3] ↓ cân bằng chuyển dịch theo chiều thuận cân bằng chuyển dịch theo chiều thuận P ↑ cân bằng chuyển dịch theo chiều thuận T ↓ cân bằng chuyển dịch theo chiều thuận Chuyển dịch cân bằng Co(H2O)6 2+ + 4Cl- ⇌ CoCl42- +6 H2O Hpư >0 Làm lạnh Đun nóng V=1lit , SnO2(r) + 2H2(k) ⇌ 2H2O(k) + Sn (l) G1100 = 0; 0,1mol 0,316 mol 1 mol 1mol 1)Tính Kc, KP ở 1100K 2) Tính ( G01100)pư và xác định chiều pư khi: SnO2(r) + 2H2(k) ⇌ 2H2O(k) + Sn (l) V= 1 lit ; 0,01 mol 0,1 mol 0,1 mol 1mol 3)Cân bằng sẽ chuyển dịch về phía nào trong các trường hợp Tăng nhiệt độ.Cho biết Kp= 1,5 ở 900K. Tăng thể tích bình phản ứng lên 10 lần.
File đính kèm:
 bai_giang_hoa_dai_cuong_can_bang_hoa_hoc_nguyen_minh_kha.pdf
bai_giang_hoa_dai_cuong_can_bang_hoa_hoc_nguyen_minh_kha.pdf

