Bài giảng Hóa đại cương: Điện hóa học - Nguyễn Minh Kha
PHẢN ỨNG OXY HÓA – KHỬ VÀ DÒNG ĐIỆN
Phản ứng oxy hóa – khử (O – K)
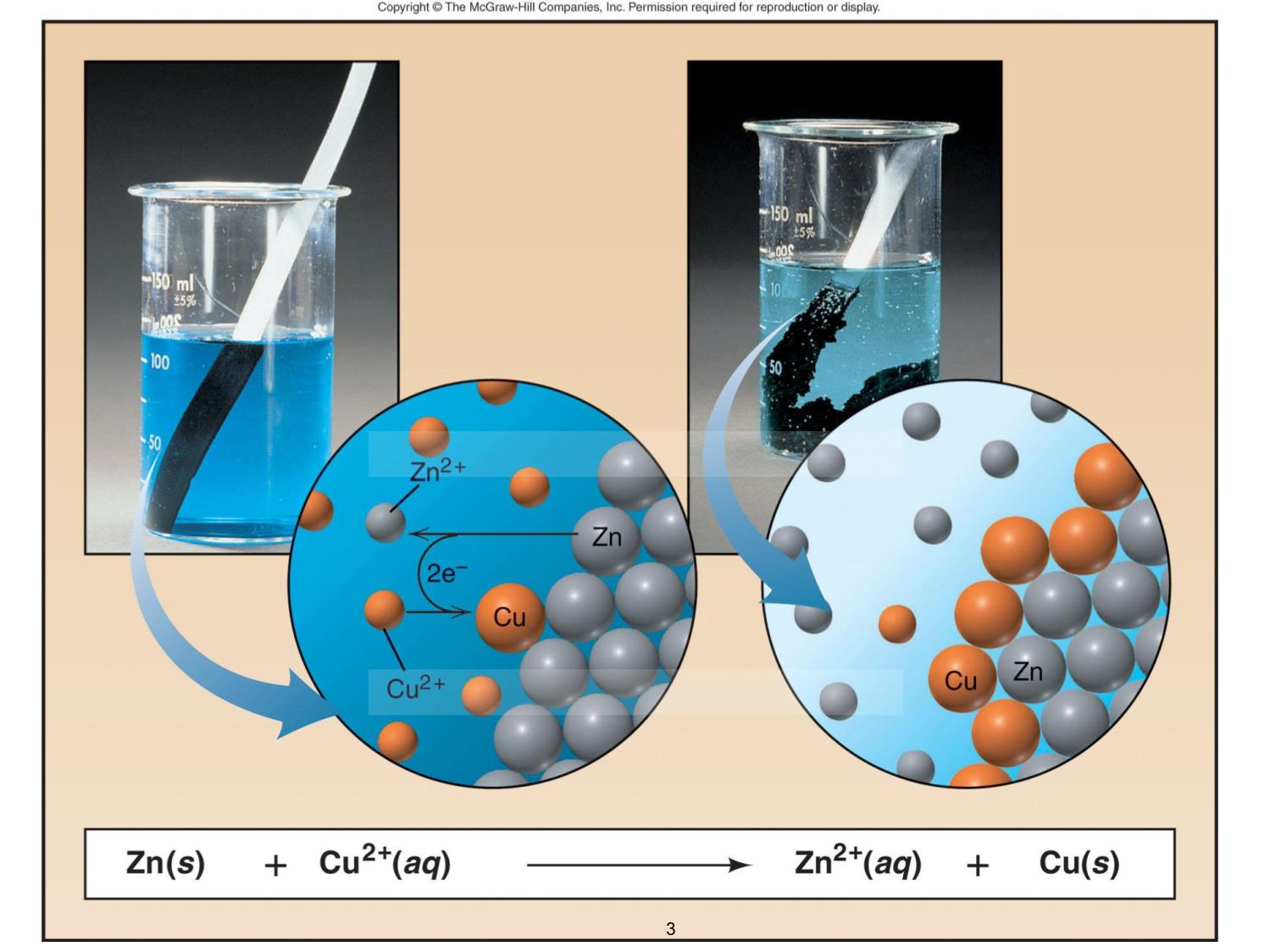
Phản ứng trong đó có sự trao đổi electron
giữa các nguyên tử của những nguyên tố
tham gia phản ứng làm thay đổi số oxy hóa
các nguyên tố

Trang 1

Trang 2
Trang 3

Trang 4

Trang 5

Trang 6

Trang 7

Trang 8

Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa đại cương: Điện hóa học - Nguyễn Minh Kha", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa đại cương: Điện hóa học - Nguyễn Minh Kha

Chương XIII ĐIỆN HĨA HỌC Giảng viên: ThS. Nguyễn Minh Kha 1 PHẢN ỨNG OXY HÓA – KHỬ VÀ DÒNG ĐIỆN Phản ứng oxy hóa – khử (O – K) Phản ứng trong đó có sự trao đổi electron giữa các nguyên tử của những nguyên tố tham gia phản ứng làm thay đổi số oxy hóa các nguyên tố. 2 3 Quá trình cho electron gọi là quá trình oxy hóa, chất cho electron gọi là chất khử (chất bị oxy hóa). Ví dụ: Zn – 2e Zn+2 Quá trình nhận electron gọi là quá trình khử, chất nhận electron gọi là chất oxy hóa. Ví dụ: Cu +2 + 2e Cu 4 Phản ứng tổng quát: Qt oxh: Kh I Ox I + ne Qt khử: Ox II + ne Kh II Pt oxh – kh: Kh I + Ox II Ox I + Kh II Cặp oxy hóa – khử: Ox I /Kh I , Ox II /Kh II Ví dụ: Qt oxh: Zn Zn2+ + 2e Qt khử: Cu 2+ + 2e Cu Pt oxh – kh: Zn + Cu2+ → Zn2+ + Cu Pt phân tử: Zn + CuSO 4 → ZnSO 4 + Cu Cặp oxy hoá khử: Zn 2+ /Zn; Cu 2+ /Cu 5 Cân bằng phản ứng O – K Nguyên tắc 1: Tổng số electron cho của chất khử phải bằng tổng số electron chất oxy hóa nhận vào. Các bước tiến hành cân bằng. Bước 1: Xác định sự thay đổi số oxy hóa của các chất. Bước 2: Lập phương trình electron – ion, với hệ số sao cho đúng qui tắc trên. Bước 3: Thiết lập phương trình ion của phản ứng. Bước 4: Cân bằng theo hệ số tỉ lượng. 6 Ví dụ: Al + CuSO 4 Al 2 (SO 4 ) 3 + Cu Al - 3e Al+3 Cu +2 + 2e Cu 2Al + 3Cu +2 = 2Al +3 + 3Cu 2Al + 3CuSO 4 2Al 2 (SO 4 ) 3 + 3Cu X2 X3 7 Nguyên tắc 2 (môi trường acid) Đối với phản ứng O – K xảy ra trong môi trường acid nếu dạng Ox của chất Ox có chứa nhiều nguyên tử Oxy hơn dạng khử của nó thì phải thêm H + vào vế trái (dạng Ox) và thêm nước vào vế phải (dạng khử). Nếu dạng khử của chất Kh chứa ít nguyên tử Oxy hơn dạng Ox của nó thì thêm nước vào vế trái (dạng Kh) và H + vào vế phải (dạng Ox). Thiếu O bên nào, thêm H 2 O bên đó, bên kia thêm H + 8 Ví dụ: OHSOKKNOMnSOSOHKNOKMnO 242344224 9 Nguyên tắc 3: (môi trường base) Phản ứng O – K xảy ra trong môi trường base, nếu dạng Ox của chất Ox chứa nhiều Oxy hơn dạng khử thì phải thêm nước vào vế trái, OH - vào vế phải. Nếu dạng Kh của chất Kh chứa ít Oxy hơn dạng Ox của nó thì phải thêm OH - vào vế trái, nước vào vế phải. Thiếu O bên nào thêm OH - bên đó, bên kia là H 2 O. 10 Ví dụ: OHKClCrOKKOHCrClKClO 24233 11 Nguyên tắc 4: (môi trường trung tính) Phản ứng O-K trong môi trường trung tính. Nếu dạng Ox của chất Ox chứa nhiều nguyên tử Oxy hơn dạng Kh của nó thì phải thêm nước vào vế trái, OH - vào vế phải. Nếu dạng Kh của chất Kh chứa ít nguyên tử Oxy hơn dạng Ox của nó thì phải thêm nươc vào vế trái, H + vào vế phải. Thêm nước vế trái, vế phải thêm: OH - nếu qt nhận electron, H + nếu qt cho electron. 12 Ví dụ: KOHKNOMnOOHKNOKMnO 32224 13 Cách tiến hành phản ứng oxyhố khử Trực tiếp - chất OXH tiếp xúc KH Hố năng pư nhiệt năng Gián tiếp – chất OXH khơng tiếp xúc trực tiếp với chất KH Hĩa năng pư điện năng Cu(s) + 2 Ag+(aq) ---> Cu 2+(aq) + 2Ag(s) e- Chất khử e- e- Chất oxh Anode Cathode Màng ngăn NGUYÊN TỐ GALVANIC VÀ ĐIỆN CỰC Nguyên tố galvanic (1780): Là thiết bị chuyển hóa năng sang điện năng. Cấu tạo gồm hai thanh kim loại, nhúng trong dung dịch muối của nó, nối với nhau qua sợi dây dẫn kim loại. Hai thanh kim loại này một thanh có tính khử mạnh hơn (để cho e) một thanh có tính khử yếu hơn (để ion của nó nhận e). Luigi Galvani (Italia) 15 CẤU TẠO VÀ HOẠT ĐỘNG NGUYÊN TỐ GANVANIC SO4 2 - Zn2+ Mật độ e trên thanh Zn nhiều hơn thanh đồng 0(Zn2+/Zn) < 0(Cu2+/Cu) Zn2+ (dd) +2e ⇌ Zn Cu2+(dd) +2e ⇌ Cu e Zn sang Cu Zn + Cu2+ (dd) = Zn2+ (dd) + Cu 16 KÝ HIỆU NGUYÊN TỐ GANVANIC (-) Zn | Zn2+ (dd) || Cu2+(dd) | Cu (+) (-) M1| M1 n+(dd)|| M2 n+(dd)| M2 (+) Quá trình khử Catod(+) Quá trình oxyhố Anod (-) - < + Zn -2e Zn2+(dd) Cu2+(dd) +2e Cu (-) Điện cực(1)|dd(1)||dd(2)|Điện cực(2) (+) 17 a. Điện cực kim loại. d. Điện cực oxy hĩa - khử. b. Điện cực kim loại phủ muối c. Điện cực khí AgAgCl Cl-(dd) Pt ,H2 H + (dd) Pt Fe2+(dd), Fe3+dd) Zn Zn2+(dd) CÁC LOẠI ĐIỆN CỰC Zn2+(dd) +2e ⇌ Zn AgCl +1e ⇌ Ag + Cl-(dd) 2H+(dd) +2e ⇌ H2 Fe3+(dd) +1e ⇌ Fe2+(dd) ỨNG DỤNG: Lập pin trong đĩ xảy ra các phản ứng sau Cd (r) + Cu2+ (dd) = Cd2+ (dd) + Cu (r) H2(k) + Cl2(k) = 2HCl (dd) Zn (r ) + 2Fe3+ (dd) = Zn2+(dd) + 2Fe2+ (dd) 2H+(dd) + 2Hg(l) +2Cl-(dd) = H2(k) + Hg2Cl2(r) THẾ ĐIỆN CỰC Thế điện cực (V), hay còn gọi là thế Oxy hóa – Khử, hay là bán thế phản ứng, là một đại lượng không thể đo trực tiếp, mà phải so sánh với một điện cực chuẩn. Người ta chọn Hydro làm điện cực chuẩn: 2H + (dd) + 2e H 2 (k), điện cực là platinum. Quy ước: 0 H2 = 0 (V). (Thế điện cực tuyệt đối của nó ước chừng 4.4 – 4.6 V) Vậy thế điện cực là một đại lượng bằng thế hiệu của nó so với điện cực hydro tiêu chuẩn. 20 Điện cực Hydro tiêu chuẩn Pt | H2 | H +(dd) 0H + / H2 = 0 ; [H +] =1mol/l, PH2 =1atm 21 Cách xác định thế điện cực Thế điện cực của một điện cực bất kỳ bằng thế hiệu của nĩ so với điện cực Hydro tiêu chuẩn. E0 = 0đc - 0 hydro E0 = 0đc 22 0 ( Cu2+/Cu) = 0,34V 23 0( Zn2+/Zn) = - 0,76V 24 Phương trình Nernst: Kh –ne Ox, Với a là hoạt độ. Hoạt độ của các kim loại tinh khiết (và cả lỏng tinh khiết) coi như bằng 1. Với dung dịch thật (sử dụng C) ở nhiệt độ 298K, ta có (R=8.314, T=298, F=96500): Kh Ox a a nF RT ln0 ][ ][ lg 059.00 0 Kh Ox n 25 phụ thuộc vào bản chất chất tham gia quá trình điện cực ( 0, n), nhiệt độ T, nồng độ chất tham gia quá trình điện cực C. Ta có: G = -nF , hay G0 = -nF 0 Sau đây là bảng thế điện cực tiêu chuẩn của một số bán phản ứng (Thế Ox-Kh). 26 Bán phản ứng 1bar, 298K, C i = 1M 0 (V) Li+(aq) + e− → Li(s) −3.05 K+(aq) + e− → K(s) −2.93 Ba2+(aq) + 2e− → Ba(s) −2.91 Ca2+(aq) + 2e− → Ca(s) −2.76 Na+(aq) + e− → Na(s) −2.71 Mg2+(aq) + 2e− → Mg(s) −2.38 Be2+(aq) + 2e− → Be(s) −1.85 Al3+(aq) + 3e− → Al(s) −1.68 Ti3+(aq) + 3e− → Ti(s) −1.21 Mn2+(aq) + 2e− → Mn(s) −1.18 Sn(s) + 4H+ + 4e− → SnH4(g) −1.07 2 H2O(l)+2e –→H2(g)+2OH –(aq) −0.83 Zn2+(aq) + 2e− → Zn(s) −0.76 Cr3+(aq) + 3e− → Cr(s) −0.74 Fe2+(aq) + 2e− → Fe(s) −0.44 Cr3+(aq) + e− → Cr2+(aq) −0.42 Sn2+(aq) + 2e− → Sn(s) −0.13 2H+(aq) + 2e− → H2(g) 0.00 Sn4+(aq) + 2e− → Sn2+(aq) +0.15 Cu2+(aq) + e− → Cu+(aq) +0.16 SO4 2−(aq) + 4H+ + 2e− → 2H2O(l) + SO2(aq) +0.17 Cu2+(aq) + 2e− → Cu(s) +0.34 O2(g)+2H2O(l)+4e – → 4OH–(aq) +0.40 SO2(aq)+4H ++4e−→S(s)+ 2H2O +0.50 Cu+(aq) + e− → Cu(s) +0.52 I2(s) + 2e − → 2I−(aq) +0.54 27 MnO4 –(aq) + 2H2O(l) + 3e – → MnO2(s) + 4 OH –(aq) +0.59 S2O3 2− + 6H+ + 4e− → 2S(s) + 3H2O +0.60 O2(g) + 2H + + 2e− → H2O2(aq) +0.70 Fe3+(aq) + e− → Fe2+(aq) +0.77 Hg2 2+(aq) + 2e− → 2Hg(l) +0.80 Ag+(aq) + e− → Ag(s) +0.80 NO3 –(aq) + 2H+(aq) +e– → NO2(g) + H2O(l) +0.80 Hg2+(aq) + 2e− → Hg(l) +0.85 MnO4 −(aq) + H+ + e− → HMnO4 −(aq) +0.90 2Hg2+(aq) + 2e− → Hg2 2+(aq) +0.91 MnO2(s) + 4H + + e− → Mn3+(aq) + 2H2O +0.95 Br2(aq) + 2e − → 2Br−(aq) +1.09 2IO3 −(aq) + 12H+ + 10e− → I2(s) + 6H2O +1.20 ClO4 −(aq) + 2H+ + 2e− → ClO3 −(aq) + H2O +1.20 O2(g) + 4H + + 4e− → 2H2O +1.23 MnO2(s) + 4H + + 2e− → Mn2+(aq) + 2H2O +1.23 Cl2(g) + 2e − → 2Cl−(aq) +1.36 Cr2O7 2−(aq) + 14H+ + 6e− → 2Cr3+(aq) + 7H2O +1.36 MnO4 −(aq) + 8H+ + 5e− → Mn2+(aq) + 4H2O +1.51 2HClO(aq) + 2H+ + 2e− → Cl2(g) + 2H2O +1.63 MnO4 −(aq) + 4H+ + 3e− → MnO2(s) + 2H2O +1.70 H2O2(aq) + 2H + + 2e− → 2H2O +1.76 28 SỨC ĐIỆN ĐỘNG CỦA NGUYÊN TỐ GALVANIC Thế hiệu cực đại xuất hiện giữa hai cực của nguyên tố ganvanic gọi là sức điện động của nguyên tố ganvanic, khi mà nguyên tố galvanic hoạt động T – N. Kí hiệu: Sức điện động tiêu chuẩn của nguyên tố galvanic. E 0 đo ở p = 1 atm, C M (hay a) = 1; T = 298K. E 000E 29 aKh1 + bOXH2 cOXH1 + dKh2 - G = A’ = nFE b 2 a 1 d 2 c 10 OXHKh KhOXH lnRTGG b 2 a 1 d 2 c 1 OXHKh KhOXH lnRTKlnRTnFE b 2 a 1 d 2 c 1 OXHKh KhOXH ln nF RT Kln nF RT E K nF RT E ln0 G0 = -nFE0 ba dc OXHKh KhOXH nF RT EE 21 210 ln cd sp nF RT EE ln0 30 Ví dụ tính hằng số cân bằng 3324 FeCeFeCe Tính hằng số cân bằng của phản ứng: 34 CeeCe 23 FeeFe o=1.700V o=0.767V Được tạo thành bởi 2 bán phản ứng sau: 31 CHIỀU CỦA QUÁ TRÌNH O – K Xét các cặp O-K: Ox 1 /Kh 1 , Ox 2 /Kh 2 Kh 1 Ox 1 + ne , 1 Kh 2 Ox 2 + ne , 2 Khi trộn các cặp này, sẽ có phản ứng: Kh 1 + Ox 2 Ox 1 + Kh 2 Phản ứng xảy ra theo chiều thuận khi: 121212 0 nFnFEG / 32 Quy tắc xét chiều phản ứng: “Phản ứng O – K xảy ra theo chiều dạng Ox của cặp O – K có lớn hơn sẽ Ox dạng Kh của cặp O – K có nhỏ hơn”. Thực tế có thể dùng 0 để xét. Nhưng khi 0 + - 0 - bé quá thì phải tính toán trên . 33 Ví dụ với phản ứng trong nguyên tố galvanic: Zn + Cu +2 = Zn +2 + Cu Với + là của cặp Cu+2/Cu và - là của cặp Zn +2 /Zn, ta có 2 2 Cu Zn0 Zn/CuZn/Cu C C ln F2 RT EE V...E Zn/Cu 1176303370000 34 Epin = + - - = Cu - Zn 35 PIN NỒNG ĐỘ (-)Cu| Cu2+; 0,1M || 1,0M ; Cu2+ |Cu (+) C C ln nF RT E C C n E lg 059,0 ở 250C ỨNG DỤNG Khi ghép một tấm bạc trong dung dịch bão hịa AgBr và một tấm bạc khác trong dung dịch AgNO3 0,01M ta được pin nồng độ cĩ suất điện động ở 250C là 0,245V. Hãy tính tích số tan của AgBr ở 250C. 38 SỰ ĐIỆN PHÂN ĐIỆN PHÂN DUNG DỊCH CHẤT ĐIỆN LY TRONG NƯỚC Định nghĩa: Sự điện phân là quá trình O – K xảy ra trên bề mặt điện cực khi cho dòng điện một chiều đi qua dung dịch chất điện ly hoặc qua chất điện ly nóng chảy và có làm theo sự biến đổi nhiệt năng thành hóa năng. Ở đây ta xét quá trình điện phân một dung dịch chất điện ly trong nước. 39 Các quá trình Cathode Ở đây dạng Ox chính là các cation kim loại và hydro của dung dịch chất điện ly. Ta cần so sánh thế điện cực của kim loại và hydro. H2 = -0.059pH = -0.059x7 = -0.41 V Tức là ở điều kiện trung tính, H2 = -0.41 V. Nếu kl > H2 kim loại kết tủa: Phần cuối dãy. Nếu kl < H2 H 2 : Phần đầu dãy. 40 Trong môi trường acid: 2H+ + 2e H 2 Trong môi trường trung tính hay base: 2H 2 O + 2e H 2 + 2OH- Nếu kl -0.41 thì tùy vào nồng độ và điều kiện tiến hành (khoảng giữa dãy). 41 Các quá trình anode Dạng khử là anion, gốc axit và OH- của dung dịch, và tùy theo vật liệu, điện cực có thể bị ăn mòn: Có anod trơ (graphit, platin.) và anod tan (Ni..). Anode tan Hoặc anode phóng điện, hoặc hòa tan anode. Nếu kim loại anode có nhỏ hơn cặp O – K thì anode bị hòa tan. M –ne M+n Ngược lại A- hoặc OH- bị oxy hóa. 42 Anode trơ Khả năng cho electron theo thứ tự: Anion không chứa Oxy: I-, Br-, Cl-, S-2 Kế đến là OH-. 4OH - – 4e O 2 + 2H 2 O (môi trường kiềm). 2H 2 O – 4e O 2 + 4H + (môi trường acid hay trung tính). Anion chứa Oxy: SO 4 -2 , MnO 4 - , SO 3 -2 43 Một số ví dụ Điện phân CuCl 2 , anode trơ Cathode Anode 41033702 .. Cu/Cu CueCu 22 222 CleCl 44 Điện phân dung dịch K 2 SO 4 với anod trơ H+ bị khử. Cathode: Anode: SO 4 - không bị Ox, nước (OH - ) bị Ox. Hay nói khác đi đây là quá trình điện phân nước. 41.0924.2 / KK 22 2444 HOHeOH KOHOHK 22 442 OHeOH 42242 SOHSOH 45 Điện phân dung dịch nước NiSO 4 với anod Ni tan Nhưng NiSO 4 tồn tại trong môi trường acid, nên: Do đó, ở cathode Và anode 41.025.0 /2 NiNi 2281442 22 .,eHOOH NieNi 22 424222 NiSOSONiNieNi 46 Thế phân giải và quá thế Thế phân giải là thế hiệu tối thiểu cần thiết để tiến hành quá trình điện phân đã cho. Ký hiệu: E p Nói chung với những hệ T – N thì E p bằng sức điện động của nguyên tố galvanic tạo thành từ sản phẩm điện phân. Hiệu số giữa thế phân giải và sức điện động của nguyên tố galvanic tương ứng phản ứng nghịch gọi là quá thế điện phân: 0 = E p - E. 47 Định luật Faraday Lượng chất được tạo thành hay hòa tan ở điện cực khi điện phân tỉ lệ thuận với lượng điện đi qua chất điện ly. Những lượng điện bằng nhau sẽ tạo thành hay hòa tan ở điện cực khi điện phân những đương lượng như nhau của các chất. Michael Faraday 48 Công thức cho định luật m = (AIt)/(nF) hay m = (Đ A q)/F F: Hằng số Faraday bằng 96500 (coulomb) m: khối lượng chất điện phân ra. Đ A : Đương lượng gam của A. A: Nguyên tử gam của A. n: Hóa trị chất biến đổi. I: Cường độ dòng điện (Ampe) t: Thời gian điện phân (sec) 49
File đính kèm:
 bai_giang_hoa_dai_cuong_dien_hoa_hoc_nguyen_minh_kha.pdf
bai_giang_hoa_dai_cuong_dien_hoa_hoc_nguyen_minh_kha.pdf

