Xác định đồng thời aspartame và saccharin trong một số loại đồ uống bằng phương pháp sắc ký lỏng hiệu năng cao
In this research, we reported some results of simultaneous identification of aspartame and saccharin by
using High Performance Liquid Chromatography method (HPLC) and simultaneous identification the
content of aspartame and saccharin in some beverages by using HPLC. It is shown that, detection limit
and quantitative limit by HPLC for aspartame was 0,2 ppm and 0,667 ppm; for Saccharin was 0,03
ppm and 0,1 ppm; the linear concentration of aspartame ranged from 0,5 to 100 ppm, with a coefficient
R2 is 0,9997; while the linear concentration of saccharin was in a range of 0,1 to 200 ppm with the
same coefficient as aspartame. The content of aspartame and saccharin in analytical samples
fluctuated from 6,931 to 19,06 ppm and from 41,70 to 79,69ppm. The recovery of aspartame and
saccharin in analytical samples fluctuated from 90,14 to 98,75% and from 90,45 to 99,15 %.

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5
Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Xác định đồng thời aspartame và saccharin trong một số loại đồ uống bằng phương pháp sắc ký lỏng hiệu năng cao

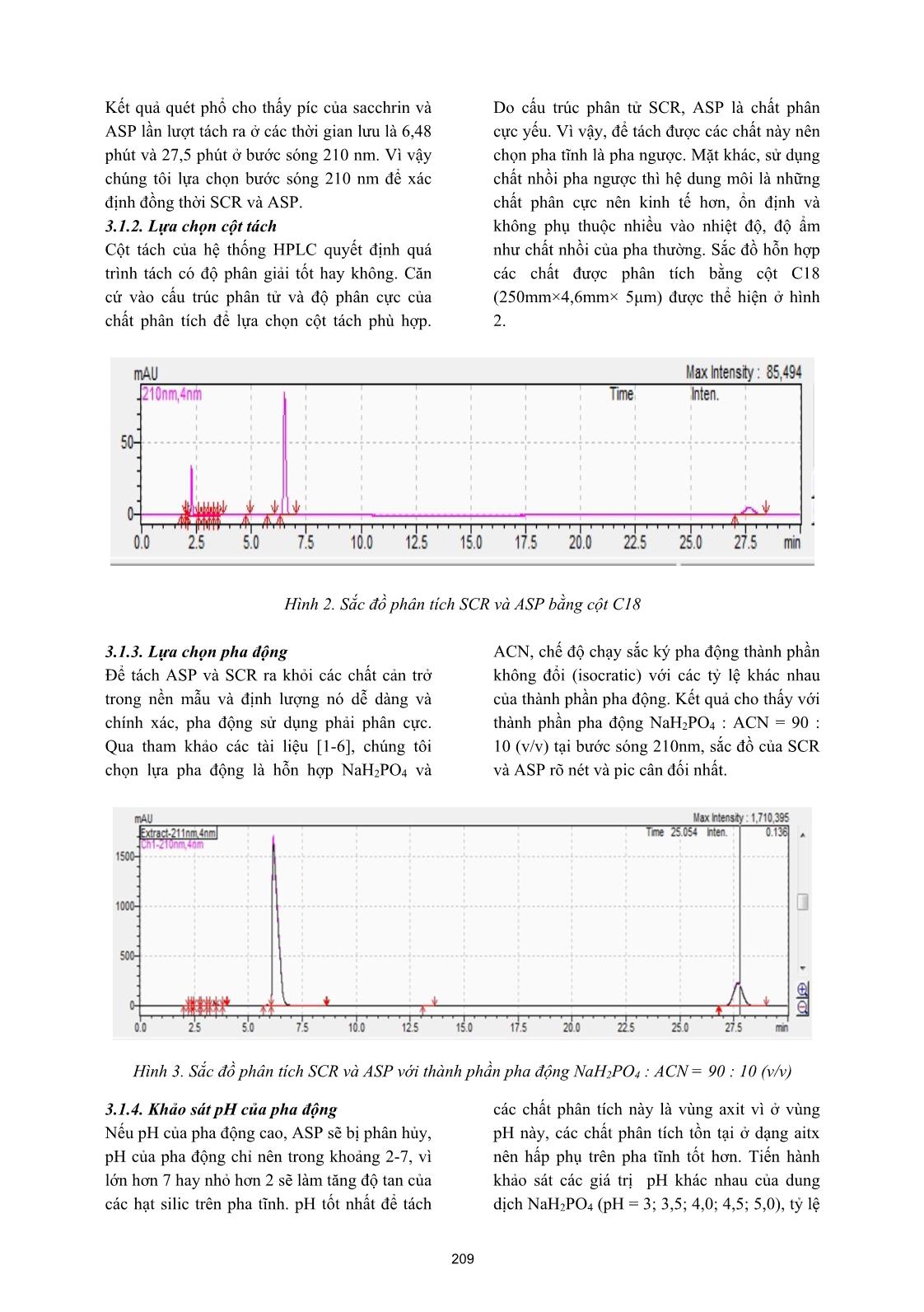
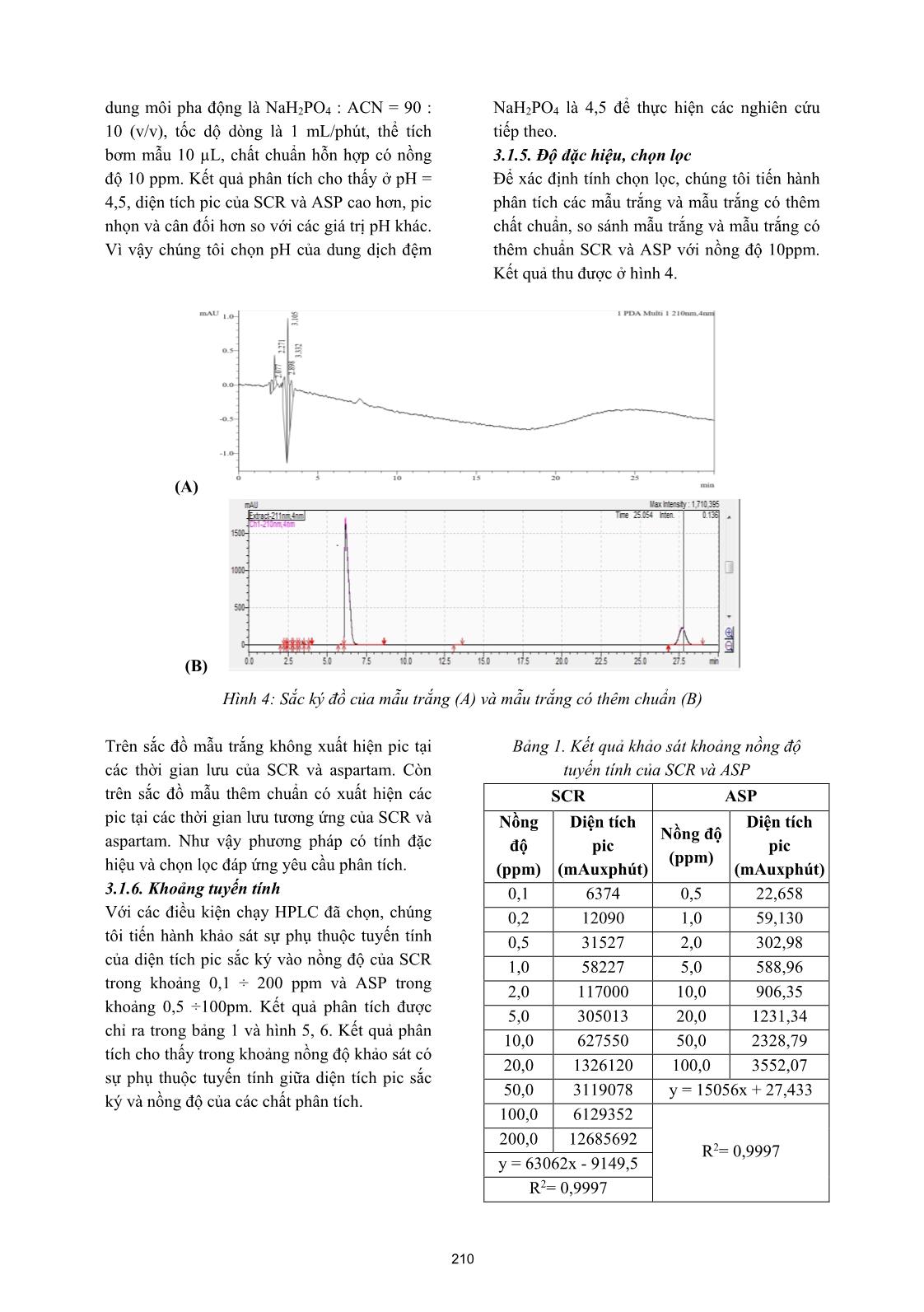
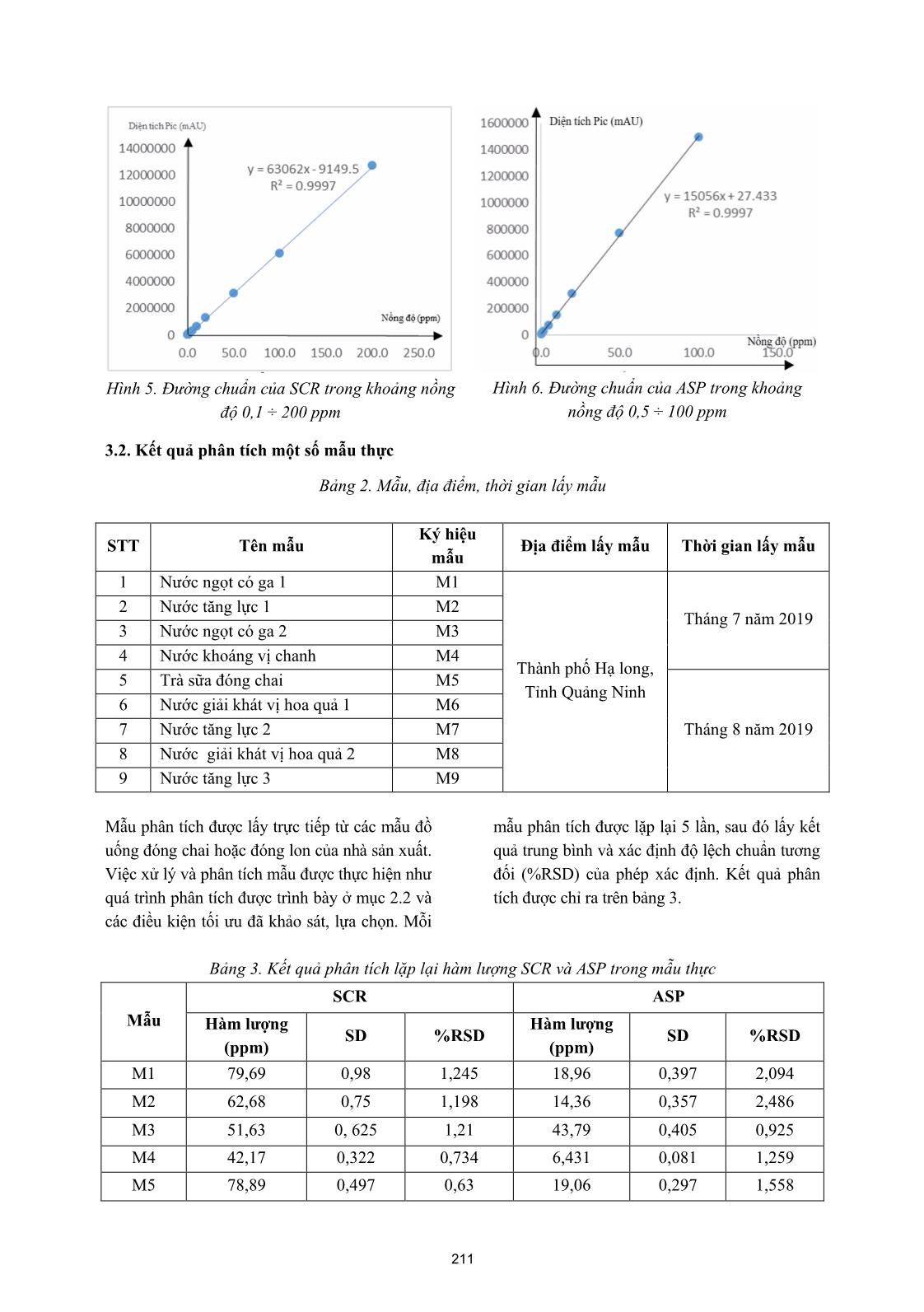
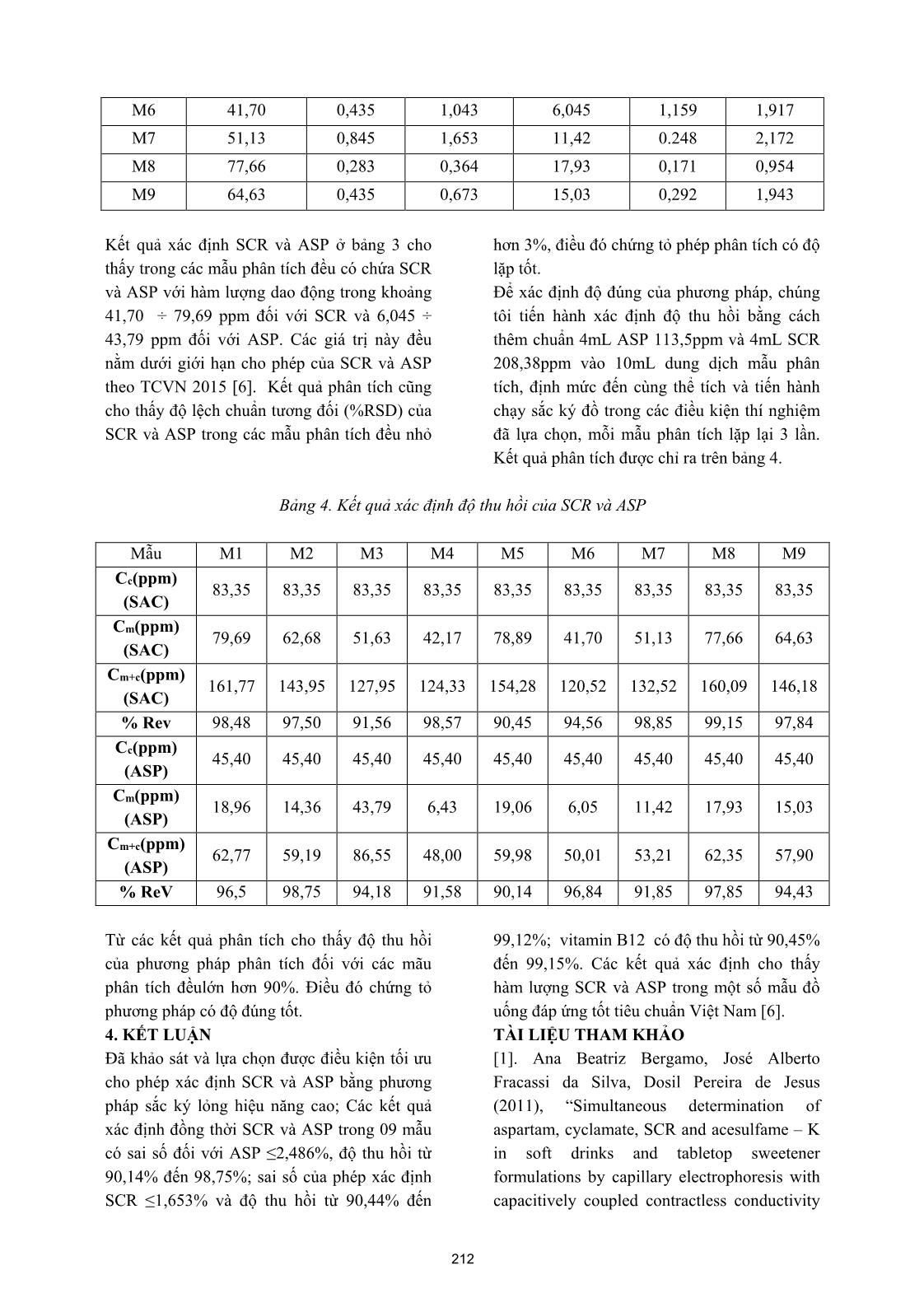
Tạp chí phân tích Hóa, Lý và Sinh học - Tập 25, Số 2/2020 XÁC ĐỊNH ĐỒNG THỜI ASPARTAME VÀ SACCHARIN TRONG MỘT SỐ LOẠI ĐỒ UỐNG BẰNG PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO Đến tòa soạn 2-12-2019 Dương Thị Tú Anh Khoa Hóa học-Trường Đại học Sư phạm - Đại học Thái Nguyên Phạm Thanh Tùng Trường THPT Cửa Ông, Thành phố Cẩm Phả, Tỉnh Quảng Ninh Đoàn Mạnh Cường Khoa Công nghệ điện tử & Truyền thông- Trường ĐHCN TT &TT- Đại học Thái Nguyên SUMMARRY SIMULTANEOUS IDENTIFICATION OF ASPARTAME AND SACCHARIN IN SOME DAILY BEVERAGES BY USING HIGH PERFORMANCE LIQUID CHROMATOGRAPHY METHOD In this research, we reported some results of simultaneous identification of aspartame and saccharin by using High Performance Liquid Chromatography method (HPLC) and simultaneous identification the content of aspartame and saccharin in some beverages by using HPLC. It is shown that, detection limit and quantitative limit by HPLC for aspartame was 0,2 ppm and 0,667 ppm; for Saccharin was 0,03 ppm and 0,1 ppm; the linear concentration of aspartame ranged from 0,5 to 100 ppm, with a coefficient R2 is 0,9997; while the linear concentration of saccharin was in a range of 0,1 to 200 ppm with the same coefficient as aspartame. The content of aspartame and saccharin in analytical samples fluctuated from 6,931 to 19,06 ppm and from 41,70 to 79,69ppm. The recovery of aspartame and saccharin in analytical samples fluctuated from 90,14 to 98,75% and from 90,45 to 99,15 %. 1. MỞ ĐẦU Asparame (ASP) là chất ngọt rất được ưa chuộng. ASP cũng không ổn định trong các dung dịch nước và dần dần chuyển thành diketopiperazine (DKP). Ngay sau khi được con người tiêu thụ, ASP phân hủy thành 3 hợp chất hóa học: phenylalanine (khoảng 50% trọng lượng), aspartic acid (40%), và methanol (10%). Những chất này có thể tồn tại trong gan, thận và não trong một thời gian khá dài. Các tác dụng phụ thường gặp khi sử dụng ASP bao gồm đau đầu, đau nửa đầu, rối loạn tâm lý, chóng mặt và xuất hiện các cơn hưng cảm. Saccharin (SCR) là một chất phụ gia tạo ngọt nhân tạo, nó được sử dụng để làm ngọt các sản phẩm như đồ uống giải khát, kẹo, bánh bích quy, thuốc chữa bệnh, kem đánh răng; là chất làm ngọt chính trong các loại thuốc dùng cho trẻ em, bao gồm aspirin nhai, xi-rô ho, các loại thuốc kê đơn và không kê đơn khác, ngoài ra nó còn được sử dụng trong cả những sản phẩm mỹ phẩm, vitamin và dược phẩm. Sử dụng SCR làm xuất hiện chứng nhạy cảm ánh sáng, buồn nôn, rối loạn tiêu hóa, nhịp tim nhanh và một số loại ung thư. Tuy nhiên tất cả những biến chứng do việc sử dụng SCR vẫn còn là một tranh cãi và chưa có kết luận nào thực sự có tính thuyết phục. Việc sử dụng ASP và SCR quá liều lượng hoặc không đúng cách sẽ gây ảnh hưởng lớn tới sức khỏe con người. Chính bởi vậy, việc kiểm soát hàm lượng ASP và SCR trong các mẫu thực 207 phẩm nói chung cũng như mẫu đồ uống nói riêng là rất cần thiết. Có rất nhiều phương pháp phân tích đã được nghiên cứu và áp dụng để xác định hàm lượng ASP và SCR trong thực phẩm như phương pháp trắc quang, phương pháp chuẩn độ thể tích, phương pháp điện di mao quản, phương pháp sắc ký lỏng hiệu năng cao [1- 6]. Trong bài báo này, chúng tôi thông báo kết quả xác định đồng thời ASP và SCR trong một số loại đồ uống bằng phương pháp sắc ký lỏng hiệu năng cao. 2. THỰC NGHIỆM 2.1. Thiết bị và hóa chất Thiết bị Máy sắc ký lỏng hiệu năng cao HPLC - hãng Shimadzu (Nhật bản) kết nối máy tính, Detector DAD, cột C18 (250 mm x 4,6 mm x 5µm); bể rung siêu âm (wise clean): Daihan, Máy ly tâm: HermLe, Z300 WUC-A10H; Cân phân tích Scientech SA 210 độ chính xác 0,0001g; Máy đồng nhất mẫu: IKA, T25 BASIC ULTRA-TURRAX; Máy đo pH và các dụng cụ thủy tinh khác. Hóa chất Chất chuẩn gốc riêng rẽ thuộc hãng Sigma: SCR 99,95%, ASP 99,85%. Các hóa chất khác: K4[Fe(CN)6].3H2O (merk), ZnSO4.7H2O (merk), NaH2PO4 (merk), H3PO4 (merk), Acetonitril (merk), Methanol (MeOH,merck) Dung môi pha mẫu: dung dịch đệm photphat (pH =4,5): dung dịch axetonitril (ACN) tỉ lệ 90:10 về thể tích. 2.2. Quá trình phân tích Lấy 5 ÷ 10 mL mẫu lỏng vào ống ly tâm; thêm 5mL MeOH, lắc đều trên máy lắc votex, thêm 30 mL nước cất, rung siêu âm 30 phút. Sau đó, chuyển toàn bộ lượng mẫu vào bình định mức 100 mL, thêm 2 mL dung dịch carrez 1 (15g K4[Fe(CN)6].3H2O trong 100 mL nước cất), lắc đều, tiếp tục thêm 2 mL dung dịch carrez 2 (30g ZnSO4.7H2O trong 100 mL nước cất), lắc đều, định mức đến vạch bằng nước cất 2 lần rồi lọc qua giấy lọc băng xanh. Dung dịch thu được tiếp tục được lọc qua màng lọc whatman 0,45 µm và định lượng bằng phương pháp HPLC với detector DAD ở bước sóng 210nm, dựa vào thời gian lưu, diện tích pic để định tính và định lượng chất phân tích. 3. KẾT QUẢ VÀ THẢO LUẬN 3.1. Khảo sát các điều kiện phân tích 3.1.1. Lựa chọn detector và xác định bước sóng hấp thụ cực đại Detector là một bộ phận quan trọng quyết định độ nhạy của phương pháp. SCR và ASP có khả năng hấp thụ ánh sáng trong vùng tử ngoại rất tốt do trong cấu tạo phân tử của các chất phân tích này đều có liên kết π . Vì vậy, detector DAD và detector UV đều có thể được sử dụng cho việc định tính và định lượng SCR và ASP, song detector DAD cho phép đo đồng thời tại nhiều bước sóng (đo phổ UV) trong quá trình sắc ký. Để thuận lợi cho quá trình phân tích chúng tôi lựa chọn detector DAD khi thực hiện các nghiên cứu tiếp theo. Xác định bước sóng hấp thụ cực đại của SCR và ASP: sử dụng detector DAD để quét tìm, với khoảng quét phổ là 190 ÷ 400 nm. Nồng độ của SCR và ASP là 10 ppm. Hình ảnh quét phổ của SCR và ASP thể hiện ở hình 1. Hình 1. Sắc ký đồ của của SCR và ASP 208 Kết quả quét phổ cho thấy píc của sacchrin và ASP lần lượt tách ra ở các thời gian lưu là 6,48 phút và 27,5 phút ở bước sóng 210 nm. Vì vậy chúng tôi lựa chọn bước sóng 210 nm để xác định đồng thời SCR và ASP. 3.1.2. Lựa chọn cột tách Cột tách của hệ thống HPLC quyết định quá trình tách có độ phân giải tốt hay không. Căn cứ vào cấu trúc phân tử và độ phân cực của chất phân tích để lựa chọn cột tách phù hợp. Do cấu trúc phân tử SCR, ASP là chất phân cực yếu. Vì vậy, để tách được các chất này nên chọn pha tĩnh là pha ngược. Mặt khác, sử dụng chất nhồi pha ngược thì hệ dung môi là những chất phân cực nên kinh tế hơn, ổn định và không phụ thuộc nhiều vào nhiệt độ, độ ẩm như chất nhồi của pha thường. Sắc đồ hỗn hợp các chất được phân tích bằng cột C18 (250mm×4,6mm× 5μm) được thể hiện ở hình 2. Hình 2. Sắc đồ phân tích SCR và ASP bằng cột C18 3.1.3. Lựa chọn pha động Để tách ASP và SCR ra khỏi các chất cản trở trong nền mẫu và định lượng nó dễ dàng và chính xác, pha động sử dụng phải phân cực. Qua tham khảo các tài liệu [1-6], chúng tôi chọn lựa pha động là hỗn hợp NaH2PO4 và ACN, chế độ chạy sắc ký pha động thành phần không đổi (isocratic) với các tỷ lệ khác nhau của thành phần pha động. Kết quả cho thấy với thành phần pha động NaH2PO4 : ACN = 90 : 10 (v/v) tại bước sóng 210nm, sắc đồ của SCR và ASP rõ nét và pic cân đối nhất. Hình 3. Sắc đồ phân tích SCR và ASP với thành phần pha động NaH2PO4 : ACN = 90 : 10 (v/v) 3.1.4. Khảo sát pH của pha động Nếu pH của pha động cao, ASP sẽ bị phân hủy, pH của pha động chỉ nên trong khoảng 2-7, vì lớn hơn 7 hay nhỏ hơn 2 sẽ làm tăng độ tan của các hạt silic trên pha tĩnh. pH tốt nhất để tách các chất phân tích này là vùng axit vì ở vùng pH này, các chất phân tích tồn tại ở dạng aitx nên hấp phụ trên pha tĩnh tốt hơn. Tiến hành khảo sát các giá trị pH khác nhau của dung dịch NaH2PO4 (pH = 3; 3,5; 4,0; 4,5; 5,0), tỷ lệ 209 dung môi pha động là NaH2PO4 : ACN = 90 : 10 (v/v), tốc dộ dòng là 1 mL/phút, thể tích bơm mẫu 10 µL, chất chuẩn hỗn hợp có nồng độ 10 ppm. Kết quả phân tích cho thấy ở pH = 4,5, diện tích pic của SCR và ASP cao hơn, pic nhọn và cân đối hơn so với các giá trị pH khác. Vì vậy chúng tôi chọn pH của dung dịch đệm NaH2PO4 là 4,5 để thực hiện các nghiên cứu tiếp theo. 3.1.5. Độ đặc hiệu, chọn lọc Để xác định tính chọn lọc, chúng tôi tiến hành phân tích các mẫu trắng và mẫu trắng có thêm chất chuẩn, so sánh mẫu trắng và mẫu trắng có thêm chuẩn SCR và ASP với nồng độ 10ppm. Kết quả thu được ở hình 4. (A) (B) Hình 4: Sắc ký đồ của mẫu trắng (A) và mẫu trắng có thêm chuẩn (B) Trên sắc đồ mẫu trắng không xuất hiện pic tại các thời gian lưu của SCR và aspartam. Còn trên sắc đồ mẫu thêm chuẩn có xuất hiện các pic tại các thời gian lưu tương ứng của SCR và aspartam. Như vậy phương pháp có tính đặc hiệu và chọn lọc đáp ứng yêu cầu phân tích. 3.1.6. Khoảng tuyến tính Với các điều kiện chạy HPLC đã chọn, chúng tôi tiến hành khảo sát sự phụ thuộc tuyến tính của diện tích pic sắc ký vào nồng độ của SCR trong khoảng 0,1 ÷ 200 ppm và ASP trong khoảng 0,5 ÷100pm. Kết quả phân tích được chỉ ra trong bảng 1 và hình 5, 6. Kết quả phân tích cho thấy trong khoảng nồng độ khảo sát có sự phụ thuộc tuyến tính giữa diện tích pic sắc ký và nồng độ của các chất phân tích. Bảng 1. Kết quả khảo sát khoảng nồng độ tuyến tính của SCR và ASP SCR ASP Nồng độ (ppm) Diện tích pic (mAuxphút) Nồng độ (ppm) Diện tích pic (mAuxphút) 0,1 6374 0,5 22,658 0,2 12090 1,0 59,130 0,5 31527 2,0 302,98 1,0 58227 5,0 588,96 2,0 117000 10,0 906,35 5,0 305013 20,0 1231,34 10,0 627550 50,0 2328,79 20,0 1326120 100,0 3552,07 50,0 3119078 y = 15056x + 27,433 100,0 6129352 R2= 0,9997 200,0 12685692 y = 63062x - 9149,5 R2= 0,9997 210 Hình 5. Đường chuẩn của SCR trong khoảng nồng độ 0,1 ÷ 200 ppm Hình 6. Đường chuẩn của ASP trong khoảng nồng độ 0,5 ÷ 100 ppm 3.2. Kết quả phân tích một số mẫu thực Bảng 2. Mẫu, địa điểm, thời gian lấy mẫu STT Tên mẫu Ký hiệu mẫu Địa điểm lấy mẫu Thời gian lấy mẫu 1 Nước ngọt có ga 1 M1 Thành phố Hạ long, Tỉnh Quảng Ninh Tháng 7 năm 2019 2 Nước tăng lực 1 M2 3 Nước ngọt có ga 2 M3 4 Nước khoáng vị chanh M4 5 Trà sữa đóng chai M5 Tháng 8 năm 2019 6 Nước giải khát vị hoa quả 1 M6 7 Nước tăng lực 2 M7 8 Nước giải khát vị hoa quả 2 M8 9 Nước tăng lực 3 M9 Mẫu phân tích được lấy trực tiếp từ các mẫu đồ uống đóng chai hoặc đóng lon của nhà sản xuất. Việc xử lý và phân tích mẫu được thực hiện như quá trình phân tích được trình bày ở mục 2.2 và các điều kiện tối ưu đã khảo sát, lựa chọn. Mỗi mẫu phân tích được lặp lại 5 lần, sau đó lấy kết quả trung bình và xác định độ lệch chuẩn tương đối (%RSD) của phép xác định. Kết quả phân tích được chỉ ra trên bảng 3. Bảng 3. Kết quả phân tích lặp lại hàm lượng SCR và ASP trong mẫu thực Mẫu SCR ASP Hàm lượng (ppm) SD %RSD Hàm lượng (ppm) SD %RSD M1 79,69 0,98 1,245 18,96 0,397 2,094 M2 62,68 0,75 1,198 14,36 0,357 2,486 M3 51,63 0, 625 1,21 43,79 0,405 0,925 M4 42,17 0,322 0,734 6,431 0,081 1,259 M5 78,89 0,497 0,63 19,06 0,297 1,558 211 M6 41,70 0,435 1,043 6,045 1,159 1,917 M7 51,13 0,845 1,653 11,42 0.248 2,172 M8 77,66 0,283 0,364 17,93 0,171 0,954 M9 64,63 0,435 0,673 15,03 0,292 1,943 Kết quả xác định SCR và ASP ở bảng 3 cho thấy trong các mẫu phân tích đều có chứa SCR và ASP với hàm lượng dao động trong khoảng 41,70 ÷ 79,69 ppm đối với SCR và 6,045 ÷ 43,79 ppm đối với ASP. Các giá trị này đều nằm dưới giới hạn cho phép của SCR và ASP theo TCVN 2015 [6]. Kết quả phân tích cũng cho thấy độ lệch chuẩn tương đối (%RSD) của SCR và ASP trong các mẫu phân tích đều nhỏ hơn 3%, điều đó chứng tỏ phép phân tích có độ lặp tốt. Để xác định độ đúng của phương pháp, chúng tôi tiến hành xác định độ thu hồi bằng cách thêm chuẩn 4mL ASP 113,5ppm và 4mL SCR 208,38ppm vào 10mL dung dịch mẫu phân tích, định mức đến cùng thể tích và tiến hành chạy sắc ký đồ trong các điều kiện thí nghiệm đã lựa chọn, mỗi mẫu phân tích lặp lại 3 lần. Kết quả phân tích được chỉ ra trên bảng 4. Bảng 4. Kết quả xác định độ thu hồi của SCR và ASP Mẫu M1 M2 M3 M4 M5 M6 M7 M8 M9 Cc(ppm) (SAC) 83,35 83,35 83,35 83,35 83,35 83,35 83,35 83,35 83,35 Cm(ppm) (SAC) 79,69 62,68 51,63 42,17 78,89 41,70 51,13 77,66 64,63 Cm+c(ppm) (SAC) 161,77 143,95 127,95 124,33 154,28 120,52 132,52 160,09 146,18 % Rev 98,48 97,50 91,56 98,57 90,45 94,56 98,85 99,15 97,84 Cc(ppm) (ASP) 45,40 45,40 45,40 45,40 45,40 45,40 45,40 45,40 45,40 Cm(ppm) (ASP) 18,96 14,36 43,79 6,43 19,06 6,05 11,42 17,93 15,03 Cm+c(ppm) (ASP) 62,77 59,19 86,55 48,00 59,98 50,01 53,21 62,35 57,90 % ReV 96,5 98,75 94,18 91,58 90,14 96,84 91,85 97,85 94,43 Từ các kết quả phân tích cho thấy độ thu hồi của phương pháp phân tích đối với các mãu phân tích đềulớn hơn 90%. Điều đó chứng tỏ phương pháp có độ đúng tốt. 4. KẾT LUẬN Đã khảo sát và lựa chọn được điều kiện tối ưu cho phép xác định SCR và ASP bằng phương pháp sắc ký lỏng hiệu năng cao; Các kết quả xác định đồng thời SCR và ASP trong 09 mẫu có sai số đối với ASP ≤2,486%, độ thu hồi từ 90,14% đến 98,75%; sai số của phép xác định SCR ≤1,653% và độ thu hồi từ 90,44% đến 99,12%; vitamin B12 có độ thu hồi từ 90,45% đến 99,15%. Các kết quả xác định cho thấy hàm lượng SCR và ASP trong một số mẫu đồ uống đáp ứng tốt tiêu chuẩn Việt Nam [6]. TÀI LIỆU THAM KHẢO [1]. Ana Beatriz Bergamo, José Alberto Fracassi da Silva, Dosil Pereira de Jesus (2011), “Simultaneous determination of aspartam, cyclamate, SCR and acesulfame – K in soft drinks and tabletop sweetener formulations by capillary electrophoresis with capacitively coupled contractless conductivity 212 detection”, Food Chemistry, 124, pages 1714- 1717. [2]. Agata Zygler, Andrzej Wasik, Agata Kot- Wasik, Jacek Namieśnik (2011), “Determination of nine high-intensity sweeteners in various foods by high- performance liquid chromatography with mass spectrometric detection”, Anal Bioanal Chem, 400:2159–2172. [3]. Chui-Shiang Chang , Tai Sheng Yeh (2014), “Detection of 10 sweeteners in various foods by liquid chromatography/tandem mass spectrometry”, Journal of food and drug analysis , 22 (3) , 318 -328 [4]. Maja SERDAR, Zorka KNEŽEVIĆ (2011), “Determination of artificial sweeteners in beverages and special nutritional products using high performance liquid chromatography”, Arh Hig Rada Toksikol, 62, pages 169-173. [5]. Shah, Romina and de Jager, Lowri S. (2017), "Recent Analytical Methods for the Analysis of Sweeteners in Food: A Regulatory Perspective", Food and Drug Administration, Papers. 5. [6]. TCVN 10993 (2015), Thực phẩm-xác định đồng thời chín chất tạo ngọt bằng sắc ký lỏng hiệu năng cao sử dụng detector tán xạ bay hơi. 213
File đính kèm:
 xac_dinh_dong_thoi_aspartame_va_saccharin_trong_mot_so_loai.pdf
xac_dinh_dong_thoi_aspartame_va_saccharin_trong_mot_so_loai.pdf

