Phát hiện đột biến gen tổng hợp chuỗi nặng Beta - Myosin (MYH7) trong bệnh cơ tim phì đại
Bệnh cơ tim phì đại (BCTPĐ) là 1 bệnh tim mạch được đặc trưng bởi rối loạn sự phát triển các sợi tơ cơ của cơ tim dẫn đến phì đại bất thường cơ thất trái. Sự phì đại này có thể ở thành tâm thất trái (đồng tâm) hoặc ở vách liên thất (lệch tâm).

Trang 1

Trang 2

Trang 3
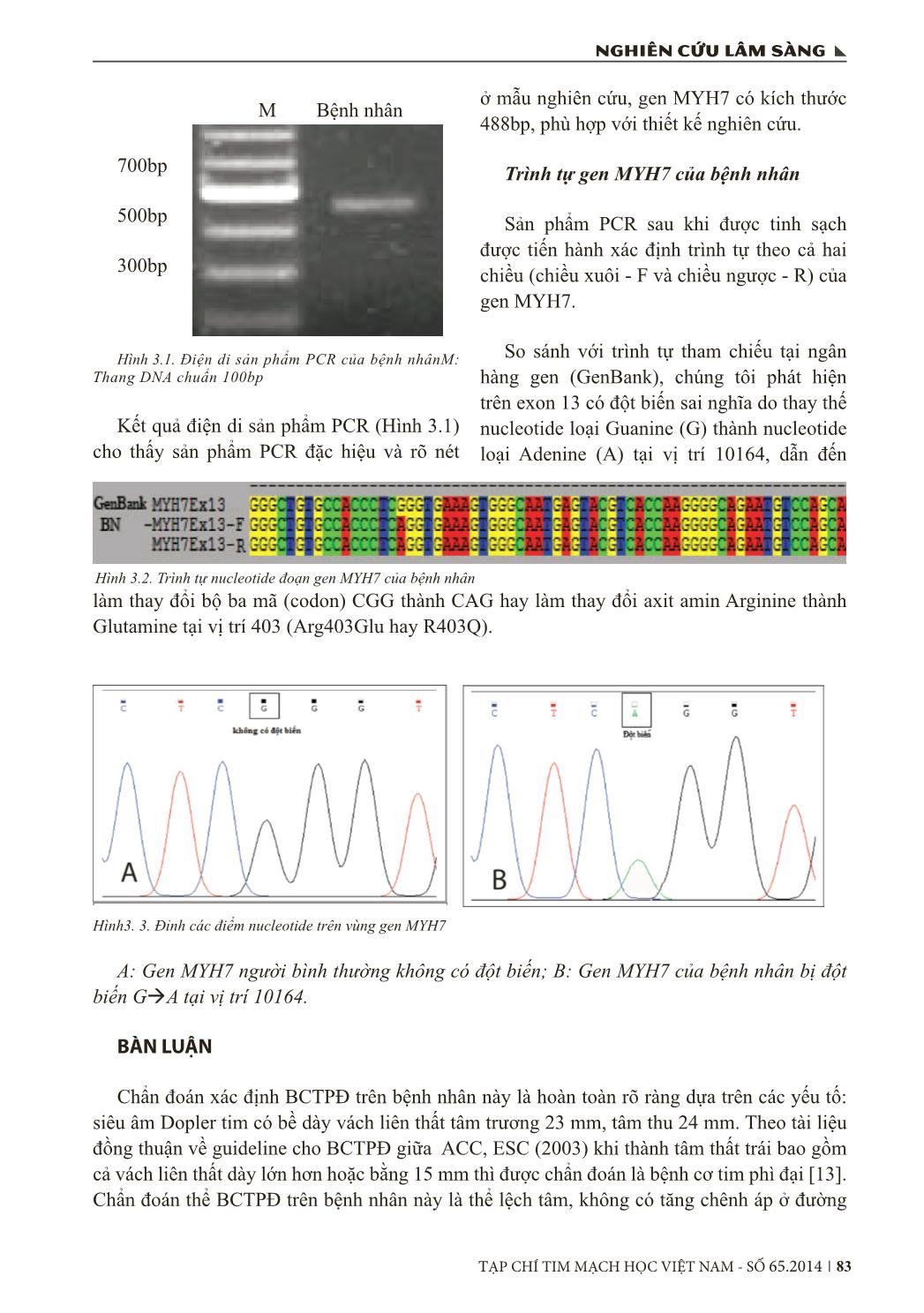
Trang 4

Trang 5

Trang 6

Trang 7

Trang 8

Trang 9
Bạn đang xem tài liệu "Phát hiện đột biến gen tổng hợp chuỗi nặng Beta - Myosin (MYH7) trong bệnh cơ tim phì đại", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Phát hiện đột biến gen tổng hợp chuỗi nặng Beta - Myosin (MYH7) trong bệnh cơ tim phì đại

Nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.201480 PHÁT HIỆN ĐỘT BIẾN GEN TỔNG HỢP CHUỖI NẶNG BETA - MYOSIN (MYH7) TRONG BỆNH CƠ TIM PHÌ ĐẠI Trương Thanh Hương, Dương Đức Hùng, Nguyễn Thị Mai Ngọc * Lương Thị Lan Anh**, Nguyễn Thị Trang** * Viện Tim mạch Việt Nam ** Bộ môn Y sinh học Di truyền, Trường Đại học Y Hà Nội TÓM TẮT Bệnh cơ tim phì đại (BCTPĐ) là 1 bệnh tim mạch được đặc trưng bởi rối loạn sự phát triển các sợi tơ cơ của cơ tim dẫn đến phì đại bất thường cơ thất trái. Sự phì đại này có thể ở thành tâm thất trái (đồng tâm) hoặc ở vách liên thất (lệch tâm). Tỷ lệ mắc bệnh ước tính khoảng 1/500-1000 người. Bệnh nhân bị BCTPĐ có nguy cơ bị các rối loạn nhịp tim như tim nhanh thất hay rung thất, có thể dẫn đến đột tử mà không có dấu hiệu báo trước. Trên các bệnh nhân BCTPĐ hoặc nghi ngờ BCTPĐ có tính chất gia đình, 50-60% trường hợp tìm thấy đột biến một trong các gen mã hoá các thành phần tạo ra sợi tơ cơ. Mục tiêu: Phát hiện đột biến gen MYH7 của bệnh nhân mắc cơ tim phì đại. Đối tượng nghiên cứu: Bệnh nhân nam, 36 tuổi, chẩn đoán BCTPĐ, có cơn choáng ngất thoảng qua. Phương pháp nghiên cứu: Phân tích gen MYH7 bằng kỹ thuật di truyền phân tử. Kết quả: Phát hiện đột biến Arg403Glu tại exon 13 của gen MYH7. Kết luận: Nhân trường hợp phát hiện đột biến Arg403Glu gen MYH7 ở bệnh nhân BCTPĐ đã làm sáng tỏ thêm về cơ chế BCTPĐ tại Việt Nam, mở thêm hướng chẩn đoán đối với BCTPĐ, giúp người thầy thuốc tầm soát bệnh tốt hơn. Từ khóa: MYH7, Cơ tim phì đại. ĐẶT VẤN ĐỀ Bệnh cơ tim phì đại (BCTPĐ) là 1 bệnh tim mạch được đặc trưng bởi rối loạn sự phát triển các sợi tơ cơ của cơ tim dẫn đến phì đại bất thường cơ thất trái. Sự phì đại này có thể ở thành tâm thất trái (đồng tâm) hoặc ở vách liên thất (lệch tâm). Tỷ lệ mắc bệnh ước tính khoảng 1/500-1000 người [1]. Bệnh nhân bị BCTPĐ có nguy cơ bị các rối loạn nhịp tim như tim nhanh thất hay rung thất, có thể dẫn đến đột tử mà không có dấu hiệu báo trước. Đây là một nguyên nhân hàng đầu dẫn đến đột tử ở các bệnh nhân dưới 35 tuổi [16]. Sự phì đại thất trái hay gặp nhất là phì đại vách liên thất, chiếm tới 46% [9], có thể có hay không kèm theo sự tắc nghẽn đường ra thất trái. Lâm sàng của bệnh nghèo nàn và thay đổi tuỳ thuộc vào tuổi phát hiện bệnh, mức độ nặng nhẹ của quá trình tiến triển bệnh. BCTPĐ có thể biểu hiện ở trẻ nhỏ mặc dù người ta thường phát hiện bệnh ở tuổi thiếu niên hoặc ở người trưởng thành [16], [9]. Những quan tâm gần đây về gen di truyền của bệnh lý này đã mở ra nhiều hướng mới trong tiên lượng, theo dõi và điều trị. Trên các bệnh nhân BCTPĐ hoặc nghi ngờ BCTPĐ có tính chất gia đình, 50-60% trường hợp tìm thấy đột biến một trong các gen mã hoá các thành phần tạo ra sợi tơ cơ. BCTPĐ nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.2014 81 được xác định tuân theo quy luật di truyền trội trên nhiễm sắc thể thường. Các nhà khoa học đã tìm thấy trên 900 đột biến thuộc 20 gen liên quan đến bệnh. Tất cả các gen đều tham gia mã hóa cấu trúc cho các protein của tế bào cơ tim. Thành phần chủ yếu của cơ tim là xơ actin và xơ myosin. Xơ myosin sắp xếp với xơ actin thành đơn vị co duỗi cơ. Trên mỗi đơn vị co duỗi cơ myosin - actin còn có gắn thêm các phân tử troponin gồm 3 tiểu đơn vị là A, C và T. Các đột biến gây BCTPĐ thường liên quan đến gen tổng hợp protein cấu tạo xơ myosin (MYH7) và troponin (TNNT, TPMA, MYBPC, TNNI3), trong số này, đột biến gen MYH7 chiếm tới 30 - 45% các trường hợp. [16], [9], [21]. Phân tích gen đột biến cho phép phát hiện và chẩn đoán những trường hợp có nguy cơ cao bị BCTPĐ trước khi có biểu hiện lâm sàng. Có đột biến gen MYH7 khẳng định chắc chắn BCTPĐ khi có các triệu chứng lâm sàng. Nếu đột biến gen được phát hiện thấy ở những bệnh nhân chưa có biểu hiện lâm sàng thì những trường hợp này bắt buộc phải theo dõi định kỳ. Ở Việt Nam, lần đầu tiên chúng tôi tiến hành nghiên cứu gen MYH7 ở các bệnh nhân BCTPĐ với mong muốn tìm hiểu mối liên quan tới việc biến đổi kiểu gen và đặc điểm lâm sàng của BCTPĐ, đồng thời dự đoán trước nguy cơ mắc bệnh cũng như tư vấn dự phòng biến cố tim mạch như rối loạn nhịp, ngất, đột tử, khả năng di truyền bệnh,Chúng tôi xin báo cáo một trường hợp BCTPĐ đã phát hiện thấy có đột biến gen MYH7. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU Đối tượng nghiên cứu: Bệnh nhân nam, 36 tuổi, nhập viện ngày 05/9/2011 vì có các cơn choáng và đau thắt ngực. Bệnh nhân có tiền sử đã được chẩn đoán BCTPĐ từ 2003, nhưng điều trị không đều. Nhưng đến 2007 ngoài đau ngực, bệnh nhân thấy khó thở khi gắng sức. Vì vậy, bệnh nhân đã chủ động đi khám và được theo dõi định kỳ và điều trị đều hàng tháng (tildiem 60 mg uống 2 viên/1 ngày). Khoảng mấy tháng trước khi nhập viện, bệnh nhân xuất hiện các cơn choáng thoáng qua. Trong gia đình bệnh nhân: Mẹ, 2 chị và anh trai cũng được chẩn đoán BCTPĐ. Bệnh nhân được thăm khám và siêu âm Doppler tim và các thăm dò chức năng khác để chẩn đoán xác định và đánh giá mức độ BCTPĐ. Bệnh nhân được lấy máu làm các xét nghiệm cận lâm sàng, đồng thời phân tích gen MYH7 tại Bộ môn Y sinh học - Di truyền, Trường Đại học Y Hà Nội. Phương pháp nghiên cứu: Thăm khám lâm sàng. Chẩn đoán hình ảnh: • Chụp tim phổi thẳng. • Siêu âm Doppler tim. Thông tim ống lớn và Chụp động mạch vành: đánh giá mức chênh áp ở đường ra thất trái, mức độ hở van hai lá, hệ động mạch vành: xét đốt vách liên thất. Xét nghiệm cận lâm sàng: Các xét nghiệm: công thức máu, sinh hóa máu • Điện tâm đồ. Nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.201482 Phân tích gen MYH7 DNA được tách chiết từ tế bào bạch cầu lympho máu ngoại vi bằng kit Phenol/ChCl3. Các exon chứa các đột biến có nguy cơ gây BCTPĐ (exon 13 và 14) được nhân lên bằng phản ứng PCR với 40 chu kì luận nhiệt (95oC- 5 phút/55oC-30 giây/72oC-30 giây). Thể tích ... thể 14, nơi chứa gen MYH7 [22]. Garcia và cs. (Úc) giải trình tự exon 13 - 16 của gen MYH7 trong 30 bệnh nhân cơ tim phì đại, trong độ tuổi từ 18 - 60, trong đó có 25 bệnh nhân có tiền sử gia đình mắc bệnh cơ tim phì đại. Trong nghiên cứu này phát hiện ở 1 bệnh nhận xuất hiện 1 đột biến (Arg453Cys, exon 14) trên gen MYH7 [6]. Villard và cs. đã phân tích tất cả các exon của hai gen MYH7 và TNNT2 sử dụng phương pháp SSCP ở 96 bệnh nhân (54 bệnh nhân có tiền sử gia đình và 42 bệnh nhân không thường xuyên mắc bệnh ). Đột biến gen MYH7 đã được xác định ở 5 bệnh nhân có tiền sử gia đình và ở 2 bệnh nhân không thường xuyên mắc bệnh. Trong nghiên cứu này đã phát hiện ra rằng hầu hết nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.2014 85 các đột biến đều ở gen MYH7 và cũng là thời điểm khởi phát bệnh bị chậm lại. Garcia và cs. nghiên cứu tần số của gen sarcomere ở 120 bệnh nhân cơ tim phì đại tại Tây Ban Nha, trong số đó, 16% có tiền sử gia đình. Họ đã nghiên cứu kiểm tra trên 5 gen và xác định được các đột biến ở 32 bệnh nhân, trong đó có 10 đột biến trên gen MYH7 [5]. Tại Iran, Montazeri và cs đã nghiên cứu các đột biến phổ biến trên gen MYH7, bao gồm exon 13-15 ở 50 bệnh nhân và xác định được đột biến G10195A trong exon 13 và một đột biến A10419C trong exon 14 [20]. Các kết quả của một vài nghiên cứu ở Iran và nghiên cứu sâu rộng trong các phần khác của thế giới về gen này với sự ảnh hưởng của chúng đến bệnh cơ tim phì đại cho rằng exon 8-24 của gen MYH7 ảnh hưởng nhiều nhất trong căn bệnh này. Một số đột biến thuộc gen MYH7 được cho là có ý nghĩa tiên lượng bởi liên quan đến nguy cơ đột tử của bệnh như Arg403Gln, Arg719Trp, Arg453Cys [1,31]. Tuy nhiên, một số trường hợp đột biến chỉ là người mang gen, không biểu hiện bệnh như: Gly256Glu, Val606Met, Leu908Val [1,29]. Nghiên cứu của Liu và cộng sự để sàng lọc các đột biến của gen có nguy cơ gây bệnh cơ tim phì đại trong 10 gia hệ ở Trung Quốc. Trong nghiên cứu này, trong 3 gia hệ đã xác định có đột biến gen MYH7, 3 bệnh nhân đã đột ngột qua đời ở tuổi 20 - 48 trong khi tập luyện thể thao. Kết quả của nghiên cứu này cho thấy các đột biến của gen MYH7 ở những bệnh nhân cơ tim phì đại có liên quan với nguy cơ đột tử cao do tim [12]. Trong một gia đình Trung Quốc gồm 3 thế hệ, Ko và cs. (1996) đã quan sát thấy sự cùng tồn tại của đột tử và suy tim giai đoạn cuối do đột biến Arg453Cys [11]. Tuổi trung bình của các thành viên bị đột tử có tính chất gia đình là 34 năm. Geisterfer-Lowrance và cs. (1990) tìm thấy một đột biến sai nghĩa trong chuỗi beta myosin ở bệnh nhân cơ tim phì đại dẫn đến làm thay thế arginine thành glutamine tại vị trí 403 (R403Q) [7]. Perryman và cs. (1992) chứng minh rằng đột biến R403Q thường gặp trên phân tử mRNA của cơ tim [23]. Radovan và cs. mô tả trường hợp trẻ tuổi BCTPĐ tắc nghẽn mang đột biến Arg403Glu tại exon 13 của gen MYH7 [24]. Spindler và cs. (1998) đã nghiên cứu ảnh hưởng của đột biến tại codon 403 của gen MYH7. Họ đã quan sát thấy 3 sự thay đổi lớn trong sinh lý học và năng lượng sinh học ở tim chuột đột biến. Đầu tiên, trong khi không bị rối loạn chức năng tâm thu, chức năng tâm trương bị suy giảm trong thời gian kích thích co bóp. Thứ hai, trong điều kiện chuột bị đột biến R403Q thì tim chuột có hàm lượng phosphocreatine thấp hơn và tăng hàm lượng phosphate vô cơ dẫn đến giảm giá trị năng lượng tự do sinh ra từ quá trình thủy phân ATP. Thứ ba, chuột bị đột biến tim đã được tăng perfusate canxi bằng cách giảm xuống 2 lần nhịp tim so với đối chứng. Các tác giả trên đã kết luận rằng tim của chuột mang đột biến R403Q đã bị phụ thuộc vào việc làm rối loạn chức năng tâm trương tương tự như biểu hiện của người bị bệnh cơ tim phì đại có tính chất gia đình [27]. Trong nghiên cứu của chúng tôi, gen MYH7 đã được kiểm tra và xác định được trên exon 13 xuất hiện đột biến sai nghĩa do thay thế nucleotide loại Guanine (G) thành nucleotide loại Adenine (A) tại vị trí 10162, dẫn đến làm thay đổi codon CGG thành CAG hay làm thay đổi axit amin Arginine thành Glutamine tại vị trí 403 (Arg403Glu hay R403Q). Việc phát hiện này giúp chúng tôi lý giải rõ hơn về biểu hiện lâm sàng của bệnh nhân, với những cơn choáng ngất thoảng qua là một trong các triệu chứng của BCTPĐ và là tiền triệu của Nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.201486 cái chết đột tử dễ xảy đến với nhóm bệnh nhân mang loại đột biến này. Đồng thời dựa vào vị trí và kiểu đột biến gen có thể giúp tiên lượng kiểu hình cũng như mức độ nặng (nguy cơ rối loạn nhịp dẫn đến đột tử ) những trường hợp BCTPĐ. Vì vậy, nếu test gen MHY7 âm tính và không có triệu chứng lâm sàng thì những trường hợp này được khẳng định chắc chắn nguy cơ mắc BCTPĐ là rất thấp mặc dù họ được sinh ra trong gia đình có tiền sử bị BCTPĐ mang đột biến gen MYH7. KẾT LUẬN Lần đầu tiện tại Việt Nam, người bệnh BCTPĐ được phân tích gen MYH7 và phát hiện được đột biến có liên quan tới biểu hiện bệnh. Mặc dù đây không phải là đột biến mới và đã được thế giới công bố, nghiên cứu của chúng tôi cho thấy đã làm sáng tỏ thêm về cơ chế BCTPĐ tại Việt Nam, mở thêm hướng chẩn đoán đối với BCTPĐ, giúp người thầy thuốc tầm soát bệnh tốt hơn. SUMMARY DETECTION OF MUTATION IN THE BETA - MYOSIN HEAVY CHAIN (MYH7) IN HYPERTROPHIC CARDIOMYOPATHY Hypertrophic cardiomyopathy (HC) is a cardiac disease characterized by a sarcomeric disarray that leads to cardiac muscle cell hypertrophy. The prevalence of HC has been estimated in 1 in 500 to 1000 persons, and HC is the most common cause of sudden death in the young. The genes involved in HC encode proteins of the sarcomere. The first HC locus was mapped to the long arm of chromosome 14 (14q1). The gene encodes the beta-myosin heavy chain (MYH7) gene, and more than 50 different mutations have been identified worldwide. Objectives: To investigate mutation on MYH7 gene. Subject: A 36 year-old male patient, history of hypertrophic cardiomyopathy. Methods: sequencing MYH7 gene, using reference and control. Results: The mutation Arg403Glu of MYH7 gene was found in HC patient. Conclusion: Our study illustrates that detection MYH7 gene mutations in HC patient has shed light on the pathogenesis of HC in Vietnam, more open diagnosis direction for HC and help doctors screening better for this disease. Key words: MYH7 gene, Hypertrophic cardiomyopathy. nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.2014 87 TÀI LIỆU THAM KHẢO 1. Ackerman MJ, VanDriest SL, Ommen SR, Will ML, Nishimura RA, Tajik AJ, Gersh BJ. Prevalence and age- dependence of malignant mutations in the beta-myosin heavy chain and troponin T genes in hypertrophic cardiomyopathy: a comprehensive outpatient perspective. J Am Coll Cardiol. 2002 Jun 19;39(12):2042-8. 2. Braunwald E, Lambrew C, Rockoff D, et al. Idiopathic hypertrophic subaortic stenosis: I. A description of the disease based upon an analysis of 64 patients. Circulation 1964;30 Suppl IV:3–217. 3. E. G. Torrecilla, M. A. Garci´a Ferna´ndez, H. Bueno, M. Moreno and J. Pulmonary venous flow in hypertrophic ardiomyopathy as assessed by the transoesophageal approach. European Heart Journal (1999) 20, 293–302. 4. Eliecer Coto1,4,5, Julián R. Reguero, Resequencing the whole MYH7 gene (including the intronic, promoter, and 3´ UTR sequences) in hypertrophic cardiomyopathy. J Mol Diagn. 2012 Sep;14(5):518-24. 5. Garcia-Castro M, Coto E, Reguero JR, et al. Mutations in sarcomeric genes MYH7, MYBPC3, TNNT2, TNNI3, and TPM1 in patients with hypertrophic cardiomyopathy. Rev Esp Cardiol 2009 Jan;62(1):48-56. 6. Garcia-Castro M, Reguero JR, Batalla A, et al. Hypertrophic cardiomyopathy: Low frequency of mutations in the β-myosin heavy chain (MYH7) and cardiac troponin t (TNNT2) genes among spanish patients. Clin Chemistry 2003; 49(8): 1279-1285. 7. Geisterfer-Lowrance, A. A. T., Kass, S., Tanigawa, G., Vosberg, H.-P., McKenna, W., Seidman, C. E., Seidman, J. G. A molecular basis for familial hypertrophic cardiomyopathy: a beta cardiac myosin heavy chain gene missense mutation. Cell 1990; 62: 999-1006. 8. Hougs L HO, Bundgaard H, Kober L, et al. One third of Danish hypertrophic cardiomyopathy patients with MYH7 mutations have mutations [corrected] in MYH7 rod region. Eur J Hum Genet 2005; 13(5):161-165. 9. Kaski JP, Syrris P, Esteban MT, Jenkins S, Pantazis A, Deanfield JE, McKenna WJ, Elliott PM. Prevalence of sarcomere protein gene mutations in preadolescent children with hypertrophic cardiomyopathy. Circ Cardiovasc Genet. 2009 Oct;2(5):436-441. 10. Klues HG, Leuner C, Kuhn H. Left ventricular outflow tract obstruction in patients with hypertrophic cardiomyopathy: increase in gradient after exercise. J Am Coll Cardiol 1992;19:527–33. 11. Ko, Y.-L., Chen, J.-J., Tang, T.-K., Cheng, J.-J., Lin, S.-Y., Liou, Y.-C., Kuan, P., Wu, C.-W., Lien, W.-P., Liew, C.- C. Malignant familial hypertrophic cardiomyopathy in a family with a 453arg-to-cys mutation in the beta-myosin heavy chain gene: coexistence of sudden death and end-stage heart failure. Hum. Genet. 1996; 97: 585-590. 12. Liu W, Xie W, Hu D, et al. [Analysis of MYH7, MYBPC3 and TNNT2 gene mutations in 10 Chinese pedigrees with familial hypertrophic cardiomyopathy and the correlation between genotype and phenotype] Chinese [Abstract]. Zhonghua Xin Xue Guan Bing Za Zhi 2006; 34(3): 202. 13. Luis C. Afonso, Juan Bernal, Jeroen J. Bax, and Theodore P. Abraham. Echocardiography in Hypertrophic Cardiomyopathy: The Role of Conventional and Emerging Technologies J. Am. Coll. Cardiol. Img. 2008;1;787-800. 14. Maron BJ, Bonow RO, Cannon RO III, Leon MB, Epstein SE. Hypertrophic cardiomyopathy. Interrelations of clinical manifestations, pathophysiology, and therapy. N Engl J Med 1987;316:844–52. 15. Maron BJ, Epstein SE, Roberts WC. Hypertrophic cardiomyopathy and transmural myocardial infarction without significant atherosclerosis of the extramural coronary arteries. Am J Cardiol. 1979 Jun;43(6):1086-1102. 16. Maron BJ, Gardin JM, Flack JM, Gidding SS, Kurosaki TT, Bild DE. Prevalence of hypertrophic cardiomyopathy in a general population of young adults. Echocardiographic analysis of 4111 subjects in the CARDIA Study. Coronary Artery Risk Development in (Young) Adults. Circulation. 1995 Aug; 15;92(4):785-9. 17. Maron BJ, Savage DD, Wolfson JK, Epstein SE. Prognostic significance of 24 hour ambulatory electrocardiographic monitoring in patients with hypertrophic cardiomyopathy: a prospective study. Am J Cardiol. 1981 Aug;48(2):252-7. 18. Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA 2002;287:1308–20. Nghiên cứu lâm sàng TẠP CHÍ TIM MẠCH HỌC VIỆT NAM - SỐ 65.201488 19. McKenna WJ, England D, Doi YL, Deanfield JE, Oakley C, Goodwin JF. Arrhythmia in hypertrophic cardiomyopathy. I: Influence on prognosis. Br Heart J. 1981 Aug;46(2):168-72. 20. Montazeri M, Houshmand MHM, Ghani Kakhki M, et al. Investigations of hot spot regions in MYH7 genes in Iranian hypertrophic cardiomyopathy patients. Proceeding of the 4PthP national biotechnology congress. Kerman: Kerman University of Medical Sciences; 2005. 21. Morita H, Rehm HL, Menesses A, McDonough B, Roberts AE, Kucherlapati R, Towbin JA, Seidman JG, Seidman CE. Shared genetic causes of cardiac hypertrophy in children and adults. N Engl J Med. 2008 May 1;358(18):1899-908. 22. Pare, J. A. P., Fraser, R. G., Pirozynski, W. J., Shanks, J. A., Stubington, D. Hereditary cardiovascular dysplasia: a form of familial cardiomyopathy. Am. J. Med. 1961; 31: 37-62. 23. Perryman, M. B., Yu, Q., Marian, A. J., Mares, A., Jr., Czernuszewicz, G., Ifegwu, J., Hill, R., Roberts, R. Expression of a missense mutation in the messenger RNA for beta-myosin heavy chain in myocardial tissue in hypertrophic cardiomyopathy. J. Clin. Invest. 1992; 90: 271-277. 24. Radovan HP, Št_pánka H, Martin B. Familial hypertrophic cardiomyopathy owing to double heterozygosity for a 403Arg_Trp mutation in exon 13 of the MYH7 gene and a novel mutation, 453Arg_His, in exon 14 of the MYH7 gene: A case report. Exp Clin Cardiol 2001; 6(4): 223-227. 25. Reena Tanjore, Advithi RangaRaju and Pratibha Nallari Genetic Variations of β-MYH7 in hypertrophic cardiomyopathy and dilated cardiomyopathy. Indian J Hum Genet. 2010 May-Aug; 16(2): 67–71. 26. Sherif F. Nagueh, Nasser M. Lakkis, Katherine J. Middleton, William H. Spencer III, William A. Zoghbi and Miguel A. Doppler Estimation of Left Ventricular Filling Pressures in Patients With Hypertrophic Cardiomyopathy Circulation 1999, 99:254-261. 27. Spindler, M., Saupe, K. W., Christe, M. E., Sweeney, H. L., Seidman, C. E., Seidman, J. G., Ingwall, J. S. Diastolic dysfunction and altered energetics in the alpha-MHC-403/+ mouse model of familial hypertrophic cardiomyopathy. J. Clin. Invest. 1998; 101: 1775-1783. 28. Stewart S, Schreiner B. Coexisting idiopathic hypertrophic subaortic stenosis and coronary artery disease. Clinical implication and operative management. J Thorac Cardiovasc Surg. 1981 Aug;82(2):278-80. 29. Van Driest SL, Ackerman MJ, Ommen SR, Shakur R, Will ML, Nishimura RA, Tajik AJ, Gersh BJ. Prevalence and severity of “benign” mutations in the beta-myosin heavy chain, cardiac troponin T, and alpha-tropomyosin genes in hypertrophic cardiomyopathy. Circulation. 2002 Dec 10;106(24):3085-90. 30. Wang H et al., “Genetic heterogeneity of myosin heavy chain 7 gene G823E mutation in familial hypertrophic cardiomyopathy in Chinese”, PubMed, 2008; 2;88(44):3120-2. 31. Watkins H, Rosenzweig A, Hwang DS, Levi T, McKenna W, Seidman CE, Seidman JG. Characteristics and prognostic implications of myosin missense mutations in familial hypertrophic cardiomyopathy. N Engl J Med. 1992 Apr 23;326(17):1108-14.
File đính kèm:
 phat_hien_dot_bien_gen_tong_hop_chuoi_nang_beta_myosin_myh7.pdf
phat_hien_dot_bien_gen_tong_hop_chuoi_nang_beta_myosin_myh7.pdf

