Nghiên cứu đáp ứng xơ hoá gan ở bệnh nhân xơ gan còn bù do virus viêm gan B điều trị bằng Entecavir
Việc đánh giá về đáp ứng xơ hoá gan sau khi điều trị kháng virus HBV ở nước ta cho đến hiện nay còn rất ít, đặc biệt trên đối tượng bệnh nhân đã có xơ gan. Nghiên cứu này nhằm xác định sự thay đổi chỉ số xơ hoá gan và các yếu tố liên quan ở bệnh nhân xơ gan do HBV được điều trị bằng entecavir.

Trang 1

Trang 2
Trang 3
Trang 4

Trang 5

Trang 6

Trang 7
Bạn đang xem tài liệu "Nghiên cứu đáp ứng xơ hoá gan ở bệnh nhân xơ gan còn bù do virus viêm gan B điều trị bằng Entecavir", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Nghiên cứu đáp ứng xơ hoá gan ở bệnh nhân xơ gan còn bù do virus viêm gan B điều trị bằng Entecavir

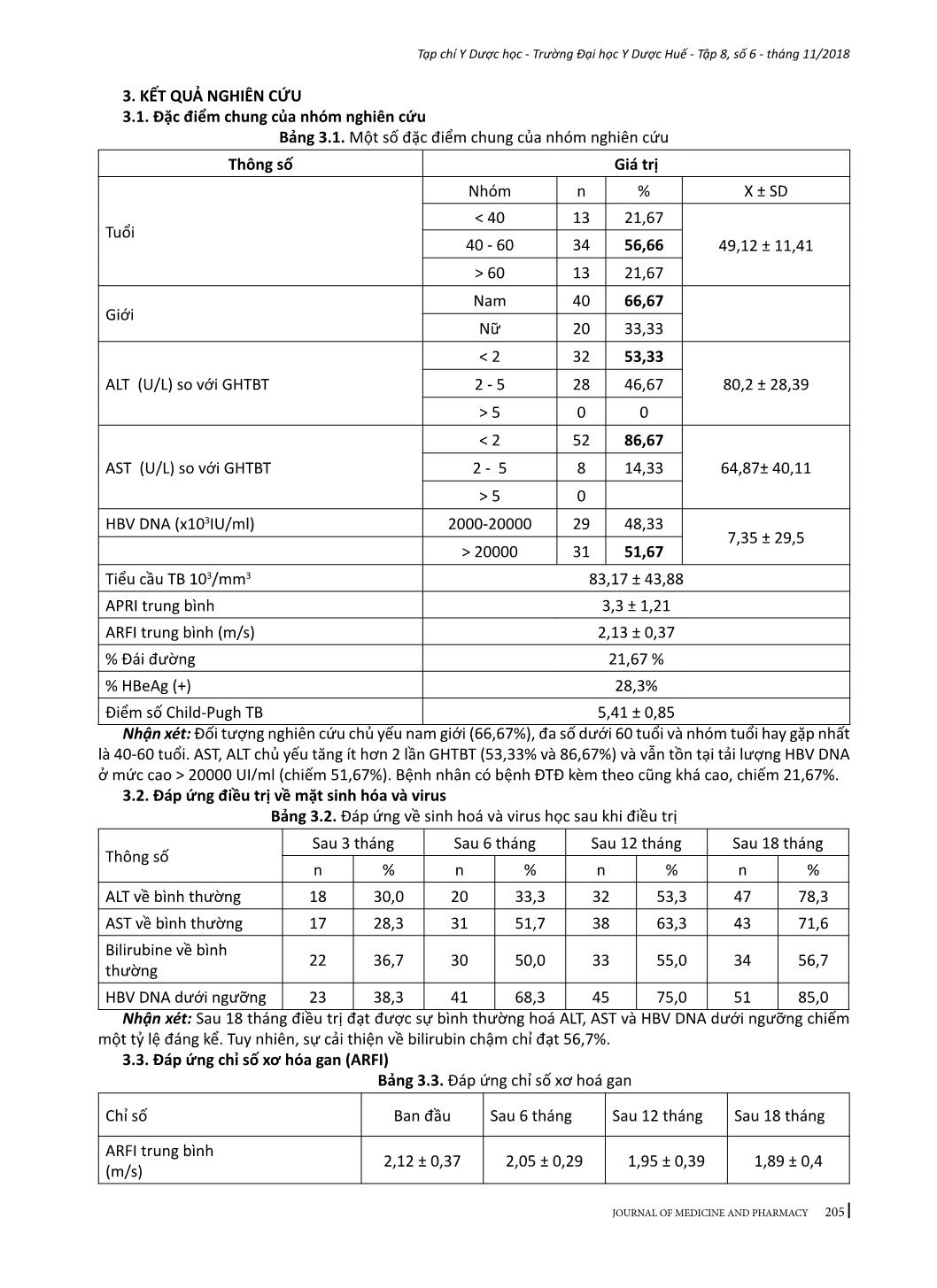
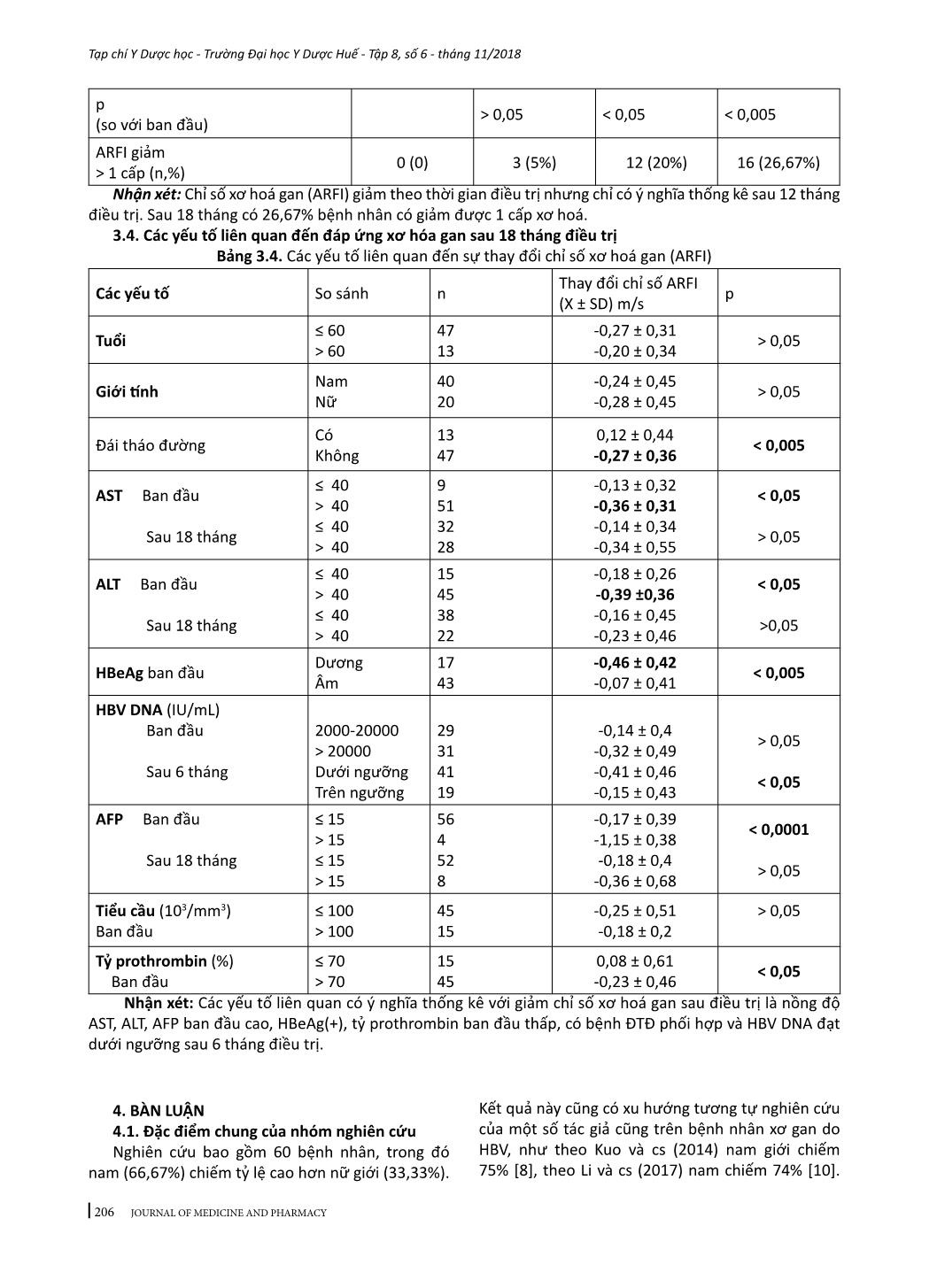
203 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY NGHIÊN CỨU ĐÁP ỨNG XƠ HOÁ GAN Ở BỆNH NHÂN XƠ GAN CÒN BÙ DO VIRUS VIÊM GAN B ĐIỀU TRỊ BẰNG ENTECAVIR Đoàn Hiếu Trung1, Trần Xuân Chương2 (1) Nghiên cứu sinh Trường Đại học Y Dược, Đại học Huế, chuyên ngành Nội tiêu hóa (2) Bộ môn Truyền nhiễm, Trường Đại học Y Dược Huế Tóm tắt Đặt vấn đề: Việc đánh giá về đáp ứng xơ hoá gan sau khi điều trị kháng virus HBV ở nước ta cho đến hiện nay còn rất ít, đặc biệt trên đối tượng bệnh nhân đã có xơ gan. Nghiên cứu này nhằm xác định sự thay đổi chỉ số xơ hoá gan và các yếu tố liên quan ở bệnh nhân xơ gan do HBV được điều trị bằng entecavir. Đối tượng và phương pháp: 60 bệnh nhân xơ gan còn bù do HBV đến khám và điều trị tại bệnh viện Đà Nẵng từ 06/2016 đến 06/2018. Độ xơ hoá được đo bằng kỹ thuật ghi hình xung lực truyền âm (ARFI: Acoustic Radiation Forced Imaging). Thuốc: Entecavir của công ty BMS (BaracludeR), hàm lượng 0,5mg, ngày uống 1 viên sau ăn sáng 2 giờ, theo dõi trong 18 tháng. Kết quả: Điều trị Entecavir có thể đem lại sự cải thiện về chỉ số xơ hóa gan 20 % sau 12 tháng và 26,67% sau 18 tháng ở bệnh nhân xơ gan do virus viêm gan B. Sự cải thiện mức độ xơ hóa gan có ý nghĩa sau ít nhất là 12 tháng điều trị. Yếu tố liên quan đến cải thiện đáp ứng xơ hóa gan trong nghiên cứu này gồm hoạt độ AST, ALT, AFP ban đầu cao, HBeAg(+), thời gian prothrombin ban đầu thấp và đạt HBV DNA dưới ngưỡng sau 6 tháng điều trị. Kết luận: Điều trị entecavir có thể giúp đem lại sự cải thiện về xơ hóa gan ở bệnh nhân xơ gan do virus viêm gan B, nhưng cần thiết phải điều trị lâu dài. Từ khoá: Entecavir, xơ gan còn bù do HBV, xơ hoá gan, ARFI Abstract LIVER FIBROSIS RESPONSE TO ENTECAVIR TREATMENT IN PATIENTS WITH HBV-RELATED COMPENSATED CIRRHOSIS Doan Hieu Trung1, Tran Xuan Chuong2 (1) PhD students of Hue University of Medicine and Pharmacy, Hue University (2) Department of Infectious diseases, Hue University of Medicine and Pharmacy Background: Evaluating improvement of liver fibrosis response after anti HBV therapy in our country until now is very limited, especially in patients with cirrhosis. This study aimed at assessing the respone in liver fibrosis determined by ARFI and its related factors for patients with compensated HBV-related cirrhosis undergoing entecavir therapy. Subjects and methods: 60 patients with compensated HBV-related cirrhosis were enrolled at Da Nang Hospital from 06/2016 to 06/2018. All received entecavir 0,5mg a day 2 hours after breakfast and followed in 18 months. Liver fibrosis is measured by Acoustic Radiation Forced Imaging (ARFI). Results: Entecavir treatment may result in improvement of liver fibrosis in 20% after 12 months and 26.67% after 18 months in patients with compensated hepatitis B virus-related cirrhosis. The improvement in fibrosis levels was significant after at least 12 months of treatment. Factors associated with improvement of fibrosis response in this study included AST, ALT, AFP are high, HBeAg (+), low prothrombin time at baseline, and indetectable HBV DNA after 6 months of treatment. Conclusion: Entecavir treatment may help to improve liver fibrosis in patients with hepatitis B virus-related compensated cirrhosis, but long-term treatment is needed. Key words: Entecavir, HBV cirrhosis, liver fibrosis, ARFI. - Địa chỉ liên hệ: Đoàn Hiếu Trung, email: dhtrungbsdn@gmail.com - Ngày nhận bài: 12/10/2018; Ngày đồng ý đăng: 8/11/2018, Ngày xuất bản: 17/11/2018 204 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY 1. ĐẶT VẤN ĐỀ Viêm gan B mạn đang ảnh hưởng đến khoảng 400 triệu người trên toàn thế giới và đưa đến các biến chứng nặng như xơ gan, mất bù gan và ung thư biểu mô tế bào gan (HCC) [8]. Mức độ của xơ hoá gan liên quan đến tiên lượng của bệnh gan. Điều trị kháng virus lâu dài để đạt được sự ức chế bền vững HBV đã được chứng minh làm cải thiện đáng kể các giai đoạn xơ hóa ở bệnh nhân viêm gan B mạn (VGBM) [11]. Do đó, theo dõi giai đoạn xơ hóa gan trong quá trình điều trị kháng virus là rất quan trọng để đánh giá hiệu quả của liệu pháp và tiên lượng bệnh. Sinh thiết gan được xem là tiêu chuẩn vàng, tuy nhiên cũng có nhiều hạn chế [7],[9]. Hiện nay một số kỹ thuật đánh giá xơ hoá gan không xâm nhập được FDA chấp nhận áp dụng trong lâm sàng như ARFI, Fibroscan,...Do đó tránh được nhiều trường hợp sinh thiết gan không cần thiết. Ở Việt Nam chưa có nhiều nghiên cứu về đáp ứng xơ hoá gan sau khi điều trị kháng virus ở bệnh nhân xơ gan do HBV. ARFI là một kỹ thuật còn khá mới và bước đầu cho thấy có nhiều ưu điểm để đánh giá xơ hoá gan, giúp đưa ra các chỉ định điều trị, theo dõi điều trị và đặc biệt có thể dự đoán các biến chứng [1],[5]. Chúng tôi thực hiện nghiên cứu này nhằm khảo sát đáp ứng xơ hoá gan và các yếu tố liên quan đối với bệnh nhân xơ gan còn bù do HBV điều trị bằng entecavir. 2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU 2.1. Đối tượng nghiên cứu Những bệnh nhân > 18 tuổi và ≤ 75 tuổi đến khám và điều trị ở Bệnh viện Đà Nẵng tại khoa Nội tiêu hóa-gan mật và phòng khám Nội tiêu hóa, từ 06/2016 đến 06/2018. Có 60 bệnh nhân được chọn, thỏa mãn tiêu chuẩn sau: * Tiêu chuẩn chọn bệnh - HBsAg dương tính > 6 tháng hoặc HBsAg và anti-HBs IgG dương tính. - HBV DNA ≥ 2000 UI/ml (104 copies/ml) - Xơ gan còn bù: Chẩn đoán dựa vào hội chứng suy tế bào gan, tăng áp cửa trên lâm sàng kết hợp với cận lâm sàng và thoã mãn 2 điều kiện sau: + Chưa có 1 trong các biến chứng như xuất huyết do vỡ giãn tĩnh mạch thực quản-dạ dày, bệnh não gan, cổ trướng (ascite) hay hoàng đảm. + và phải đáp ứng tiêu chí ARFI ≥ 1,75 m/s [4] và APRI ≥ 2 [14]. * Tiêu chuẩn loại trừ - Anti HCV (+), anti-HIV (+) - Viêm gan tự miễn - Nghiện rượu - Xơ gan mất bù hoặc ung thư gan 2.2. Phương pháp nghiên cứu - Thiết kế ... Âm 17 43 -0,46 ± 0,42 -0,07 ± 0,41 < 0,005 HBV DNA (IU/mL) Ban đầu Sau 6 tháng 2000-20000 > 20000 Dưới ngưỡng Trên ngưỡng 29 31 41 19 -0,14 ± 0,4 -0,32 ± 0,49 -0,41 ± 0,46 -0,15 ± 0,43 > 0,05 < 0,05 AFP Ban đầu Sau 18 tháng ≤ 15 > 15 ≤ 15 > 15 56 4 52 8 -0,17 ± 0,39 -1,15 ± 0,38 -0,18 ± 0,4 -0,36 ± 0,68 < 0,0001 > 0,05 Tiểu cầu (103/mm3) Ban đầu ≤ 100 > 100 45 15 -0,25 ± 0,51 -0,18 ± 0,2 > 0,05 Tỷ prothrombin (%) Ban đầu ≤ 70 > 70 15 45 0,08 ± 0,61 -0,23 ± 0,46 < 0,05 Nhận xét: Các yếu tố liên quan có ý nghĩa thống kê với giảm chỉ số xơ hoá gan sau điều trị là nồng độ AST, ALT, AFP ban đầu cao, HBeAg(+), tỷ prothrombin ban đầu thấp, có bệnh ĐTĐ phối hợp và HBV DNA đạt dưới ngưỡng sau 6 tháng điều trị. 4. BÀN LUẬN 4.1. Đặc điểm chung của nhóm nghiên cứu Nghiên cứu bao gồm 60 bệnh nhân, trong đó nam (66,67%) chiếm tỷ lệ cao hơn nữ giới (33,33%). Kết quả này cũng có xu hướng tương tự nghiên cứu của một số tác giả cũng trên bệnh nhân xơ gan do HBV, như theo Kuo và cs (2014) nam giới chiếm 75% [8], theo Li và cs (2017) nam chiếm 74% [10]. 207 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY Tuổi trung bình là 49,12 ± 11,41 tuổi, kết quả này cũng tương tự với một số nghiên cứu có tuổi trung bình từ 49,41 đến 54,3 tuổi [8],[10]. AST và ALT tăng trung bình gấp 1,5-2 lần giới hạn trên bình thường, điều này sẽ ít gây ảnh hưởng đến kết quả đo độ đàn hồi gan (ARFI). Các chỉ số khác nằm trong giới hạn phù hợp ở đối tượng bệnh nhân xơ gan còn bù, đặc biệt phản ánh qua chỉ số Child-Pugh trung bình là 5,41 ± 0,85 điểm. 4.2. Đáp ứng về sinh hoá và virus học Kết quả nghiên cứu của chúng tôi cho thấy các chỉ số sinh hoá và virus học (bảng 2) được cải thiện đáng kể sau 12 tháng điều trị và sau 18 tháng thì tỷ lệ bình thường hoá AST và ALT lần lượt là 71,6% và 78,3%, bilirubin toàn phần đạt dưới ngưỡng là 56,7% và HBV DNA dưới ngưỡng chiếm tỷ lệ khá cao (85%). Tuy nhiên, nghiên cứu của Trần Văn Huy và cs (2015) qua các thời điểm theo dõi trên đối tượng viêm gan B mạn, đặc biệt sau 24 tháng điều trị đạt được tỷ lệ đáp ứng cao hơn của chúng tôi. Tỷ lệ bình thường hoá ALT, AST lần lượt là 93,5%, 89,1% và HBV DNA dưới ngưỡng đạt 97,8% [1]. Điều này có thể do đối tượng nghiên cứu của chúng tôi là bệnh nhân đã bị xơ gan nên đáp ứng miễn dịch sẽ khác với bệnh nhân viêm gan mạn, hơn nữa tình trạng xơ hoá gan cũng ảnh hưởng đến cải thiện về sinh hoá và virus. 4.3. Đánh giá đáp ứng xơ hoá gan Xơ hoá gan là sự hình thành tổ chức mô sẹo để đáp ứng với tổn thương nhu mô gan thứ phát sau các nguyên nhân gây viêm gan mạn như viêm gan mạn do virus B, C, bệnh gan mỡ không do rượu (NAFLD),...Hậu quả đưa đến đảo lộn cấu trúc nhu mô gan bình thường. Sự thay thế liên tục và tiến triển của tế bào gan bằng các cơ chất ngoại bào (matrix) và các mô xơ đưa đến xơ gan [2]. Trước đây người ta cho rằng xơ hoá gan tiến triển là một quá trình không thể hồi phục, nhưng gần đây qua nghiên cứu cho thấy ngay cả xơ gan cũng có thể được đảo ngược nếu nguyên nhân bị loại bỏ [3],[11]. Vì vậy, đối với viêm gan B mạn, việc tối ưu hóa sự ức chế virus với mục tiêu kiểm soát xơ hóa gan và ngăn chặn sự tiến triển đến các biến chứng nặng là mục đích điều trị nhiễm HBV mạn [11]. Trong các phương pháp đánh giá xơ hóa gan không xâm lấm hiện nay, đo đàn hồi gan được xem là một kỹ thuật có độ chính xác khá cao, khả thi, dễ thực hiện, trong đó ghi hình xung lực truyền âm (ARFI) là kỹ thuật đã được nhiều nghiên cứu cho thấy có độ chính xác, độ nhạy và độ đặc hiệu tương đương với kỹ thuật Fibroscan, thậm chí có nhiều ưu điểm hơn Fibroscan như có thể làm ở người béo phì, khoảng liên sườn hẹp, có báng và cung cấp được nhiều thông tin về tình trạng của gan nhờ vào hình ảnh siêu âm 2D [5],[9] và hiện nay kỹ thuật ARFI đã được FDA công nhận để đánh giá xơ hoá gan. Kết quả nghiên cứu của chúng tôi cho thấy chỉ số xơ hoá gan có sự giảm dần so với ban đầu trong quá trình theo dõi (bảng 3). Tuy nhiên, chỉ sau 12 tháng sự giảm này mới có ý nghĩa thống kê (1,95 ± 0,39 m/s vs 2,12 ± 0,37, p < 0,05) và chỉ số xơ hoá giảm tốt hơn sau 18 tháng điều trị (1,88 ± 0,4 m/s, p < 0,005). So với kết quả đánh giá xơ hoá gan bằng kỹ thuật đo độ đàn hồi thoáng qua (Fibroscan) của Li và cs (2017) cũng trên đối tượng bệnh nhân xơ gan do HBV điều trị bằng entecavir, cho thấy có sự cải thiện rõ rệt về chỉ số xơ hoá gan chỉ sau 6 tháng điều trị (giảm từ 21,59±10.25 kPa xuống còn 15,76 ± 9.52 kPa, p < 0,001). Theo kết quả của Trần Văn Huy và cs (2015) trên đối tượng bệnh nhân viêm gan B mạn điều trị bằng entecavir, chỉ số xơ hoá gan cải thiện rõ chỉ sau 24 tháng điều trị (1,12 ± 0,24 m/s vs 1,46 ± 0,34 m/s, p < 0,05) [1]. Các kết quả này nhìn chung cho thấy chỉ số xơ hoá gan giảm sớm hơn ở đối tượng bệnh nhân xơ gan so với đối tượng bệnh nhân viêm gan mạn. Điều này có thể là do bệnh nhân không xơ gan có tình trạng gan tốt hơn so với những người đã bị xơ gan và sự thay đổi mô học gan chủ yếu dựa trên tình trạng viêm hoại tử [10]. Ngoài ra, việc cần thiết điều trị kháng virus lâu dài theo kết quả của hầu hết các nghiên cứu cho thấy là yếu tố quyết định để cải thiện tình trạng xơ hoá [13]. Điều trị lamivudine và entecavir cho bệnh nhân viêm gan B mạn sau 1 năm đạt được cải thiện chỉ số xơ hoá gan lần lượt là 35-38% và 36-39%. Tỷ lệ này cao hơn nhiều sau 3 năm điều trị bằng entecavir làm giảm xơ hóa gan ở 57–100% bệnh nhân [12]. Qua các kết quả của các nghiên cứu đều thống nhất ở điểm điều trị kháng HBV bằng các thuốc kháng virus đường uống ở bệnh nhân viêm gan B mạn kể cả đã bị xơ gan có thể dẫn đến sự cải thiện chỉ số xơ hóa gan, tuy nhiên cần phải điều trị lâu dài. Như vậy, kết hợp nhiều dữ liệu cho thấy sự hồi phục xơ hoá liên quan đến viêm gan B có thể không chỉ đơn thuần là kết quả từ sự ức chế HBV DNA mà có thể có những lợi ích khác khi điều trị lâu dài với các thuốc kháng virus đường uống (NA). Nghiên cứu cho thấy sự giảm độ cứng của gan sau khi điều trị kháng virus liên quan có ý nghĩa với sự suy giảm acid hyaluronic [8]. Ngoài ra, việc điều trị lâu dài bằng các NA cũng được chứng minh rằng có thể khôi phục chức năng của các tế bào T đặc hiệu HBV và có thể điều chỉnh hệ miễn dịch. Do đó, tác dụng điều hòa miễn dịch điều trị NA lâu dài cũng có thể đóng một vai trò trong hồi phục xơ hóa gan. Các tế bào hình sao gan đóng một vai trò quan trọng trong quá trình sinh xơ hoá và vẫn chưa rõ liệu các NA có thể trực 208 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY tiếp hoặc gián tiếp điều chỉnh các tế bào hình sao gan hoạt hóa hay không. Tuy nhiên, với sự tiến bộ đáng kể của khoa học giúp ngày càng hiểu rõ hơn về cơ chế sinh xơ hoá và sự đảo ngược của xơ gan, từ đó có thể đưa ra các chiến lược điều trị hiệu quả hơn đối với bệnh nhân xơ hoá gan tiến triển hoăc xơ gan do HBV [13]. 4.4. Các yếu tố liên quan đến cải thiện chỉ số xơ hoá gan Sự đáp ứng về chỉ số xơ hoá gan cần đòi hỏi thời gian điều trị kháng virus lâu dài và chỉ đạt được ở một số bệnh nhân nhất định. Vì vậy, việc tìm ra các yếu tố liên quan để dự báo về khả năng đáp ứng cải thiện xơ hoá gan là rất quan trọng, đặc biệt giúp người bệnh an tâm hơn trong quá trình điều trị [1]. Tuy nhiên, kết quả từ các nghiên cứu cho thấy các yếu tố liên quan đến chỉ số đáp ứng xơ hoá gan là chưa hằng định, phụ thuộc vào giai đoạn của bệnh và thời gian điều trị kháng virus [1],[8],[10],[15]. Trong nghiên cứu của chúng tôi, khi phân tích hồi quy đơn biến cho thấy đáp ứng xơ hoá gan có mối liên quan có ý nghĩa với một số yếu tố như nồng độ AST, ALT, AFP ban đầu cao, HBeAg(+), thời gian prothrombin ban đầu thấp và đạt được tải lượng HBV DNA dưới ngưỡng sau 6 tháng điều trị. Các yếu tố còn lại chưa thấy có mối liên quan (bảng 4). So với một vài nghiên cứu khác cũng trên đối tượng xơ gan do HBV cho kết quả không hằng định. Kết quả của chúng tôi khá phù hợp với nghiên cứu của Kuo và cs năm 2015, tuy nhiên trong nghiên cứu này tình trạng HBeAg không thấy mối liên quan và không đề cập đến dự kiện tải lượng HBV DNA dưới ngưỡng sau 6 tháng điều trị [8]. Theo Li và cs (2017) kết quả cho thấy có sự suy giảm đáng kể giá trị độ cứng gan sau khi điều trị liên quan đến chỉ số độ cứng và tải lượng HBV DNA ban đầu cao và không có sự thay đổi đáng kể về nồng độ ALT, TBIL và AFP [10]. Điều này có thể do thực hiện nghiên cứu trong thời gian ngắn (6 tháng). Tương tự, trên đối tượng viêm gan B mạn cũng tìm thấy có một số yếu tố liên quan đến đáp ứng xơ hoá gan. Theo nghiên cứu của Trần Văn Huy và cs (2015), đáp ứng xơ hóa gan sau 24 tháng chỉ có mối liên quan khá chặt chẽ với tuổi bệnh nhân, đáp ứng AST và HBV DNA sau 24 tuần [1]. Tuy nhiên, theo nghiên cứu của Yo và cs (2015) cho thấy độ cứng của gan ban đầu cao là yếu tố duy nhất liên quan đến sự thay đổi độ cứng của gan sau điều trị [15]. Ngoài ra, nghiên cứu của chúng tôi nhận thấy ĐTĐ cũng là một yếu tố phối hợp gây ảnh hưởng đến đáp ứng xơ hoá gan. Kết quả này cũng phù hợp với nghiên cứ của Kuo và cs, khi phân tích đơn biến và đa biến cho thấy ĐTĐ liên quan chặt chẽ đến việc giảm cải thiện chỉ số xơ hoá gan khi điều trị (p< 0,001 và p < 0,05), đặc biệt ở bệnh nhân xơ gan do HBV ngay cả khi được điều trị bằng ETV [8] . Một số nghiên cứu khác cũng cho thấy bệnh nhân ĐTĐ2 có thể làm giảm hiệu quả của thuốc kháng virus ở bệnh nhân viêm gan C mạn và đưa đến các hậu quả xấu [8]. Tuy nhiên, chưa có nhiều nghiên cứu đề cập mối liên quan giữa ĐTĐ2 với điều trị kháng virus ở bệnh nhân viêm gan B mạn. Một nghiên cứu trước đây cho thấy ĐTĐ là yếu tố nguy cơ độc lập cho sự phát triển ung thư biểu mô tế bào gan (HCC) ở bệnh nhân viêm gan B mạn, đặc biệt ở bệnh nhân đã bị xơ gan [6]. Từ các bằng chứng này cho thấy ở bệnh nhân viêm gan B mạn phối hợp với ĐTĐ sẽ có nguy cơ cao phát hiển HCC và có lẽ cần được theo dõi chặt chẽ hơn cho đối tượng này. 5. KẾT LUẬN - Điều trị entecvir có thể đem lại sự cải thiện về chỉ số xơ hóa gan ở bệnh nhân xơ gan do HBV, đánh giá bằng kỹ thuật ARFI. - Mức độ xơ hóa gan được cải thiện có ý nghĩa sau ít nhất là 12 tháng điều trị. - Một số yếu tố liên quan đến đáp ứng xơ hóa gan trong nghiên cứu này bao gồm nồng độ AST, ALT, AFP ban đầu cao, HBeAg(+), thời gian prothrombin ban đầu thấp và đạt được HBV DNA dưới ngưỡng sau 6 tháng điều trị. 6. KIẾN NGHỊ Ngoài việc theo dõi các chỉ điểm sinh hoá và virus học, chúng ta nên sử dụng thường quy trong lâm sàng kỹ thuật ARFI để đánh giá mức độ xơ hoá gan để theo dõi đáp ứng điều trị kháng virus viêm gan B và tiên đoán các biến chứng có thể xảy ra. TÀI LIỆU THAM KHẢO 1. Trần Văn Huy, Nguyễn Phước Bảo Quân (2015), “Nghiên cứu đáp ứng xơ hoá gan ở bệnh nhân viêm gan B mạn hoạt động điều trị bằng enyecavir”, Tạp chí Y Dược học-Trường Đại học Y Dược Huế; 6(3):15-19. 2. Cheng JY-K and Wong GL-H (2017), “Advances in the diagnosis and treatment of liver fibrosis”, Hepatoma Res; 3:156-69. 3. Dienstag JI, Goldin RD, Healthcole WC et al (2003), 209 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY “Histological outcome during long-term lamivudine therapy”, Gastroenterology;124:105-173. 4. Friedrich-Rust M, Wunder K, Kriener S, Sotoudeh F et al (2009), “Liver fibrosis in viral hepatitis: noninvasive assessment with acoustic radiation force impulse imaging versus transient elastography”, Radiology; 252(2): 595- 604. 5. Frulio N, Trillaud H(2013), “Ultrasound elastography in liver”, Diagnostic and interventional imaging; 94(5): 515-534. 6. Gao C, Zhao HC, Li JT, Yao SK (2010), “Diabetes mellitus and hepatocellular carcinoma: comparison of Chinese patients with and without HBV-related cirrhosis”, World J Gastroenterol.; 16(35): 4467-75. 7. Grizzi F and Desmet VJ (2014), “Liver biopsy interpretation and the regression of hepatitis B virus related cirrhosis”, Indian J Med Res;140: 160-162. 8. Kuo YH, Lu SN, Chen CH, Chang KC, Hung CH et al (2014), “ The changes of liver stiffness and its associated factors for chronic hepatitis B patients with entecavir therapy; PLoS One 9: e93160. 9. Lee S and Kim DY (2014), “Non-invasive diagnosis of hepatitis B virus-related cirrhosis”, World J Gastroenterol; 20(2): 445-459. 10. Li X, Jin Q , Zhang H, Jing X, Ding Z et al (2017), “Changes in liver stiffness and its associated factors during oral antiviral therapy in Chinese patients with chronic hepatitis B”, Exp Ther Med.;13(3): 1169-1175. 11. Marcellin P, Gane E, Buti M, Afdhal N, Sievert Wet al (2013), “ Regression of cirrhosis during treatment with tenofovir disoproxil fumarate for chronic hepatitis B: A 5-year open-label follow-up study”, Lancet; 381: 468-475. 12. Schiff ER, Lee SS, Chao YC, Kew Yoon S, Bessone F, Wu SS et al (2011), “ Long-term treatment with entecavir induces reversal of advanced brosis or cirrhosis in patients with chronic hepatitis B”, Clin Gastroenterol Hepatol; 9: 274-276. 13. Wang JL, Du XF, Chen SL, Yu YQ, Wang J et al (2015), “Histological outcome for chronic hepatitis B patients treated with entecavir vs lamivudine-based therapy”, World J Gastroenterol.; 21(32): 9598–9606. 14. World Health Organization (2015). Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection. 15. Yo IK, Kwon OS, Park JW, Lee JJ, Lee JH (2014), “The factors associated with longitudinal changes in liver stiffness in patients with chronic hepatitis B”, Clinical and Molecular Hepatology; 21:32-40.
File đính kèm:
 nghien_cuu_dap_ung_xo_hoa_gan_o_benh_nhan_xo_gan_con_bu_do_v.pdf
nghien_cuu_dap_ung_xo_hoa_gan_o_benh_nhan_xo_gan_con_bu_do_v.pdf

