Nghiên cứu chế tạo nano bạc - Chitosan theo phương pháp bọc in-situ định hướng làm chế phẩm phòng bệnh trên cây trồng
Hạt nano bạc - chitosan (Ag@CS) được chế tạo theo phương pháp bọc
in-situ có kích thước trung bình 12,6 nm, hạt đồng đều, phân tán tốt trong nước và ổn
định. Kết quả thực nghiệm cho thấy nhiệt độ và thời gian phản ứng ảnh hưởng lớn đến
sự hình thành các hạt nano Ag@CS, kích thước hạt và độ đồng đều. Nhiệt độ tối ưu
cho các quá trình tổng hợp hạt Ag@CS là 60oC trong thời gian 3 giờ thu được các hạt
nano Ag@CS có hàm lượng Ag chiếm 9,01%. Thế zeta của Ag@CS dạng keo thu
được sau 3 tháng có giá trị là +25,6 mV chứng tỏ các hạt Ag@CS có độ ổn định tốt,
mở ra tiềm năng cho việc sử dụng hệ vật liệu này làm chế phẩm bảo vệ thực vật.

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5
Trang 6
Trang 7

Trang 8

Trang 9
Bạn đang xem tài liệu "Nghiên cứu chế tạo nano bạc - Chitosan theo phương pháp bọc in-situ định hướng làm chế phẩm phòng bệnh trên cây trồng", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Nghiên cứu chế tạo nano bạc - Chitosan theo phương pháp bọc in-situ định hướng làm chế phẩm phòng bệnh trên cây trồng

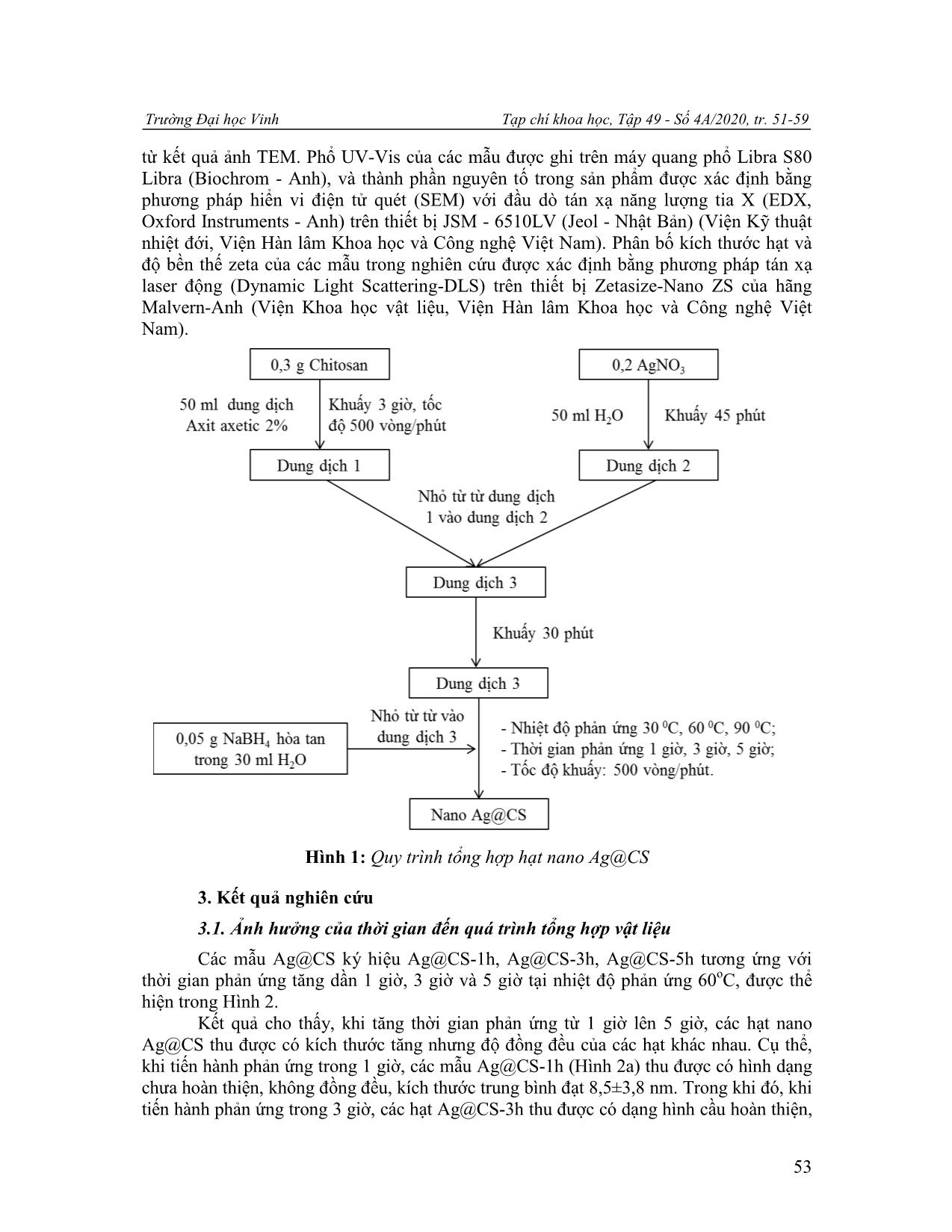
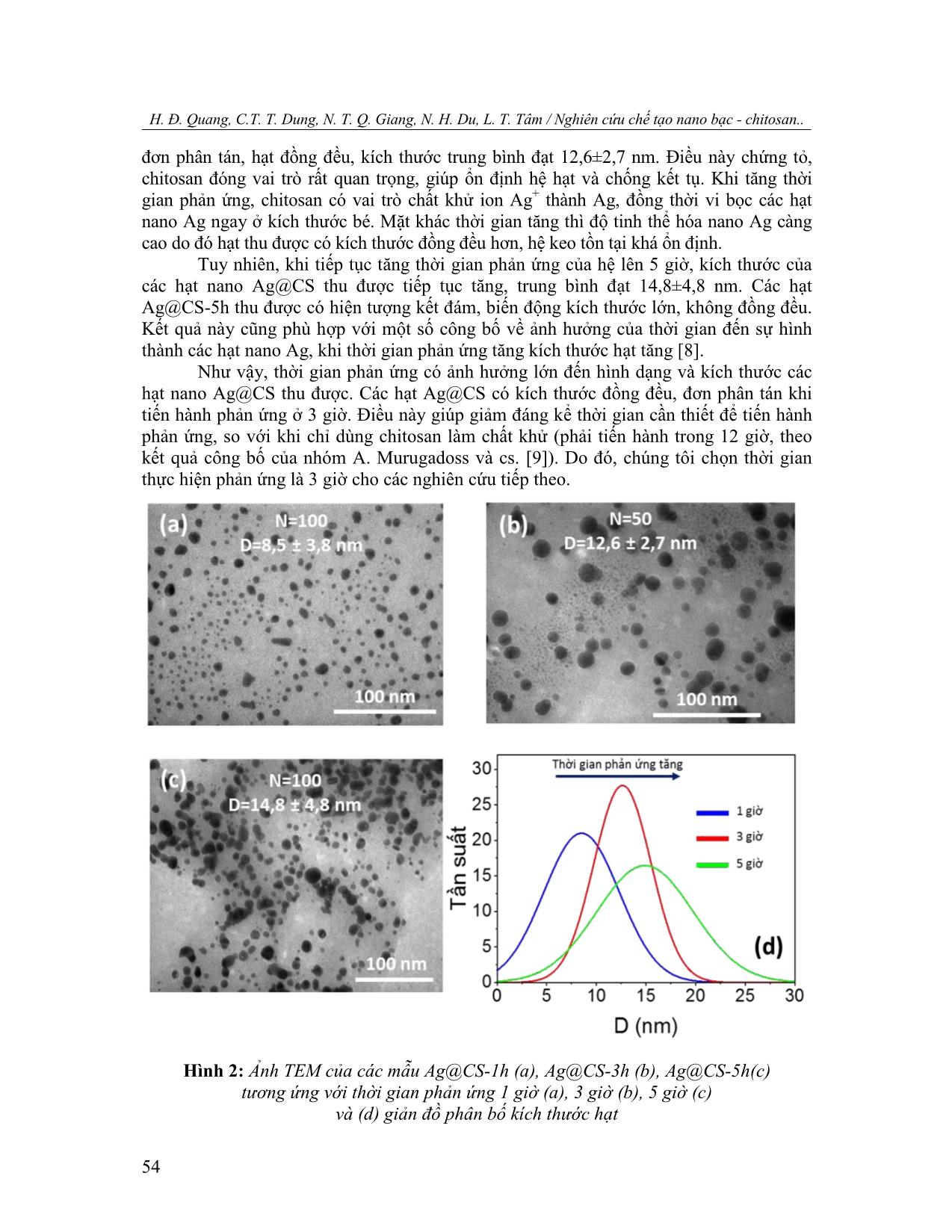
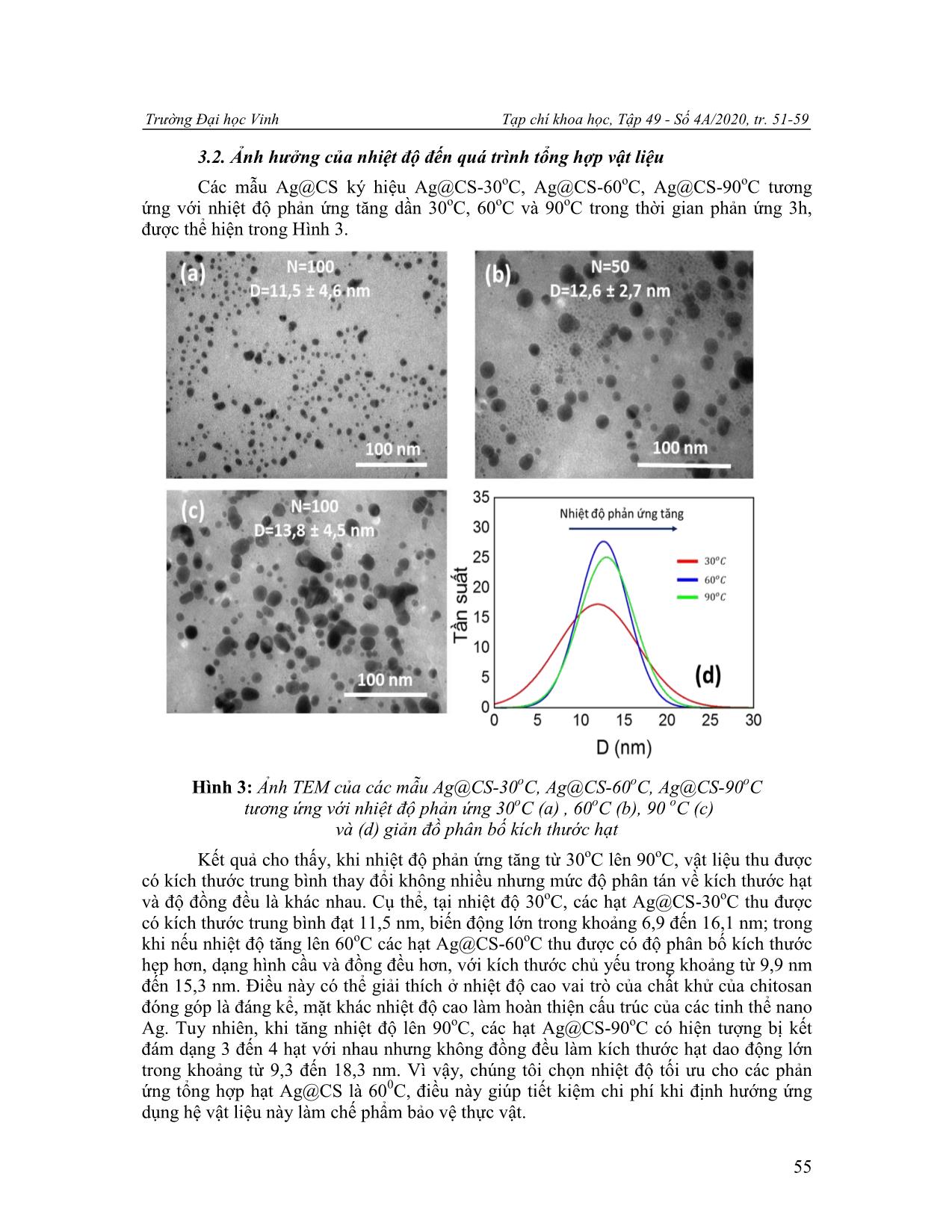
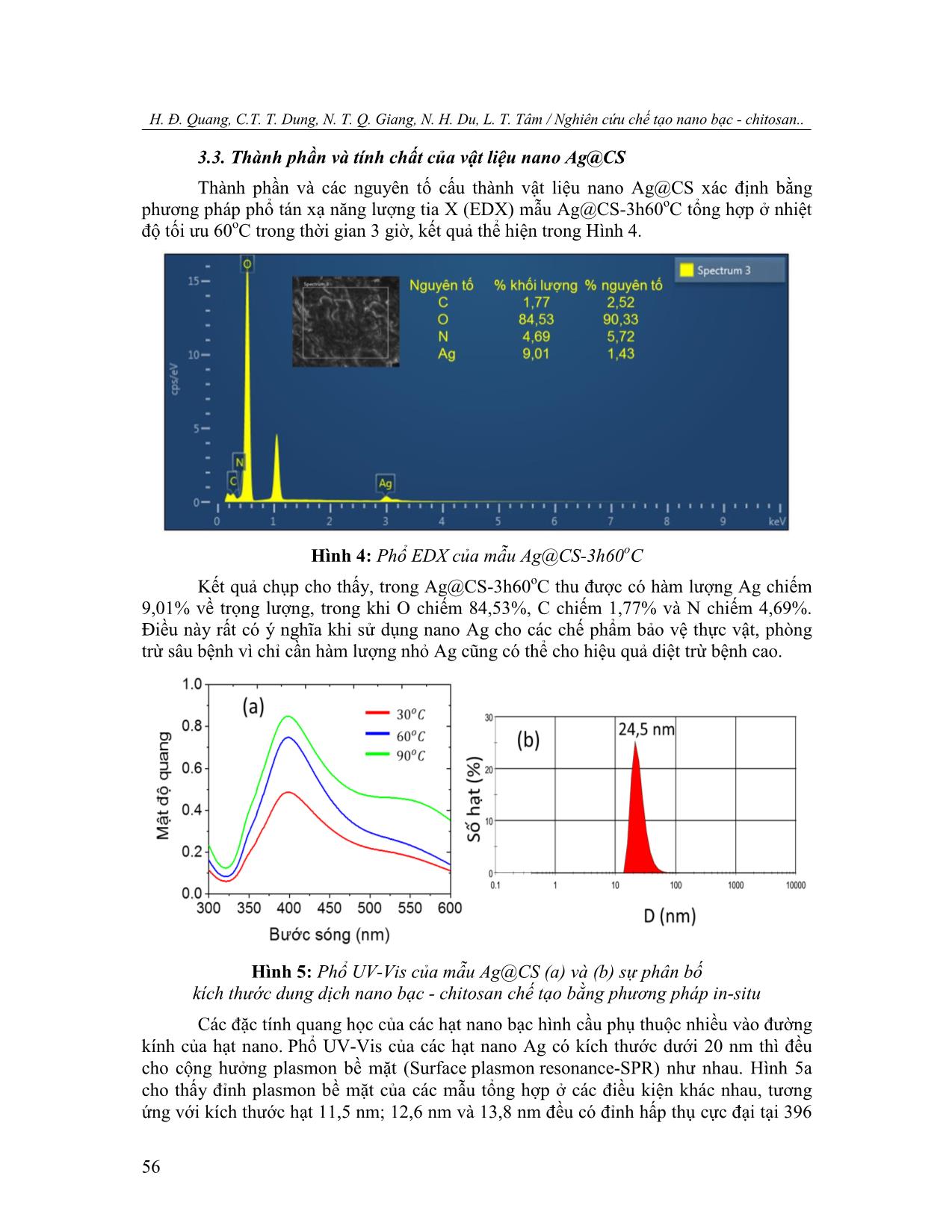
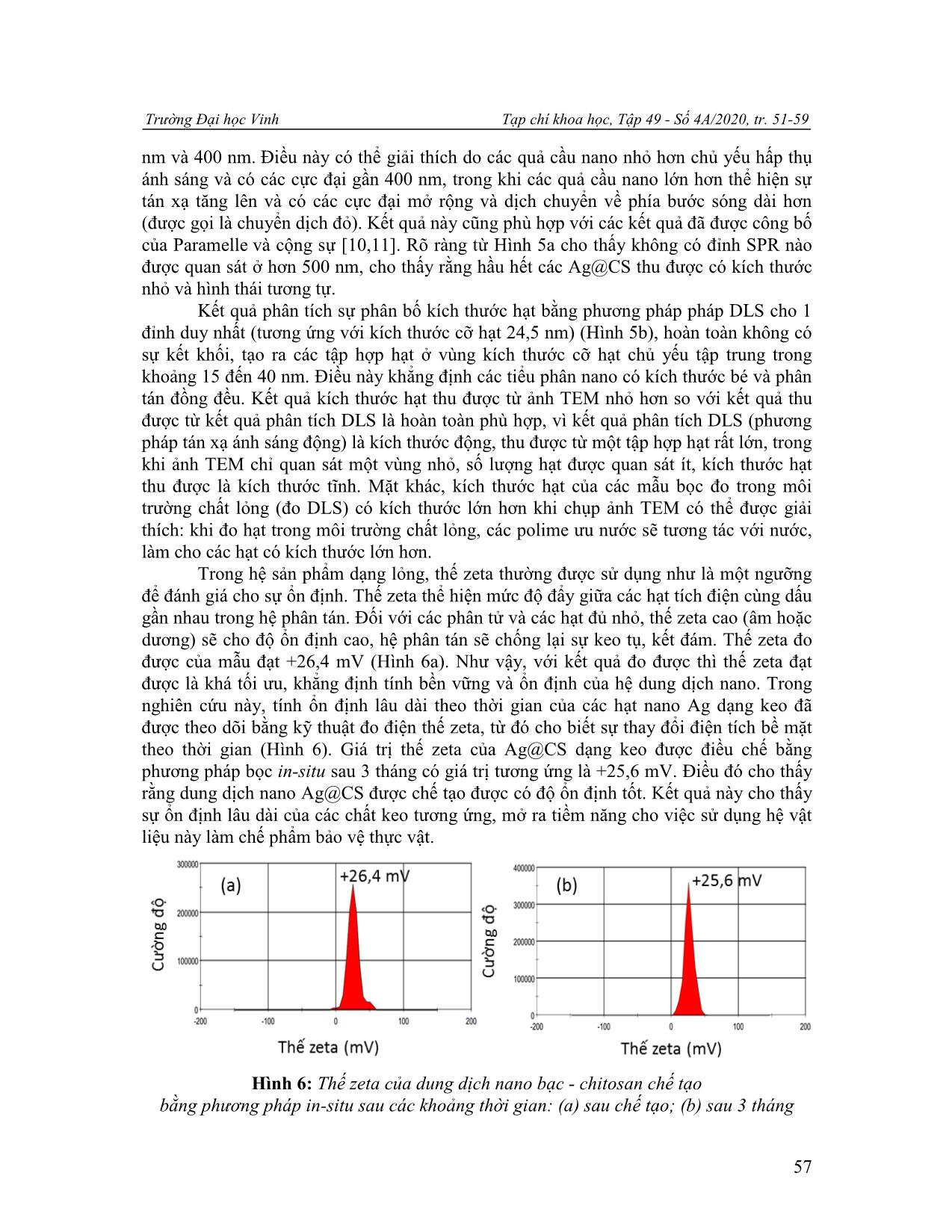
Trường Đại học Vinh Tạp chí khoa học, Tập 49 - Số 4A/2020, tr. 51-59 51 NGHIÊN CỨU CHẾ TẠO NANO BẠC - CHITOSAN THEO PHƢƠNG PHÁP BỌC IN-SITU ĐỊNH HƢỚNG LÀM CHẾ PHẨM PHÒNG BỆNH TRÊN CÂY TRỒNG Hồ Đình Quang (1), Chu Thị Thùy Dung (2), Nguyễn Thị Quỳnh Giang (1), Nguyễn Hoa Du (2), Lê Thế Tâm (1) 1 Viện Công nghệ Hóa Sinh - Môi trường, Trường Đại học Vinh 2 Viện Sư phạm Tự nhiên, Trường Đại học Vinh Ngày nhận bài 09/10/2020, ngày nhận đăng 13/12/2020 Tóm tắt: Hạt nano bạc - chitosan (Ag@CS) được chế tạo theo phương pháp bọc in-situ có kích thước trung bình 12,6 nm, hạt đồng đều, phân tán tốt trong nước và ổn định. Kết quả thực nghiệm cho thấy nhiệt độ và thời gian phản ứng ảnh hưởng lớn đến sự hình thành các hạt nano Ag@CS, kích thước hạt và độ đồng đều. Nhiệt độ tối ưu cho các quá trình tổng hợp hạt Ag@CS là 60oC trong thời gian 3 giờ thu được các hạt nano Ag@CS có hàm lượng Ag chiếm 9,01%. Thế zeta của Ag@CS dạng keo thu được sau 3 tháng có giá trị là +25,6 mV chứng tỏ các hạt Ag@CS có độ ổn định tốt, mở ra tiềm năng cho việc sử dụng hệ vật liệu này làm chế phẩm bảo vệ thực vật. Từ khóa: Nano bạc - chitosan; phương pháp bọc in-situ; phòng bệnh cây trồng. 1. Mở đầu Trong những năm gần đây, công nghệ nano đã và đang được áp dụng rất hiệu quả vào nhiều lĩnh vực nông nghiệp như: xử lý hạt giống; sản xuất thuốc bảo vệ thực vật, phân bón vi lượng cho cây; bảo quản nông sản sau thu hoạch giúp con người hướng đến nền nông nghiệp sạch và an toàn [1]. Trong lĩnh vực bảo vệ thực vật, công nghệ nano đã có những ứng dụng quan trọng trong sản xuất các chế phẩm phòng trừ bệnh do nấm, vi khuẩn, tuyến trùng, nguyên sinh động vật, tảo và động vật nhỏ gây nên [2]. Một số bệnh phổ biến trên cây ăn quả, cây lương thực như bệnh vàng lá, thối rễ, ghẻ, thán thư, rỉ sắt, loét quả, đốm nâu, khô lá được điều trị hiệu quả bằng các chế phẩm nano đồng, kẽm, bạc, titan oxit, chitosan [3-4]. Kim loại bạc (Ag) từ lâu đã được xem là chất kháng khuẩn tự nhiên và không độc hại, đặc biệt khi ở kích thước nano, khả năng kháng khuẩn của hạt nano bạc tăng mạnh với phổ diệt khuẩn rộng. Các nghiên cứu gần đây cho thấy, hạt nano bạc có tính kháng khuẩn, kháng nấm, chống viêm, kháng virut, chống tạo mạch máu mới và kháng kết tập tiểu cầu. Hạt nano bạc ức chế mạnh các chủng vi khuẩn kháng methicillin như Escherichia coli, Pseudomonas aeruginosa và Staphylococcus aureus bằng cách liên kết với thành tế bào vi khuẩn tích điện âm để làm thay đổi tính thấm và sự ổn định của vỏ tế bào [5]. Đối với các bệnh trên thực vật, các hạt nano bạc có phổ hoạt động mạnh với nhiều loại nấm như Magnaporthe grisea (bệnh đạo ôn), Bipolaris sorokiniana (bệnh thối rễ), Colletotrichum gloeosporioides (bệnh thán thư), Pythium ultimum (bệnh thối đen), Botrytis cinerea (bệnh mốc xám), Scalerotinia sclerotiorum (bệnh mốc trắng), Sphaerotheca pannosa (bệnh phấn trắng), Rhizoctonia solani (bệnh khô vằn), Colletotrichum theae Petch (bệnh thối búp chè), Phytophthora sp (bệnh vàng lá thối rễ) [6]. Tuy nhiên, khi .sử. dụng .các. hạt .nano .bạc .dưới. dạng. dung .dịch .kém. ổn. định .và .dễ bị Email: tamlt@vinhuni.edu.vn (L. T. Tâm) H. Đ. Quang, C.T. T. Dung, N. T. Q. Giang, N. H. Du, L. T. Tâm / Nghiên cứu chế tạo nano bạc - chitosan.. 52 kết tụ [7], nên thường được ổn định bằng các polyme tự nhiên như chitosan, alignate, chất tạo đặc CMC (carboxymethyl cellulose). Điều này đã được A. Murugadoss và cộng sự chứng minh khi sử dụng chitosan vừa làm chất khử, vừa làm chất ổn định khi tổng hợp các hạt nano bạc theo phương pháp in-situ [9], thu được các hạt nano bạc đồng đều, kích thước nhỏ hơn 5 nm. Trong quá trình này, chitosan đóng vai trò là tác nhân kiểm soát sự hình thành các hạt nano, phân tán chúng trong dung môi và chống kết đám, tạo ra hệ keo bạc - chitosan (Ag@CS). Mặt khác, chitosan là polyme tự nhiên có tính kháng vi sinh vật, cảm ứng kháng bệnh của thực vật, kích thích hoặc ức chế sự phát triển của các tế bào, giúp tăng cường hoạt tính của các hạt nano bạc - chitosan. Mặc dù, chitosan có thể khử ion bạc thành các hạt nano bạc, nhưng cần nhiệt độ phản ứng cao (93-95oC) trong thời gian tương đối dài (12 giờ) [9]. Trong nghiên cứu này, chúng tôi dùng phương pháp bọc in-situ để chế tạo hạt nano bạc - Chitosan (Ag@CS) bằng cách sử dụng chitosan vừa làm chất bọc, chất ổn định, vừa làm chất khử. Đặc biệt, để giảm nhiệt độ và thời gian phản ứng tổng hợp Ag@CS, chúng tôi sử dụng ít chất khử NaBH4, giúp giảm chi phí và thời gian chế tạo, điều này rất có ý nghĩa khi định hướng dùng vật liệu này làm các chế phẩm bảo vệ thực vật. Kết quả cho thấy, các hạt nano Ag@CS thu được có dạng hình cầu, đơn phân tán, đồng đều với kích thước trung bình đạt 12,6 nm. 2. Vật liệu và phƣơng pháp nghiên cứu 2.1. Vật liệu Các hóa chất dùng để tổng hợp mẫu nano Ag@CS là các sản phẩm thương mại của hãng BDH Chemicals, Sigma-Aldrich và Merck loại tinh khiết phân tích bao gồm: Silver nitrate (AgNO3), Acetic acid (CH3COOH), Sodium borohydride (NaBH4), nước cất đề ion. 2.2. Phương pháp chế tạo Cân 0,3 gam chitosan (93%) pha trong 50 ml dung dịch axit axetic 2%, khuấy đều ở tốc độ 500 vòng/phút trong thời gian 3 giờ, ở nhiệt độ 50oC (dung dịch 1). Hòa tan 0,2 gam AgNO3 trong 50 ml nước cất, khuấy trong 45 phút ở nhiệt độ phòng (dung dịch 2). Nhỏ từ từ dung dịch 1 vào dung dịch 2, khuấy liên tục trong vòng 30 phút (dung dịch 3). Cuối cùng, 0,05g NaBH4 pha trong 30 ml nước được nhỏ từ từ vào dung dịch 3 thu được dung dịch màu nâu, tiếp tục khuấy trong vòng 3 giờ, ở nhiệt độ khảo sát từ 30 đến 90oC. Ion Ag + trong dung dịch sẽ bị khử tạo thành nano Ag phân tán trong ma trận chitosan để tạo thành phức hợp nano Ag-chitosan (Ag@CS). Để khảo sát sự ảnh hưởng của thời gian khuấy, nhiệt độ lên quá trình tổng hợp, các thí nghiệm được tiến hành khuấy trong thời gian 1 giờ, 3 giờ và 5 giờ, tương ứng với nhiệt độ 30oC, 60oC và 90oC (Hình 1 ... trúc, Viện Vệ sinh dịch tễ TW). Phân bố kích thước và đường kính trung bình của hạt được tính toán bằng phần mềm công cụ hình ảnh Java (ImageJ), dựa trên dữ liệu trung bình 50-100 hạt Trường Đại học Vinh Tạp chí khoa học, Tập 49 - Số 4A/2020, tr. 51-59 53 từ kết quả ảnh TEM. Phổ UV-Vis của các mẫu được ghi trên máy quang phổ Libra S80 Libra (Biochrom - Anh), và thành phần nguyên tố trong sản phẩm được xác định bằng phương pháp hiển vi điện tử quét (SEM) với đầu dò tán xạ năng lượng tia X (EDX, Oxford Instruments - Anh) trên thiết bị JSM - 6510LV (Jeol - Nhật Bản) (Viện Kỹ thuật nhiệt đới, Viện Hàn lâm Khoa học và Công nghệ Việt Nam). Phân bố kích thước hạt và độ bền thế zeta của các mẫu trong nghiên cứu được xác định bằng phương pháp tán xạ laser động (Dynamic Light Scattering-DLS) trên thiết bị Zetasize-Nano ZS của hãng Malvern-Anh (Viện Khoa học vật liệu, Viện Hàn lâm Khoa học và Công nghệ Việt Nam). Hình 1: Quy trình tổng hợp hạt nano Ag@CS 3. Kết quả nghiên cứu 3.1. Ảnh hưởng của thời gian đến quá trình tổng hợp vật liệu Các mẫu Ag@CS ký hiệu Ag@CS-1h, Ag@CS-3h, Ag@CS-5h tương ứng với thời gian phản ứng tăng dần 1 giờ, 3 giờ và 5 giờ tại nhiệt độ phản ứng 60oC, được thể hiện trong Hình 2. Kết quả cho thấy, khi tăng thời gian phản ứng từ 1 giờ lên 5 giờ, các hạt nano Ag@CS thu được có kích thước tăng nhưng độ đồng đều của các hạt khác nhau. Cụ thể, khi tiến hành phản ứng trong 1 giờ, các mẫu Ag@CS-1h (Hình 2a) thu được có hình dạng chưa hoàn thiện, không đồng đều, kích thước trung bình đạt 8,5±3,8 nm. Trong khi đó, khi tiến hành phản ứng trong 3 giờ, các hạt Ag@CS-3h thu được có dạng hình cầu hoàn thiện, H. Đ. Quang, C.T. T. Dung, N. T. Q. Giang, N. H. Du, L. T. Tâm / Nghiên cứu chế tạo nano bạc - chitosan.. 54 đơn phân tán, hạt đồng đều, kích thước trung bình đạt 12,6±2,7 nm. Điều này chứng tỏ, chitosan đóng vai trò rất quan trọng, giúp ổn định hệ hạt và chống kết tụ. Khi tăng thời gian phản ứng, chitosan có vai trò chất khử ion Ag+ thành Ag, đồng thời vi bọc các hạt nano Ag ngay ở kích thước bé. Mặt khác thời gian tăng thì độ tinh thể hóa nano Ag càng cao do đó hạt thu được có kích thước đồng đều hơn, hệ keo tồn tại khá ổn định. Tuy nhiên, khi tiếp tục tăng thời gian phản ứng của hệ lên 5 giờ, kích thước của các hạt nano Ag@CS thu được tiếp tục tăng, trung bình đạt 14,8±4,8 nm. Các hạt Ag@CS-5h thu được có hiện tượng kết đám, biến động kích thước lớn, không đồng đều. Kết quả này cũng phù hợp với một số công bố về ảnh hưởng của thời gian đến sự hình thành các hạt nano Ag, khi thời gian phản ứng tăng kích thước hạt tăng [8]. Như vậy, thời gian phản ứng có ảnh hưởng lớn đến hình dạng và kích thước các hạt nano Ag@CS thu được. Các hạt Ag@CS có kích thước đồng đều, đơn phân tán khi tiến hành phản ứng ở 3 giờ. Điều này giúp giảm đáng kể thời gian cần thiết để tiến hành phản ứng, so với khi chỉ dùng chitosan làm chất khử (phải tiến hành trong 12 giờ, theo kết quả công bố của nhóm A. Murugadoss và cs. [9]). Do đó, chúng tôi chọn thời gian thực hiện phản ứng là 3 giờ cho các nghiên cứu tiếp theo. Hình 2: Ảnh TEM của các mẫu Ag@CS-1h (a), Ag@CS-3h (b), Ag@CS-5h(c) tương ứng với thời gian phản ứng 1 giờ (a), 3 giờ (b), 5 giờ (c) và (d) giản đồ phân bố kích thước hạt Trường Đại học Vinh Tạp chí khoa học, Tập 49 - Số 4A/2020, tr. 51-59 55 3.2. Ảnh hưởng của nhiệt độ đến quá trình tổng hợp vật liệu Các mẫu Ag@CS ký hiệu Ag@CS-30oC, Ag@CS-60oC, Ag@CS-90oC tương ứng với nhiệt độ phản ứng tăng dần 30oC, 60oC và 90oC trong thời gian phản ứng 3h, được thể hiện trong Hình 3. Hình 3: Ảnh TEM của các mẫu Ag@CS-30oC, Ag@CS-60oC, Ag@CS-90oC tương ứng với nhiệt độ phản ứng 30oC (a) , 60oC (b), 90 oC (c) và (d) giản đồ phân bố kích thước hạt Kết quả cho thấy, khi nhiệt độ phản ứng tăng từ 30oC lên 90oC, vật liệu thu được có kích thước trung bình thay đổi không nhiều nhưng mức độ phân tán về kích thước hạt và độ đồng đều là khác nhau. Cụ thể, tại nhiệt độ 30oC, các hạt Ag@CS-30oC thu được có kích thước trung bình đạt 11,5 nm, biến động lớn trong khoảng 6,9 đến 16,1 nm; trong khi nếu nhiệt độ tăng lên 60oC các hạt Ag@CS-60oC thu được có độ phân bố kích thước hẹp hơn, dạng hình cầu và đồng đều hơn, với kích thước chủ yếu trong khoảng từ 9,9 nm đến 15,3 nm. Điều này có thể giải thích ở nhiệt độ cao vai trò của chất khử của chitosan đóng góp là đáng kể, mặt khác nhiệt độ cao làm hoàn thiện cấu trúc của các tinh thể nano Ag. Tuy nhiên, khi tăng nhiệt độ lên 90oC, các hạt Ag@CS-90oC có hiện tượng bị kết đám dạng 3 đến 4 hạt với nhau nhưng không đồng đều làm kích thước hạt dao động lớn trong khoảng từ 9,3 đến 18,3 nm. Vì vậy, chúng tôi chọn nhiệt độ tối ưu cho các phản ứng tổng hợp hạt Ag@CS là 600C, điều này giúp tiết kiệm chi phí khi định hướng ứng dụng hệ vật liệu này làm chế phẩm bảo vệ thực vật. H. Đ. Quang, C.T. T. Dung, N. T. Q. Giang, N. H. Du, L. T. Tâm / Nghiên cứu chế tạo nano bạc - chitosan.. 56 3.3. Thành phần và tính chất của vật liệu nano Ag@CS Thành phần và các nguyên tố cấu thành vật liệu nano Ag@CS xác định bằng phương pháp phổ tán xạ năng lượng tia X (EDX) mẫu Ag@CS-3h60oC tổng hợp ở nhiệt độ tối ưu 60oC trong thời gian 3 giờ, kết quả thể hiện trong Hình 4. Hình 4: Phổ EDX của mẫu Ag@CS-3h60oC Kết quả chụp cho thấy, trong Ag@CS-3h60oC thu được có hàm lượng Ag chiếm 9,01% về trọng lượng, trong khi O chiếm 84,53%, C chiếm 1,77% và N chiếm 4,69%. Điều này rất có ý nghĩa khi sử dụng nano Ag cho các chế phẩm bảo vệ thực vật, phòng trừ sâu bệnh vì chỉ cần hàm lượng nhỏ Ag cũng có thể cho hiệu quả diệt trừ bệnh cao. Hình 5: Phổ UV-Vis của mẫu Ag@CS (a) và (b) sự phân bố kích thước dung dịch nano bạc - chitosan chế tạo bằng phương pháp in-situ Các đặc tính quang học của các hạt nano bạc hình cầu phụ thuộc nhiều vào đường kính của hạt nano. Phổ UV-Vis của các hạt nano Ag có kích thước dưới 20 nm thì đều cho cộng hưởng plasmon bề mặt (Surface plasmon resonance-SPR) như nhau. Hình 5a cho thấy đỉnh plasmon bề mặt của các mẫu tổng hợp ở các điều kiện khác nhau, tương ứng với kích thước hạt 11,5 nm; 12,6 nm và 13,8 nm đều có đỉnh hấp thụ cực đại tại 396 Trường Đại học Vinh Tạp chí khoa học, Tập 49 - Số 4A/2020, tr. 51-59 57 nm và 400 nm. Điều này có thể giải thích do các quả cầu nano nhỏ hơn chủ yếu hấp thụ ánh sáng và có các cực đại gần 400 nm, trong khi các quả cầu nano lớn hơn thể hiện sự tán xạ tăng lên và có các cực đại mở rộng và dịch chuyển về phía bước sóng dài hơn (được gọi là chuyển dịch đỏ). Kết quả này cũng phù hợp với các kết quả đã được công bố của Paramelle và cộng sự [10,11]. Rõ ràng từ Hình 5a cho thấy không có đỉnh SPR nào được quan sát ở hơn 500 nm, cho thấy rằng hầu hết các Ag@CS thu được có kích thước nhỏ và hình thái tương tự. Kết quả phân tích sự phân bố kích thước hạt bằng phương pháp pháp DLS cho 1 đỉnh duy nhất (tương ứng với kích thước cỡ hạt 24,5 nm) (Hình 5b), hoàn toàn không có sự kết khối, tạo ra các tập hợp hạt ở vùng kích thước cỡ hạt chủ yếu tập trung trong khoảng 15 đến 40 nm. Điều này khẳng định các tiểu phân nano có kích thước bé và phân tán đồng đều. Kết quả kích thước hạt thu được từ ảnh TEM nhỏ hơn so với kết quả thu được từ kết quả phân tích DLS là hoàn toàn phù hợp, vì kết quả phân tích DLS (phương pháp tán xạ ánh sáng động) là kích thước động, thu được từ một tập hợp hạt rất lớn, trong khi ảnh TEM chỉ quan sát một vùng nhỏ, số lượng hạt được quan sát ít, kích thước hạt thu được là kích thước tĩnh. Mặt khác, kích thước hạt của các mẫu bọc đo trong môi trường chất lỏng (đo DLS) có kích thước lớn hơn khi chụp ảnh TEM có thể được giải thích: khi đo hạt trong môi trường chất lỏng, các polime ưu nước sẽ tương tác với nước, làm cho các hạt có kích thước lớn hơn. Trong hệ sản phẩm dạng lỏng, thế zeta thường được sử dụng như là một ngưỡng để đánh giá cho sự ổn định. Thế zeta thể hiện mức độ đẩy giữa các hạt tích điện cùng dấu gần nhau trong hệ phân tán. Đối với các phân tử và các hạt đủ nhỏ, thế zeta cao (âm hoặc dương) sẽ cho độ ổn định cao, hệ phân tán sẽ chống lại sự keo tụ, kết đám. Thế zeta đo được của mẫu đạt +26,4 mV (Hình 6a). Như vậy, với kết quả đo được thì thế zeta đạt được là khá tối ưu, khẳng định tính bền vững và ổn định của hệ dung dịch nano. Trong nghiên cứu này, tính ổn định lâu dài theo thời gian của các hạt nano Ag dạng keo đã được theo dõi bằng kỹ thuật đo điện thế zeta, từ đó cho biết sự thay đổi điện tích bề mặt theo thời gian (Hình 6). Giá trị thế zeta của Ag@CS dạng keo được điều chế bằng phương pháp bọc in-situ sau 3 tháng có giá trị tương ứng là +25,6 mV. Điều đó cho thấy rằng dung dịch nano Ag@CS được chế tạo được có độ ổn định tốt. Kết quả này cho thấy sự ổn định lâu dài của các chất keo tương ứng, mở ra tiềm năng cho việc sử dụng hệ vật liệu này làm chế phẩm bảo vệ thực vật. Hình 6: Thế zeta của dung dịch nano bạc - chitosan chế tạo bằng phương pháp in-situ sau các khoảng thời gian: (a) sau chế tạo; (b) sau 3 tháng H. Đ. Quang, C.T. T. Dung, N. T. Q. Giang, N. H. Du, L. T. Tâm / Nghiên cứu chế tạo nano bạc - chitosan.. 58 4. Kết luận Bằng phương pháp bọc in-situ sử dụng chitosan làm chất ổn định, đồng thời là chất khử chúng tôi thu được các mẫu Ag@CS có kích thước nhỏ, hạt đồng đều, phân tán tốt trong nước và ổn định. Kết quả cho thấy, nhiệt độ và thời gian phản ứng có ảnh hưởng đáng kể đến sự hình thành các hạt nano Ag@CS, kích thước hạt và độ đồng đều tăng khi nhiệt độ và thời gian phản ứng tăng nhưng đạt đến một mức độ nhất định, sự tuyến tính này bị phá vỡ, các hạt có xu hướng kết tụ làm cho hạt có kích thước lớn hơn. Bằng thực nghiệm, chúng tôi thu được các hạt mẫu Ag@CS-3h60oC có điều kiện tổng hợp tối ưu ở 60oC trong thời gian 3 giờ có kích thước trung bình đạt 12,6 nm, hàm lượng Ag chiếm 9,01%. Sản phẩm có độ ổn định cao sau 3 tháng và có triển vọng ứng dụng làm các chế phẩm bảo vệ thực vật, phòng trừ nấm và bệnh hại cây trồng. Lời cảm ơn: Công trình này được thực hiện với sự hỗ trợ về kinh phí của đề tài nghiên cứu khoa học cấp Tỉnh Nghệ An mã số 01/2020/HĐ-NCKHNA. TÀI LIỆU THAM KHẢO [1] H. Chhipa, “Nanofertilizers and nanopesticides for agriculture,” Environmental Chemistry Letters, Vol. 15, pp. 15-22, 2017. [2] I. O. Adisa, V. L. R. Pullagurala, J. R. Peralta-Videa, C. O. Dimkpa, W. H. Elmer, J. Gardea-Torresdey, and J. C. White, “Recent advances in nano-enabled fertilizers and pesticides: A critical review of mechanisms of action,” Environmental Science: Nano, Vol. 6, pp. 2002- 2030, 2019. [3] X. He, H. Deng and H. Hwang, “The current application of nanotechnology in food and agriculture,” Journal of Food and Drug Analysis, Vol. 27, No. 1, pp. 1-21, 2019. [4] E. Worrall, A. Hamid, K. Mody, N. Mitter and H. Pappu, “Nanotechnology for Plant Disease Management,” Agronomy, Vol. 8, No. 12, pp. 1-24, 2018. [5] R. Kalaivani, M. Maruthupandy, T. Muneeswaran, A. Hameedha Beevi, M. Anand, C. M. Ramakritinan and A. K. Kumaraguru, “Synthesis of chitosan mediated silver nanoparticles (Ag NPs) for potential antimicrobial applications,” Frontiers in Laboratory Medicine, Vol. 2, No. 1, pp. 30-35, 2018. [6] X.-F. Zhang, Z.-G. Liu, W. Shen and S. Gurunathan, “Silver Nanoparticles: Synthesis, Characterization, Properties, Applications, and Therapeutic Approaches”, International Journal of Molecular Sciences, Vol. 17, No. 9, pp. 1-34, 2016. [7] D. K. Bhui, H. Bar, P. Sarkar, G. P. Sahoo, S. P. De and A. Misra, “Synthesis and UV-vis spectroscopic study of silver nanoparticles in aqueous SDS solution,” Journal of Molecular Liquids, Vol. 145, No. 1, pp. 33-37, 2009. [8] K. Patel, M. P. Deshpande, V. P. Gujarati, and S. H. Chaki, “Effect of Heating Time Duration on Synthesis of Colloidal Silver Nanoparticles,” Advanced Materials Research, Vol. 1141, pp. 14-18, 2016. [9] A. Murugadoss and A. Chattopadhyay, “A green chitosan-silver nanoparticle composite as a heterogeneous as well as micro-heterogeneous catalyst,” Nanotechnology, Vol. 19, pp. 1-9, 2008. Trường Đại học Vinh Tạp chí khoa học, Tập 49 - Số 4A/2020, tr. 51-59 59 [10] A. Amirjani, N. N. Koochak and D. F. Haghshenas, “Investigating the Shape and Size-Dependent Optical Properties of Silver Nanostructures Using UV-vis Spectroscopy,” J. Chem. Educ., Vol. 96, No. 11, pp. 2584-2589, 2019. [11] D. Paramelle, A. Sadovoy, S. Gorelik, P. Free, J. Hobley and D. G. Fernig, “A rapid method to estimate the concentration of citrate capped silver nanoparticles from UV- visible light spectra,” The Analyst, Vol. 139, No. 19, pp. 4855-4861, 2014. SUMMARY STUDY ON FABRICATION AG-CHITOSAN NANOPARTICLES BY IN-SITU ENCAPSULATION METHOD FOR THE PREPARATION OF NANOPROTECTIVE APPLIED IN PLANT PROTECTION Ho Dinh Quang (1) , Chu Thi Thuy Dung (2) , Nguyen Thi Quynh Giang (1) , Nguyen Hoa Du (2) , Le The Tam (1) 1 School of Biochemical Technology - Environment, Vinh University 2 School of Natural Sciences Education, Vinh University Received on 09/10/2020, accepted for publication on 13/12/2020 Silver - chitosan (Ag@CS) nanoparticles were synthesized by in-situ encapsulation method, which achieved an average size of 12.6 nm, uniform particles, well-dispersed particles in water and stable. Experimental results show that the temperature and reaction time have greatly affected on the formation of Ag@CS nanoparticles, particle size and uniformity. The optimal temperature is 60 o C during 3 hours to obtain Ag@CS nanoparticles with Ag content of 9.01%. The zeta potential of Ag@CS in the colloidal form obtained after 3 months has a value of +25.6 mV, proving that Ag@CS particles have good stability, opening up the potential for using this material system as a plant protection product. Keywords: Nano silver - chitosan; in-situ encapsulation method; plant protection products.
File đính kèm:
 nghien_cuu_che_tao_nano_bac_chitosan_theo_phuong_phap_boc_in.pdf
nghien_cuu_che_tao_nano_bac_chitosan_theo_phuong_phap_boc_in.pdf

