Kết quả điều trị ung thư biểu mô tuyến phần xa dạ dày giai đoạn II, III bằng phẫu thuật và xạ-hóa bổ trợ sau mổ
Đánh giá kết quả điều trị về tình hình tái phát, di căn, thời gian sống thêm toàn bộ, thời giansống thêm bệnh không tiến triển và các biến chứng của điều trị ung thư biểu mô tuyến phần xa dạ dày giai đoạn II-II bằng xạ - hóa bổ trợ sau mổ.

Trang 1

Trang 2
Trang 3
Trang 4
Trang 5
Trang 6

Trang 7

Trang 8
Bạn đang xem tài liệu "Kết quả điều trị ung thư biểu mô tuyến phần xa dạ dày giai đoạn II, III bằng phẫu thuật và xạ-hóa bổ trợ sau mổ", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Kết quả điều trị ung thư biểu mô tuyến phần xa dạ dày giai đoạn II, III bằng phẫu thuật và xạ-hóa bổ trợ sau mổ

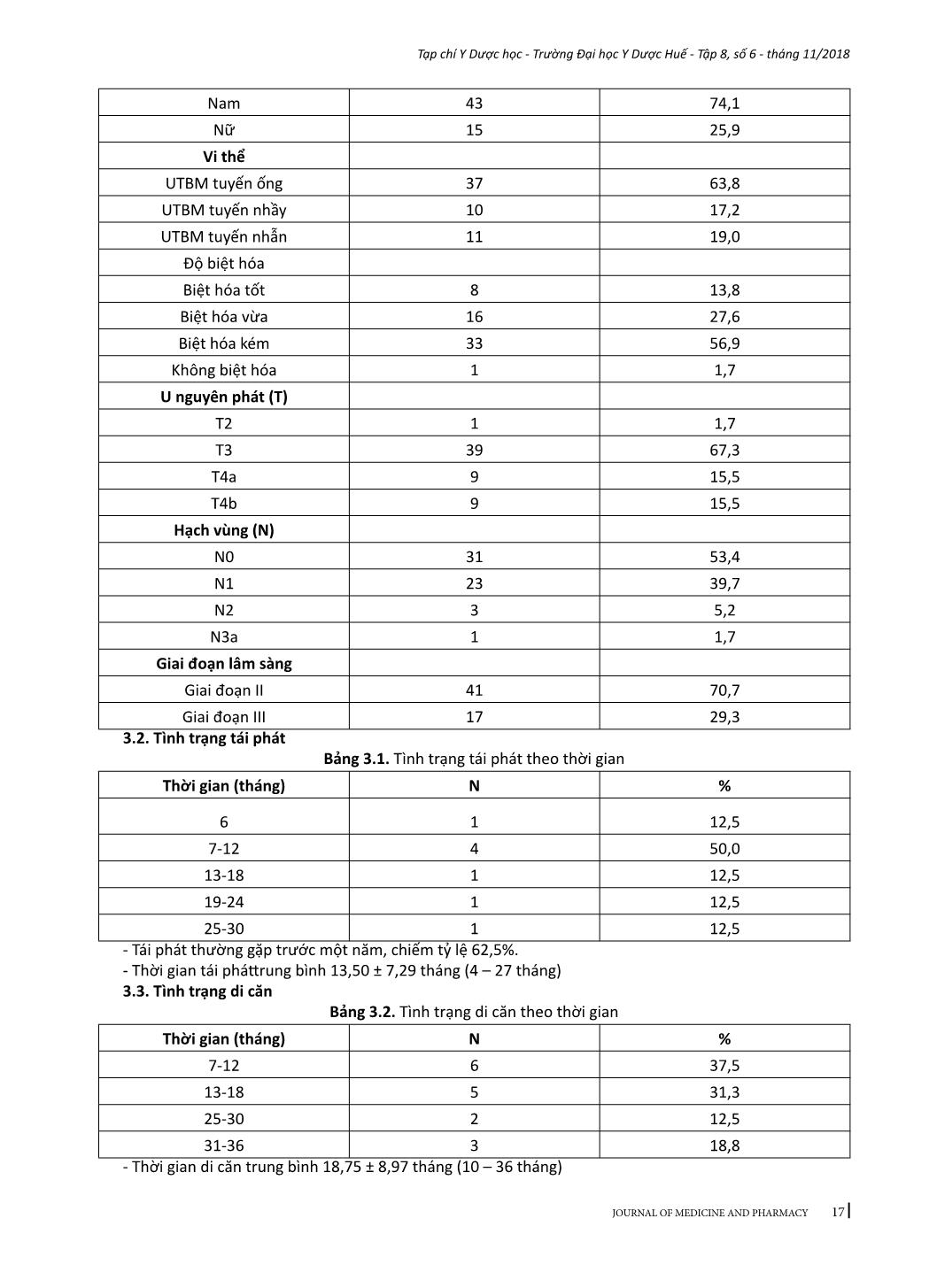
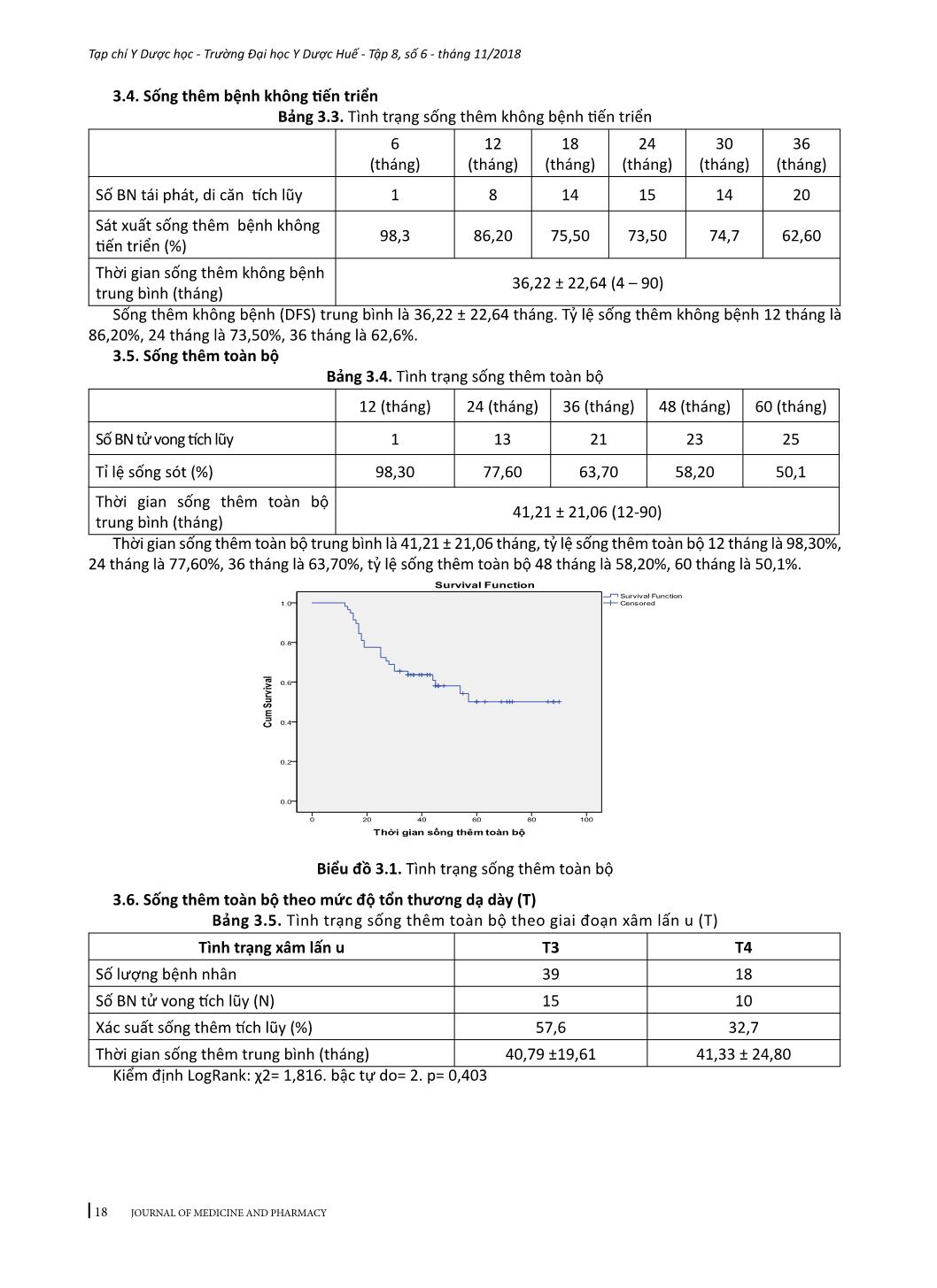
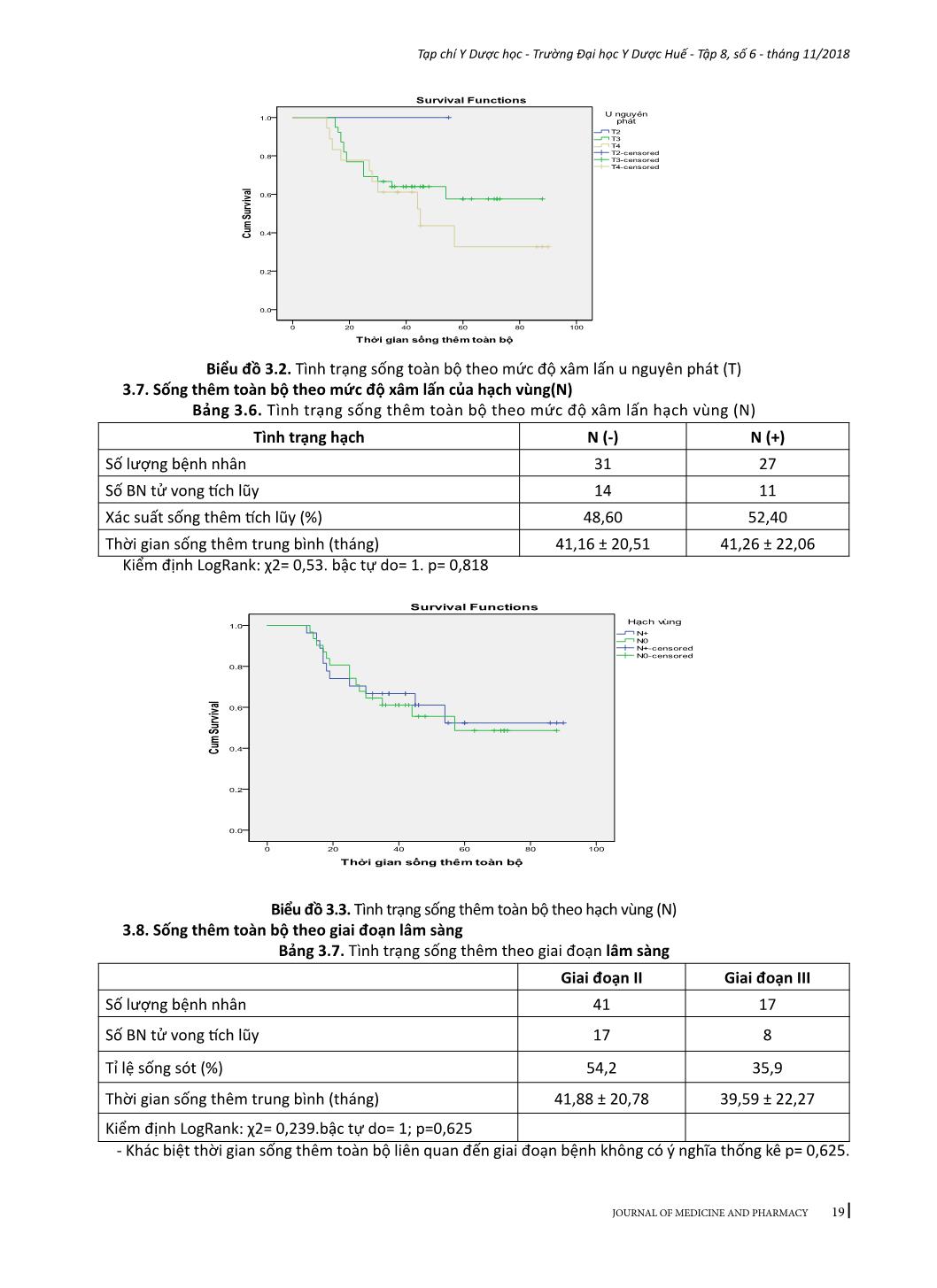
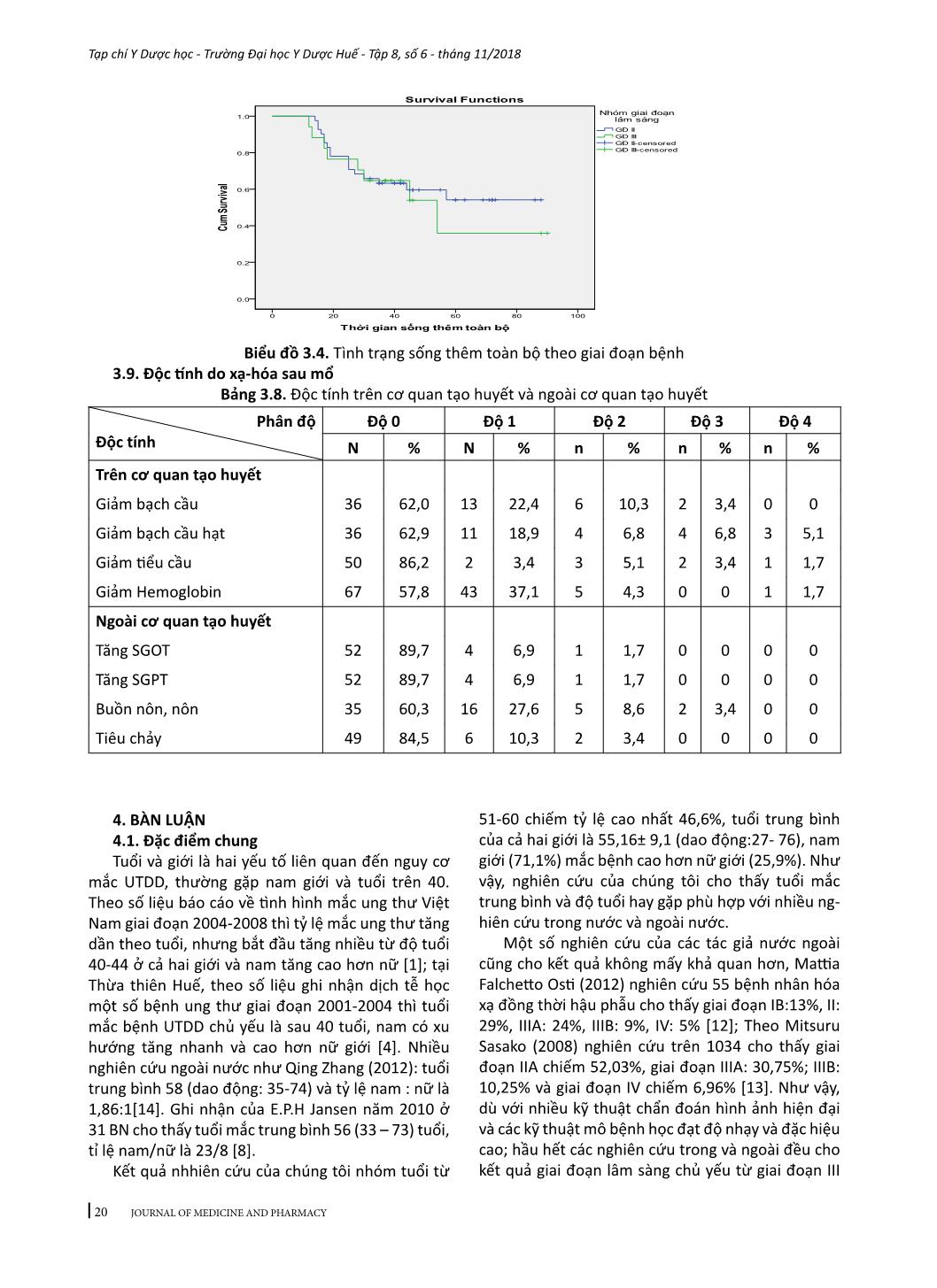
15 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY KẾT QUẢ ĐIỀU TRỊ UNG THƯ BIỂU MÔ TUYẾN PHẦN XA DẠ DÀY GIAI ĐOẠN II, III BẰNG PHẪU THUẬT VÀ XẠ-HÓA BỔ TRỢ SAU MỔ Phan Cảnh Duy1, Phạm Anh Vũ2 (1) Nghiên cứu sinh Trường Đại học Y Dược, Đại học Huế; (2) Bộ môn Ngoại, Trường Đại học Y Dược, Đại học Huế Tóm tắt Đặt vấn đề: Đánh giá kết quả điều trị về tình hình tái phát, di căn, thời gian sống thêm toàn bộ, thời giansống thêm bệnh không tiến triển và các biến chứng của điều trị ung thư biểu mô tuyến phần xa dạ dày giai đoạn II-II bằng xạ - hóa bổ trợ sau mổ. Đối tượng và phương pháp: Nghiên cứu tiến cứu 58 bệnh nhân ung thư biểu mô tuyến dạ dày giai đoạn II - III, đã được mổ cắt bán phần xa dạ dày và vét hạch D1 hoặc D2, hoàn thành phác đồ xạ - hóa đồng thời sau mổ với capecitabin và hóa trị từ 4 đến 6 chu kỳ theo phác đồ EOX tại Trung tâm Ung bướu - bệnh viện Trung ương Huế từ tháng 01/2013 đến tháng 12/2015. Kết quả: Tuổi trung bình 55,16 ± 9,1, tỷ lệ nam/nữ là 3/1, tái phát thường gặp trước một năm sau điều trị (62,5%), thời gian tái phát, di căn trung bình lần lượt là 13,50 ± 7,29 tháng và 18,75 ± 8,97 tháng. Sống thêm toàn bộ trung bình là 41,21 ± 21,06. Sống thêm không bệnh trung bình 36,22 ± 22,64 tháng. Sống thêm toàn bộ trung bình theo giai đoạn: giai đoạn II 41,88 ± 20,78 tháng; giai đoạn III 39,59 ± 22,27 tháng. Sống thêm toàn bộ trung bình theo mức độ xâm lấn của u nguyên phát: u T3 là 40,79 ± 19,61 tháng; u T4 là 41,33 ± 24,80 tháng. Sống thêm toàn bộ trung bình theo mức độ xâm lấn của hạch: N(-) 41,16 ± 20,51 tháng, N(+) 41,26 ± 22,06 tháng. Độc tính ghi nhận được: giảm bạch cầu chủ yếu độ 1 và 2 (33,6%), giảm bạch cầu hạt phần lớn ở độ 1 và 2 (26,8%); giảm tiểu cầu cũng chủ yếu độ 1 và 2 (8,6%); tỷ lệ giảm hemoglobin độ 1 và 2 khá cao (41,4%); độc tính trên hệ tiêu hóa là buồn nôn - nôn, tiêu chảy chủ yếu ở độ 1 và 2. Kết luận: Xạ - hóa bổ trợ sau mổ ung thư biểu mô tuyến phần xa dạ dày giai đoạn tiến triển tại chỗ giúp cải thiện tỷ lệ tái phát tại chỗ và tại vùng với độc tính chấp nhận được. Từ khóa: Ung thư biểu mô tuyến phần xa dạ dày, xạ hóa sau mổ Abstract THE RESULTS OF TREATMENT OF STAGE II-III DISTAL GASTRIC ADENOCARCINOMA UNDERWENT SURGERY AND POSTOPERATIVE CHEMORADIATION THERAPY Phan Canh Duy1, Pham Anh Vu2 (1) PhD Students of Hue University of Medicine and Pharmacy, Hue University (2) Dept. of Surgery, Hue University of Medicine and Pharmacy, Hue University Objectives: To evaluate the survival outcome, patterns of failure, and complications in patients treated with postoperative chemoradiation therapy in stages II-III of distal gastric cancer. Materials & methods: Prospective study on 58 patients with stages II-III gastric adenocarcinoma, underwent distal gastrectomy and D1 or D2 dissection, completed post operative chemoradiation therapy with capecitabine and 4-6 cycles with EOX regimen at Oncology center of Hue central hospital from 01/2013 to 12/2015. Results: Mean age was 55.16 ± 9.1, male/female ratio: 3/1, recurrence was common in the first year after treatment (62.5%), the average time of recurrence and metastasis were 13.50 ± 7.29 months and 18.75 ± 8.97 months, respectively. The mean overall survival was 41.21 ± 21.06 months. The mean disease free survival was 36.22 ± 22.64 months. The mean overall survival: stage II was 41.88 ± 20.78 months; stage III was 39.59 ± 22.27. The mean overall survival for extention of primary tumors: T3 was 40.79 ± 19.61 months; T4 was 41.33 ± 24.80 months. The mean overall survival for extensive of lymph nodes: N (-) was 41.16 ± 20.51 months, N (+) was 41.26 ± 22.06 months. Toxicity levels recorded as follow: leukopenia was mainly on grade 1 and 2 (33.6%), neutropenia was mostly on grade 1 and 2 (26.8%), as well as thrombocytopenia (8.6%); hemoglobin decrease was on grade 1 and 2 in most cases (41.4%); toxicity symptoms on digestive system like nausea-vomitting, diarrhea was mainly on grade 1 and 2. Conclusion: Postoperative chemoradiation therapy helps to improve local and regional recurrence in locally advanced gastric cancer with acceptable toxicities. Key words: Distal gastric adenocarcinoma, postoperative chemoradiation therapy - Địa chỉ liên hệ: Phan Cảnh Duy, email: drphancanhduy@gmail.com - Ngày nhận bài: 9/10/2018, Ngày đồng ý đăng: 10/11/2018, Ngày xuất bản: 17/11/2018 16 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY 1. ĐẶT VẤN ĐỀ Ung thư dạ dày (UTDD) là bệnh lý thường gặp nhất trong ung thư đường tiêu hóa, theo Globo- can (2012) ghi nhận đứng thứ năm trong 10 loại ung thư phổ biến trên thế giới; tỉ lệ tử vong chuẩn theo tuổi theo giới nam và nữ là 23,6/100.000 dân và 21,9/100.000 dân [10]. Ghi nhận ung thư tại Việt Nam công bố năm 2010, hàng năm có trên 10.000 trường hợp mới mắc; ung thư dạ dày đứng thứ 2 ở nam sau ung thư phổi (tỷ lệ mắc theo tuổi 24,5/100.000 dân) và đứng thứ 3 ở nữ sau ung thư vú và ung thư cổ tử cung (tỷ lệ mắc theo tuổi 12,2/100.000 dân) [1]. Phẫu thuật là phương pháp điều trị cơ bản, kỹ thuật phẫu thuật ung thư dạ dày ngày càng tiến bộ, nhưng kết quả sống thêm toàn bộ của bệnh nhân ung thư dạ dày thể tiến triển tại chỗ vẫn thấp, tỷ lệ sống chung 05 năm chỉ đạt 8-34% [7]. Tại Mỹ và một số quốc gia, điều trị bổ trợ bằng xạ - hóa sau phẫu thuật được chấp nhận là phác đồ điều trị chuẩn đối với ung thư dạ dày giai đoạn tiến triển tại chỗ (u xâm lấn đến thanh mạc hoặc có di căn hạch vùng)[9]. Nhằm cải thiện thời gian sống thêm, tại Trung tâm Ung bướu -Bệnh viện Trung ương Huế, chúng tôi đã nghiên cứu phác đồ điều trị bổ trợ hóa – xạ đồng thời và hóa trị cho các bệnh nhân UTDD giai đoạn II và III đã phẫu thuật. Chúng tôi đã tiến hành nghiên cứu này nhằm mục tiêu: Đánh giá kết quả điều trị về tình trạng tái phát, di căn, thời gian sốn ... bệnh (DFS) trung bình là 36,22 ± 22,64 tháng. Tỷ lệ sống thêm không bệnh 12 tháng là 86,20%, 24 tháng là 73,50%, 36 tháng là 62,6%. 3.5. Sống thêm toàn bộ Bảng 3.4. Tình trạng sống thêm toàn bộ 12 (tháng) 24 (tháng) 36 (tháng) 48 (tháng) 60 (tháng) Số BN tử vong tích lũy 1 13 21 23 25 Tỉ lệ sống sót (%) 98,30 77,60 63,70 58,20 50,1 Thời gian sống thêm toàn bộ trung bình (tháng) 41,21 ± 21,06 (12-90) Thời gian sống thêm toàn bộ trung bình là 41,21 ± 21,06 tháng, tỷ lệ sống thêm toàn bộ 12 tháng là 98,30%, 24 tháng là 77,60%, 36 tháng là 63,70%, tỷ lệ sống thêm toàn bộ 48 tháng là 58,20%, 60 tháng là 50,1%. Biểu đồ 3.1. Tình trạng sống thêm toàn bộ 3.6. Sống thêm toàn bộ theo mức độ tổn thương dạ dày (T) Bảng 3.5. Tình trạng sống thêm toàn bộ theo giai đoạn xâm lấn u (T) Tình trạng xâm lấn u T3 T4 Số lượng bệnh nhân 39 18 Số BN tử vong tích lũy (N) 15 10 Xác suất sống thêm tích lũy (%) 57,6 32,7 Thời gian sống thêm trung bình (tháng) 40,79 ±19,61 41,33 ± 24,80 Kiểm định LogRank: χ2= 1,816. bậc tự do= 2. p= 0,403 19 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY Biểu đồ 3.2. Tình trạng sống toàn bộ theo mức độ xâm lấn u nguyên phát (T) 3.7. Sống thêm toàn bộ theo mức độ xâm lấn của hạch vùng(N) Bảng 3.6. Tình trạng sống thêm toàn bộ theo mức độ xâm lấn hạch vùng (N) Tình trạng hạch N (-) N (+) Số lượng bệnh nhân 31 27 Số BN tử vong tích lũy 14 11 Xác suất sống thêm tích lũy (%) 48,60 52,40 Thời gian sống thêm trung bình (tháng) 41,16 ± 20,51 41,26 ± 22,06 Kiểm định LogRank: χ2= 0,53. bậc tự do= 1. p= 0,818 Biểu đồ 3.3. Tình trạng sống thêm toàn bộ theo hạch vùng (N) 3.8. Sống thêm toàn bộ theo giai đoạn lâm sàng Bảng 3.7. Tình trạng sống thêm theo giai đoạn lâm sàng Giai đoạn II Giai đoạn III Số lượng bệnh nhân 41 17 Số BN tử vong tích lũy 17 8 Tỉ lệ sống sót (%) 54,2 35,9 Thời gian sống thêm trung bình (tháng) 41,88 ± 20,78 39,59 ± 22,27 Kiểm định LogRank: χ2= 0,239.bậc tự do= 1; p=0,625 - Khác biệt thời gian sống thêm toàn bộ liên quan đến giai đoạn bệnh không có ý nghĩa thống kê p= 0,625. 20 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY Biểu đồ 3.4. Tình trạng sống thêm toàn bộ theo giai đoạn bệnh 3.9. Độc tính do xạ-hóa sau mổ Bảng 3.8. Độc tính trên cơ quan tạo huyết và ngoài cơ quan tạo huyết Phân độ Độc tính Độ 0 Độ 1 Độ 2 Độ 3 Độ 4 N % N % n % n % n % Trên cơ quan tạo huyết Giảm bạch cầu 36 62,0 13 22,4 6 10,3 2 3,4 0 0 Giảm bạch cầu hạt 36 62,9 11 18,9 4 6,8 4 6,8 3 5,1 Giảm tiểu cầu 50 86,2 2 3,4 3 5,1 2 3,4 1 1,7 Giảm Hemoglobin 67 57,8 43 37,1 5 4,3 0 0 1 1,7 Ngoài cơ quan tạo huyết Tăng SGOT 52 89,7 4 6,9 1 1,7 0 0 0 0 Tăng SGPT 52 89,7 4 6,9 1 1,7 0 0 0 0 Buồn nôn, nôn 35 60,3 16 27,6 5 8,6 2 3,4 0 0 Tiêu chảy 49 84,5 6 10,3 2 3,4 0 0 0 0 4. BÀN LUẬN 4.1. Đặc điểm chung Tuổi và giới là hai yếu tố liên quan đến nguy cơ mắc UTDD, thường gặp nam giới và tuổi trên 40. Theo số liệu báo cáo về tình hình mắc ung thư Việt Nam giai đoạn 2004-2008 thì tỷ lệ mắc ung thư tăng dần theo tuổi, nhưng bắt đầu tăng nhiều từ độ tuổi 40-44 ở cả hai giới và nam tăng cao hơn nữ [1]; tại Thừa thiên Huế, theo số liệu ghi nhận dịch tễ học một số bệnh ung thư giai đoạn 2001-2004 thì tuổi mắc bệnh UTDD chủ yếu là sau 40 tuổi, nam có xu hướng tăng nhanh và cao hơn nữ giới [4]. Nhiều nghiên cứu ngoài nước như Qing Zhang (2012): tuổi trung bình 58 (dao động: 35-74) và tỷ lệ nam : nữ là 1,86:1[14]. Ghi nhận của E.P.H Jansen năm 2010 ở 31 BN cho thấy tuổi mắc trung bình 56 (33 – 73) tuổi, tỉ lệ nam/nữ là 23/8 [8]. Kết quả nhhiên cứu của chúng tôi nhóm tuổi từ 51-60 chiếm tỷ lệ cao nhất 46,6%, tuổi trung bình của cả hai giới là 55,16± 9,1 (dao động:27- 76), nam giới (71,1%) mắc bệnh cao hơn nữ giới (25,9%). Như vậy, nghiên cứu của chúng tôi cho thấy tuổi mắc trung bình và độ tuổi hay gặp phù hợp với nhiều ng- hiên cứu trong nước và ngoài nước. Một số nghiên cứu của các tác giả nước ngoài cũng cho kết quả không mấy khả quan hơn, Mattia Falchetto Osti (2012) nghiên cứu 55 bệnh nhân hóa xạ đồng thời hậu phẫu cho thấy giai đoạn IB:13%, II: 29%, IIIA: 24%, IIIB: 9%, IV: 5% [12]; Theo Mitsuru Sasako (2008) nghiên cứu trên 1034 cho thấy giai đoạn IIA chiếm 52,03%, giai đoạn IIIA: 30,75%; IIIB: 10,25% và giai đoạn IV chiếm 6,96% [13]. Như vậy, dù với nhiều kỹ thuật chẩn đoán hình ảnh hiện đại và các kỹ thuật mô bệnh học đạt độ nhạy và đặc hiệu cao; hầu hết các nghiên cứu trong và ngoài đều cho kết quả giai đoạn lâm sàng chủ yếu từ giai đoạn III 21 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY trên 55%, điều này phần nào giải thích tỷ lệ sống thêm toàn bộ của căn bệnh này là thấp. Nghiên cứu của chúng tôi giai đoạn II chiếm tỷ lệ cao nhất với 70,7%, giai đoạn III chiếm 29,3%, chẩn đoán giai đoạn sớm hơn so với nhiều nghiên cứu. 4.2. Tình trạng tái phát tại chỗ, tại vùng và di căn Nghiên cứu Sup Kim (2011) hóa xạ đồng thời 80 bệnh nhân với 5FU-LV, trung vị thời gian theo dõi 48 tháng (dao động: 3 - 83 tháng) cho kết quả tái phát tại chỗ 6%[15]. Nghiên cứu của Qing Zhang (2012) hóa xạ đồng thời với 5FU-LV kết quả tái phát tại miệng nối: 17,6% [14] Nghiên cứu của chúng tôi thấy tỉ lệ chỉ tái phát chiếm 13,79% (8/58), thời gian tái phát trung bình 13,50 ± 7,29 tháng (4 – 27 tháng), tương đương với một số nghiên cứu trong và ngoài nước. Jeeyun Lee (2011) nghiên cứu 458 bệnh nhân cho tỷ lệ di căn xa là 20,4%[11]; Sup Kim (2011) hóa xạ đồng thời 80 bệnh nhân với 5FU-LV, trung vị thời gian theo dõi 48 tháng (dao động: 3-83 tháng) cho kết quả di căn xa là 23%[15]. Kết quả nghiên cứu của chúng tôi ghi nhận tỉ lệ di căn chung 27,58% (16/58); không khác biệt so với các nghiên cứu nước ngoài; diễn tiến nhanh trong 12 – 18 tháng, thời gian di căn trung bình 18,75 ±8,97 tháng. 4.3. Sống thêm sau điều trị Theo ghi nhận của Trịnh Thị Hoa (2009) điều trị bỗ trợ phác đồ ECX cho thấy thời gian sống thêm toàn bộ sau 03 năm là 81,8%[3]. Theo báo cáo trên 138 trường hợp của Vũ Quang Toản và CS (2016) giai đoạn IIB-IIIC cho thấy điều trị bổ trợ phác đồ EOX tỉ lệ sống thêm 03 năm, 04 năm, 05 năm tương ứng 64,5%, 54,2%, 50,8%; thời gian sống thêm trung bình toàn bộ 51±2,3 tháng [5]. Mattia Falchetto Osti (2012) nghiên cứu trên 55 bệnh nhân hóa xạ đồng thời với Capecitabine cho kết quả sống thêm toàn bộ sau 2 năm là 83%, sau 3 năm là 59,3%, sau 5 năm là 48%[12]. Nghiên cứu của chúng tôi, thời gian sống thêm toàn bộ trung bình là 41,21 ± 21,06 tháng, như vậy về kết quả sống thêm toàn bộ của chúng tôi tương đương với các nghiên cứu có uống Capecitabin. Báo cáo của Vũ Quang Toản và CS (2016) ghi nhận tỉ lệ sống không bệnh sau 03 năm, 04 năm, 05 năm tương ứng là 53,9%, 49,8% và 42,9% [5]. Theo Mattia Falchetto Osti (2012) thời gian sống thêm không bệnh sau 2 năm là 75%, sau 3 năm là 60% và sau 5 năm là 44,5%[12]. Theo Qing Zhang (2012) sống thêm không bệnh sau 5 năm là 15% [14]. Trong nghiên cứu của chúng tôi thời gian sống thêm không bệnh sau 1, 2, 3 năm lần lượt là 86,2%,73,5% và 62,6% cao hơn các nghiên cứu trước đây khi bổ trợ xạ hóa hay hóa trị. Nguyễn Tuyết Mai (2010) nghiên cứu hóa trị bổ trợ bệnh nhân từ giai đoạn II-IV với phác đồ ECX cho kết quả sống thêm toàn bộ sau 2 năm theo giai đoạn II: 100%, giai đoạn IIIa: 80,9%, giai đoạn IIIb: 75%. Park S. H (2003) nghiên cứu 290 bệnh nhân giai đoạn Ib-IV hóa xạ đồng thời với 5FU-LV, trung vị thời gian theo dõi là 49 tháng cho kết quả sống thêm sau 3 năm theo giai đoạn lâm sàng: giai đoạn I là 94%, giai đoạn II: 76%, giai đoạn III: 54% và giai đoạn IV là 13% (p< 0,001) [106]. Kết quả nghiên cứu của chúng tôi thời gian sống thêm toàn bộ của giai đoạn II là 54,2% và giai đoạn III là 35,9%; không khác biệt với các kết quả nghiên cứu trong và ngoài nước. Thời gian sống thêm toàn bộ trung bình giai đoạn II: 41,88 ± 20,78 tháng, giai đoạn III: 39,59 ± 22,27 tháng; khác biệt thời gian sống toàn bộ giai đoạn II và giai đoạn III không có ý nghiã thống kê (Kiểm định LogRank: χ2=1,067, bậc tự do=1, P=0,302). 4.3. Độc tính do xạ- hóa đồng thời Kết quả nghiên cứu của chúng tôi cho thấy độc tính giảm bạch cầu chủ yếu độ 1, 2 chiếm 33,3%, độ 3 chỉ 3,4%; giảm bạch cầu hạt độ 1, 2: 26,8%, độ 3: 6,0% và độ 4 là 4,3%; giảm hemoglobin chủ yếu độ 1 chiếm 37,1%; giảm tiểu cầu độ 1,2 : 8,6%, độ 3,4 : 3,5%, Mattia Falchetto Osti [12] nghiên cứu trên 55 bệnh nhân hóa xạ đồng thời với Capecitabine cho thấy độc tính giảm bạch cầu độ 1,2: 32%, độ 3: 4%; giảm Hb: độ 1, 2: 12%, độ 3: 2%; giảm tiểu cầu độ 1,2: 13%. Kết quả nghiên cứu của chúng tôi cho thấy độc tính trên hệ tiêu hóa là buồn nôn-nôn độ 1,2: 35,4%, độ 3: 3,4%, tiêu chảy chỉ ở độ 1 và 2 :15,5%; tăng men gan tỷ lệ rất thấp chỉ ở độ 1,2: 9,5%, không có bệnh nhân nào tăng ure và creatinin máu, Mattia Falchetto Osti [12] ngiên cứu trên 55 bệnh nhân hóa xạ đồng thời với Capecitabine nhận thấy độc tính cấp buồn nôn hoặc nôn độ 1,2: 29%, tiêu chảy độ 1,2: 10%, độ 3: 2%. Như vậy, về độc tính do xạ - hóa trị đồng thời với uống capecitabin cho tỷ lệ độc tính ngoài cơ quan tạo huyết là thấp. 5. KẾT LUẬN Qua nghiên cứu tiến cứu 58 trường hợp ung thư biểu mô tuyến dạ dày giai đoạn II, III điều trị bổ trợ hóa xạ đồng thời với capecitabin và hóa trị phác đồ EOX sau phẫu thuật cắt bán phần xa dạ dày kèm vét hạch D1 hoặc D2; trong khoảng thời gian từ tháng 01/2013 – 12/2015 tại Trung tâm Ung bướu - Bệnh viện Trung ương Huế chúng tôi rút ra một số kết luận sau: - Tuổi mắc trung bình hai giới 55,16 ± 9,1 (27 - 76 tuổi), tỉ lệ : Nam : Nữ = 3 : 1, Ung thư biểu mô tuyến 22 Tạp chí Y Dược học - Trường Đại học Y Dược Huế - Tập 8, số 6 - tháng 11/2018 JOURNAL OF MEDICINE AND PHARMACY TÀI LIỆU THAM KHẢO 1. Nguyễn Bá Đức (2010), “Ung thư dạ dày”, Điều trị nội khoa bệnh ung thư, Nxb Y học, tr.29 - 46, 66 - 74, 127 - 141. 2. Trịnh Tuấn Dũng (2009), “Nghiên cứu đặc điểm giải phẫu bệnh ung thư dạ dày”, Tạp chí Y học thành phố Hồ Chí Minh, 13(6), tr. 754-759 3. Trịnh Thị Hoa (2009), “Đánh giá hiệu quả của hóa trị bổ trợ ECX trên bênh nhân ung thư biểu mô tuyến dạ dày sau phẫu thuật tại bệnh viện K (2006 - 2009)”, Luận văn Thạc sĩ y học, Trường Đại học Y khoa Hà Nội. 4. Nguyễn Duy Thăng và CS (2006), “Nghiên cứu dịch tễ học mô tả một số bệnh ung thư tại Thừa thiên Huế giai đoạn 2001-2004”, Tạp chí Y học thực hành, 541, tr. 18-32 5. Vũ Quang Toản, Đoàn Hữu Nghị, Đỗ Anh Tú (2015), “ Điều trị ung thư dạ dày tiến triển tại chỗ bằng phẫu thuật và hóa trị bổ trợ phác đồ EOX”, Tạp chí Y học lâm sàng, Số 29 -2015, tr 270- 278 6. Lê Thị Huỳnh Trang, Lê Đông Nhật Nam, Bùi Chí Viết (2015), “Khảo sát liên quan biểu hiện quá mức HER2 với đặc điểm lâm sàng và bệnh học trong carcinom tuyến dạ dày”, Tạp chí Ung thư học Việt Nam, Số 4-2015, tr 204 –210. 7. Daniel T. Dempsey (2006), “Stomach”, Schwartz’s Manual OfSurgery Eighth Edition, Chapter 25,pp. 650 – 684 8. E. P. M. Jansen, H. Boot et al (2010), “ Postoperative chemoradiotherapy in gastric cancer - a phase I–II study of radiotherapy with dose escalation ofweekly cisplatin and daily capecitabine chemotherapy”, Annals of Oncology 21: 530–534 9. F. De Vita, F. Giuliani, M. Orditura (2007), “Adjuvant chemotherapy with epirubicin, leucovorin5- fluorouracil and etoposide regimen in resectedgastric cancer patients: a randomized phase IIItrial by the Gruppo Oncologico Italia Meridionale(GOIM 9602 Study)” Annals of Oncology 18: pp 1354–1358 10. Globocan (IARC) (2012), “Stomach Cancer Estimated Incidence, Mortality and Prevalence Worldwide in 2012”, Section of Cancer Surveillance (21/8/2014). 11. Jeeyun Lee, Do Hoon Lim, Sung Kim et al (2011), “Phase III Trial Comparing Capecitabine Plus Cisplatin Versus Capecitabine Plus Cisplatin With Concurrent Capecitabine Radiotherapy in Completely Resected Gastric Cancer With D2 Lymph Node Dissection: The ARTIST Trial”,J Clin Oncol, 30, pp. 268-273 12. Mattia Falchetto Osti et al (2012), “Adjuvant Chemoradiation with 5-Fluorouracil or Capecitabinein Patients with Gastric Cancer after D2 Nodal Dissection”, Anticancer journal, Chapter 32, pp. 1397-1402 13. Mitsuru Sasako (2008), “Surgery and adjuvant chemotherapy”, Int J Clin Oncol, 13, pp. 193 - 195 14. Qing Zhang, Jeremy Tey, Lihua Peng(2012), “Adjuvant chemoradio-therapy with or without intraoperative radiotherapy for the treatment of resectable locally advanced gastric adenocarcinoma”, Radiotherapy and Oncology Journal,102, pp. 51-55 15. Sup Kim et al (2011), “Retrospective analysis of treatment outcomes after postoperative chemoradiotherapy in advanced gastric cancer”, Radiat Oncol J, 29(4), pp. 252-259 ống chiếm tỷ lệ cao nhất (63,8%), trong đó loại kém biệt hóa chiếm chiếm hơn một nửa số bệnh nhân (56,9%). Giai đoạn lâm sàng thường gặp là giai đoạn II (70,7%). - Xạ - hóa bổ trợ sau mổ ung thư biểu mô tuyến phần xa dạ dày giai đoạn tiến triển tại chỗ giúp cải thiện tỷ lệ tái phát tại chỗ và tại vùng với các kết quả: Tái phát thường gặp trước một năm sau điều trị (62,5%), sống thêm toàn bộ trung bình là 41,21 ± 21,06 tháng, sống thêm theo giai đoạn: giai đoạn II 41,88 ± 20,78 tháng; giai đoạn III 39,59 ± 22,27 tháng. Sống thêm theo độ xâm lấn của khối u: T3 40,79 ± 19,61 tháng; T4 41,33 ± 24,80 tháng. Sống thêm theo tình trạng di căn hạch vùng: N(-) 41,16 ± 20,51 tháng, N(+) 41,26 ± 22,06 tháng. - Mặc dù có nhiều độc tính do xạ - hóa đồng thời lên hệ tạo huyết (giảm bạch cầu, giảm bạch cầu hạt, giảm tiểu cầu, giảm hemoglobin) và lên hệ tiêu hóa (buồn nôn - nôn, tiêu chảy) nhưng chủ yếu là độ 1-2, ít gặp ở độ 3-4 nên bệnh nhân dễ chấp nhận được.
File đính kèm:
 ket_qua_dieu_tri_ung_thu_bieu_mo_tuyen_phan_xa_da_day_giai_d.pdf
ket_qua_dieu_tri_ung_thu_bieu_mo_tuyen_phan_xa_da_day_giai_d.pdf

