Bài giảng Hóa đại cương - Chương 1: Những khái niệm và định luật cơ sở của hoá học - Huỳnh Kỳ Phương Hạ
Nguyên tử
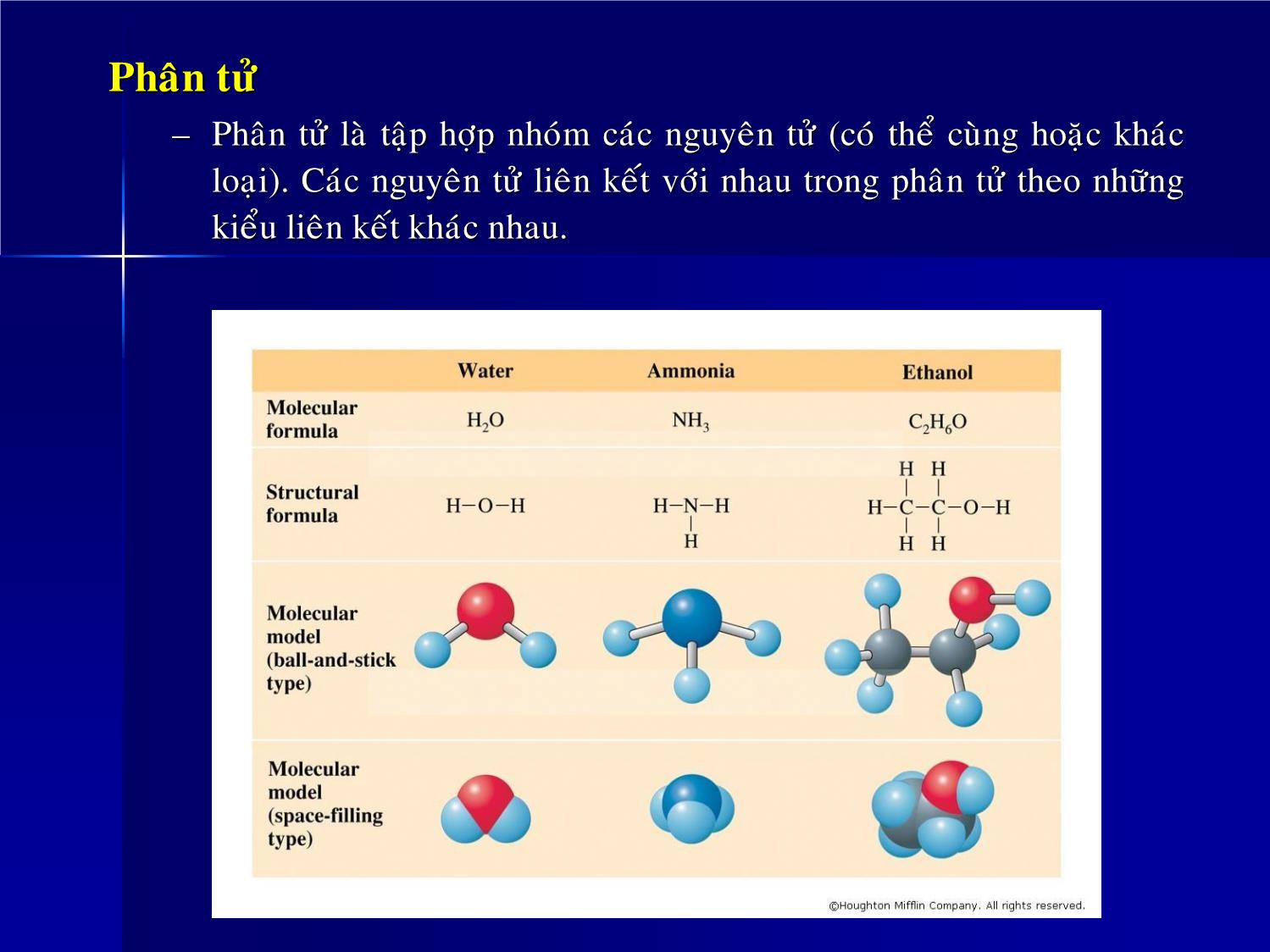
– Nguyên tử là phần tử nhỏ nhất của một nguyên tố hoá học, không
thể phân chia nhỏ hơn được nữa về mặt hoá học. Trong các phản
ứng hoá học, nguyên tử không thay đổi.
Nguyên tố hoá học
– Là chất được tạo thành từ các nguyên tử có điện tích hạt nhân giống
nhau.

Trang 1

Trang 2

Trang 3

Trang 4
Trang 5

Trang 6

Trang 7

Trang 8

Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Bài giảng Hóa đại cương - Chương 1: Những khái niệm và định luật cơ sở của hoá học - Huỳnh Kỳ Phương Hạ", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Bài giảng Hóa đại cương - Chương 1: Những khái niệm và định luật cơ sở của hoá học - Huỳnh Kỳ Phương Hạ

TRƯỜNG ĐẠI HỌC BÁCH KHOA TP. HỒ CHÍ MINH KHOA KỸ THUẬT HĨA HỌC MƠN HỌC HóA ĐẠI CƯƠNG GIẢNG VIÊN: HUỲNH KỲ PHƢƠNG HẠ TÀI LIỆU THAM KHẢO HÓA ĐẠI CƯƠNG (1,2) GS. NGUYỄN ĐÌNH SOA TẬP BÀI TẬP TRẮC NGHIỆM HÓA ĐẠI CƯƠNG (Bộ môn Công nghệ Vô cơ – Khoa Công Nghệ Hóa Học – Trường ĐH Bách Khoa TP HCM) HÓA ĐẠI CƯƠNG (GLINKA, N.L.) HÓA ĐẠI CƯƠNG VÔ CƠ (HOÀNG NHÂM) HÓA ĐẠI CƯƠNG (RENÉ DIDIER) HÓA ĐẠI CƯƠNG VÀ TRẮC NGHIỆM HÓA ĐẠI CƯƠNG (NGYỄN ĐỨC CHUNG) CÁC TÀI LIỆU HĨA ĐẠI CƢƠNG HAY GENERAL CHEMISTRY CHƢƠNG I NHỮNG KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ CỦA HOÁ HỌC Nguyên tử – Nguyên tử là phần tử nhỏ nhất của một nguyên tố hoá học, không thể phân chia nhỏ hơn được nữa về mặt hoá học. Trong các phản ứng hoá học, nguyên tử không thay đổi. Nguyên tố hoá học – Là chất được tạo thành từ các nguyên tử có điện tích hạt nhân giống nhau. Phân tử – Phân tử là tập hợp nhóm các nguyên tử (có thể cùng hoặc khác loại). Các nguyên tử liên kết với nhau trong phân tử theo những kiểu liên kết khác nhau. Đơn chất, hợp chất: -Đơn chất là các chất được cấu thành từ một nguyên tố (Oxy O 2 , Kim cương C, Nitơ N 2 ) -Hợp chất là các chất được cấu thành từ 2 nguyên tố trở lên (H 2 O, Rượu, Dấm) Luật thành phần không đổi: - Một hợp chất hóa học xác định luôn chứa cùng một số nguyên tố như nhau với tỉ lệ khối lượng xác định. Định luật bảo tồn khối lượng (Hay định luật Lomonossow - Lavoisier) là định luật cơ bản trong lĩnh vực hĩa học, đƣợc phát biểu: – Trong phản ứng hĩa học, tổng khối lƣợng các chất tham gia phản ứng bằng tổng khối lƣợng sản phẩm tạo thành. (mtrƣớc) = (msau) Lịch sử: – Năm 1748 Mikhail Lomonossow đặt ra định đề – Năm 1789 Antoine Lavoisier phát biểu định luật này • Khối lượng của 1H = 1.6735 x 10-24 g và 16O là 2.6560 x 10 -23 g. • Định nghĩa: Khối lượng của 12C = chính xác là 12 đvC hay amu (đơn vị Carbon, hay là đơn vị nguyên tử, atomic mass unit). • Từ đó: 1 amu = 1.66054 x 10 -24 g 1 g = 6.02214 x 10 23 amu Khối lượng nguyên tử (Nguyên tử lượng) Đồng vị Các nguyên tử của cùng một nguyên tố nhƣng khác nhau số neutron trong hạt nhân (đƣợc chỉ định bởi số khối). Ví dụ: – Đồng vị của Hydrogen H-1, 1H, protium (một proton, khơng cĩ neutron trong hạt nhân). – Đồng vị của Hydrogen H-2 or D, 2H, deuterium (1 proton và 1 neutron trong hạt nhân). – Đồng vị của Hydrogen H-3 or T, 3H, tritium (1 proton và 1 neutron trong hạt nhân). Nguyên tử lượng trung bình • Trong tự nhiên, các nguyên tố tồn tại ở các dạng đồng vị với tỉ lệ khác nhau, ví dụ: • C: 98.892 % 12C + 1.108 % 13C. • Nguyên tử lượng trung bình C: • (0.98892)(12 amu) + (0.0108)(13amu) = 12.011 amu. • Trong hệ thống tuần hoàn là NTL trung bình. Ví dụ: Chlorine cĩ 2 đồng vị, Cl-35 and Cl-37, cĩ nguyên tử lƣợng lần luợt là 34.96885 and 36.96590 amu. Nguyên tử lƣợng của nĩ trong tự nhiên là 35.453 amu. Thành phần % của từng đồng vị? Đặt x = phần Cl-35, y = phần Cl-37 Ta cĩ x + y = 1 y = 1 - x 34.96885*x + 36.96590*y = 35.453 Từ đĩ x = 0.7553 75.53% Cl-35 y = 1 - x = 0.2447 hay 24.47% Cl-37 Định luật tỉ lệ bội. (Định luật Đalton) – Nếu hai nguyên tố hóa hợp với nhau tạo thành một số hợp chất thì những lượng khối lượng của một nguyên tố so với cùng một lượng khối lượng của nguyên tố kia sẽ tỉ lệ với nhau như những số nguyên đơn giản. Ví dụ: FeS, FeS 2 , với cùng 56 đơn vị khối lượng Fe thì tỉ lệ S: Fe lần lượt là 32:56; 64:56. Do đó tỉ lệ S là 32:64 = 1:2 N 2 O, NO, N 2 O 3 , NO 2 , N 2 O 5 với 14 đơn vị khối lượng N thì tỉ lệ N lần lượt là : (8/14):(16/14):(24/14):(32/14):(40/14) 8:16:32:40 1:2:3:4:5 Chuyển đổi nhiệt độ C = 5/9 * (F - 32) F = (9/5)*C + 32 K = C + 273.15 - 40o F = - 40o C BẢNG CHỮ CÁI HY LẠP TƯƠNG ỨNG : alpha (a) : iota (i) : rho (r) : beta (b) : kappa (k) : ( ) sigma (s) : gamma (g) : ( ) lambda (l) : tau (t) ( ): delta (d) : mu(y) (m) : upsilon (u) : epsilon (e) : nu(y) (n) ( ): phi (f) : zeta (z) : xi (x) : chi (c) : eta (h) : omicron (o) ( ): psi (y) : theta (q) : pi (p) ( ): omega (w) Đương lượng và định luật đương lượng Đương lượng: Đ Đương lượng của một nguyên tố hay một hợp chất là số phần khối lượng của nguyên tố hay hợp chất đó kết hợp hoặc thay thế vừa đủ với một đương lượng của một nguyên tố hay hợp chất khác. Cách tính đương lượng: Công thức chung để tính đương lượng là: Đ A = M/n (n tạm gọi là số đƣơng lƣợng) Trường hợp cụ thể A là một nguyên tố M: khối lượng nguyên tử, n: Hóa trị nguyên tố. Ví dụ: Trong CO thì Đ C =12/2=6 CO 2 thì Đ C =12/4=3 A là axit: M: Phân tử lượng của axit n: Số H + tham gia phản ứng Ví dụ: H2SO4 + NaOH NaHSO4 + H2O ĐA = 98/1=98 H2SO4 + NaOH Na2SO4 + H2O ĐA = 98/2=49 A là bazơ: M: Phân tử lượng của bazơ n: Số OH - tham gia phản ứng Ví dụ: Ca(OH)2 + HCl Ca(OH)Cl + H2O ĐA = M[Ca(OH)2]/1 Ca(OH)2 + HCl CaCl2 + H2O ĐA = M[Ca(OH)2]/2 A là muối: M: Phân tử lượng của muối n: Số điện tích của ion (anion hoặc cation) đã thay thế Ví dụ: Al2(SO4)3 ĐA = M[Al2(SO4)3]/(2x3) theo Al +3 ĐA = M[Al2(SO4)3]/(3x2) theo (SO4) -2 Trong phản ứng cụ thể Fe2(SO4)3 + 2NH4OH = 2Fe(OH)SO4 + (NH4)2SO4 Đ[NH4OH] = M[NH4OH] (vì chỉ cĩ 1 nhĩm OH -) Đ[Fe2(SO4)3] = Đ[Fe2(SO4)3]/(1[SO4 -2]x2) (vì trong 2Fe.2(SO4).(SO4) cĩ 1 nhĩm SO4 -2 đã bị thay thế) A là chất oxi hóa-khử: – M: khối lượng phân tử chất. – n: số e trao đổi trong phản ứng. Ví dụ: 8Al+3KNO3+5KOH+2H2O=3NH3+8KAlO2 Đ[Al] = 27/3 (Số e trao đổi từ Al0 Al+3=3e) Đ[KOH] = M[KOH] Đ[KNO3] = M[KNO3]/8 (N+5 N-3 trao đổi 8e) Đương lượng gam (đlg): – Đương lượng gam của một chất là lượng tính bằng g của chất đó có số đo bằng đương lượng của nó. Ví dụ: – Đƣơng lƣợng của H2SO4 là 49 hay 98 thì 1 đlg là 49g hay 98g. Định luật đương lượng: – Trong một phản ứng hóa học số đương lượng của các chất tham gia phản ứng phải bằng nhau. – Trong các phản ứng hóa họa một đương lượng của chất này chỉ kết hợp hoặc thay thế một đương lượng của chất khác mà thôi. Phản ứng: aA + bB = cD + dD Số đlg của chất i = mi/Đi Từ đĩ định luật viết thành: mA/ĐA = mB/ĐB hay mA/mB = ĐA/ĐB Và: NAVA = NBVB = NCVC Trong đĩ Ni là nồng độ đƣơng lƣợng của chất i. Nồng độ đương lượng: – Là số đương lượng gam chất tan trên một lít dung dịch. – Ký hiệu N hay C N . Tƣơng quan giữa nồng độ mol và nồng độ đƣơng lƣợng N A = nC A (n: Số đƣơng lƣợng) Ví dụ: Cho phản ứng H2SO4 + 2NH4OH = (NH4)2SO4 + 2H2O Tìm khối lƣợng NH4OH cần thiết để phản ứng vừa đủ với 2 lít dd H2SO4 0.5N. Ta cĩ n của H2SO4 là 2 và đƣơng lƣợng là 49, nên CA=NA/2 = 0.25M. Khối lƣợng axit là 2x0.25x98=49g m[NH4OH]=m[H2SO4]x(Đ[NH4OH]/Đ[H2SO4]) Phương trình trạng thái khí lý tưởng pV = nRT – p: áp suất (atm,mmHg) – V: thể tích (ml, lít) – T: nhiệt độ Kenvin – n: số mol – R: Hằng số khí R = 0.082 (l.atm/mol.K) R = 62400 (ml.mmHg/mol.K) R = 1.987 (cal/mol.K) Định luật Avogadro – Một mol khí bất kỳ ở điều kiện tiêu chuẩn 0 0 C, 760mmHg) phải chứa một số phân tử là 6.023x10 23 . N = 6.023x10 23 là số Avogadro. – Từ đó tính được khối lượng chính xác của nguyên tử và phân tử. Quy tắc Bát bộ (octet - Lewis và Langmuir) – “Để cĩ một trạng thái electron ổn định giống khí trơ, các nguyên tử cĩ khuynh hƣớng nhận, cho, hay chia sẻ các electron để tầng ngồi cùng cĩ thể cĩ hoặc gĩp phần vào 4 cặp electron (bát bộ).” Quy tắc bát bộ cĩ những ngoại lệ. Thí dụ nhƣ với hydrogen và helium, số electron tối đa là 2 thay vì 8; với phosphorus (P) số này là 10; với sulfur (S) số này cĩ thể là 12
File đính kèm:
 bai_giang_hoa_dai_cuong_chuong_1_nhung_khai_niem_va_dinh_lua.pdf
bai_giang_hoa_dai_cuong_chuong_1_nhung_khai_niem_va_dinh_lua.pdf

