Ứng dụng phương pháp ngâm chiết soda và tác nhân oxy hóa để thu hồi chọn lọc molybdenum từ xúc tác thải của quá trình hydrodesulphur hóa
Xúc tác thải từ quá trình hydroprocessing chứa khoảng 4 - 12% molybdenum (Mo) (theo khối lượng) sẽ đem lại
hiệu quả kinh tế nếu thu hồi được các kim loại có giá trị. Bài báo giới thiệu quy trình thủy luyện đơn giản sử dụng
hỗn hợp soda (Na2CO3) kết hợp với H2O2 để thu hồi Mo từ xúc tác thải của quá trình hydrodesulphur hóa. Việc thu hồi
Mo phụ thuộc rất nhiều vào nồng độ H2O2 và Na2CO3 trong môi trường phản ứng, việc điều chỉnh pH cho quá trình
ngâm tách và sự có mặt của Al, Co. Với điều kiện tách tối ưu theo nồng độ Na2CO3 là 40g/l, H2O2 6% ở nhiệt độ phòng
trong khoảng thời gian 2 giờ thì hiệu suất Mo thu được khoảng 85%. Ngâm tách bằng phương pháp hấp phụ sử dụng
carbon sẽ thu được MoO3 có độ tinh khiết trên 95%.

Trang 1
Trang 2
Trang 3
Trang 4
Trang 5

Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Ứng dụng phương pháp ngâm chiết soda và tác nhân oxy hóa để thu hồi chọn lọc molybdenum từ xúc tác thải của quá trình hydrodesulphur hóa

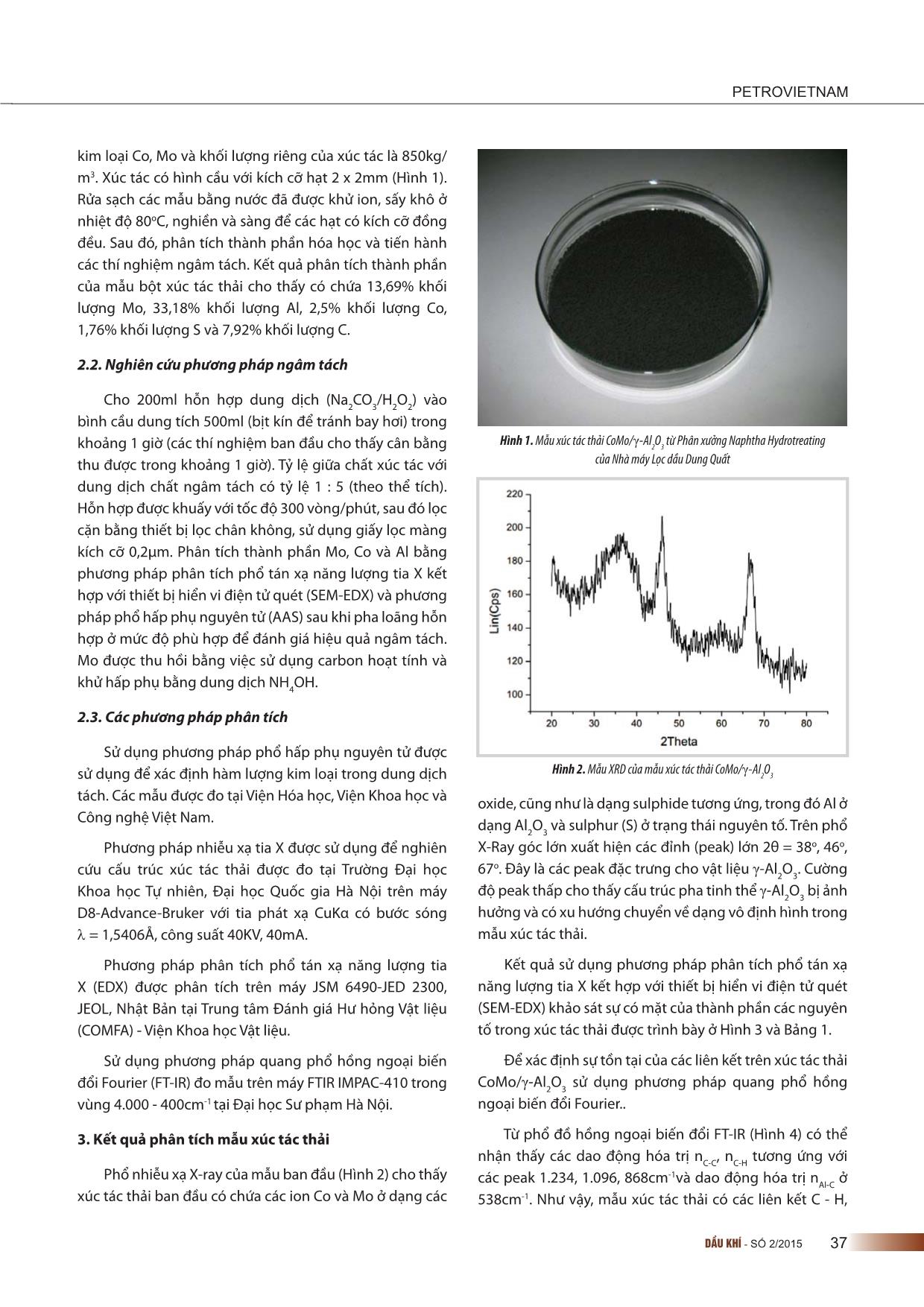
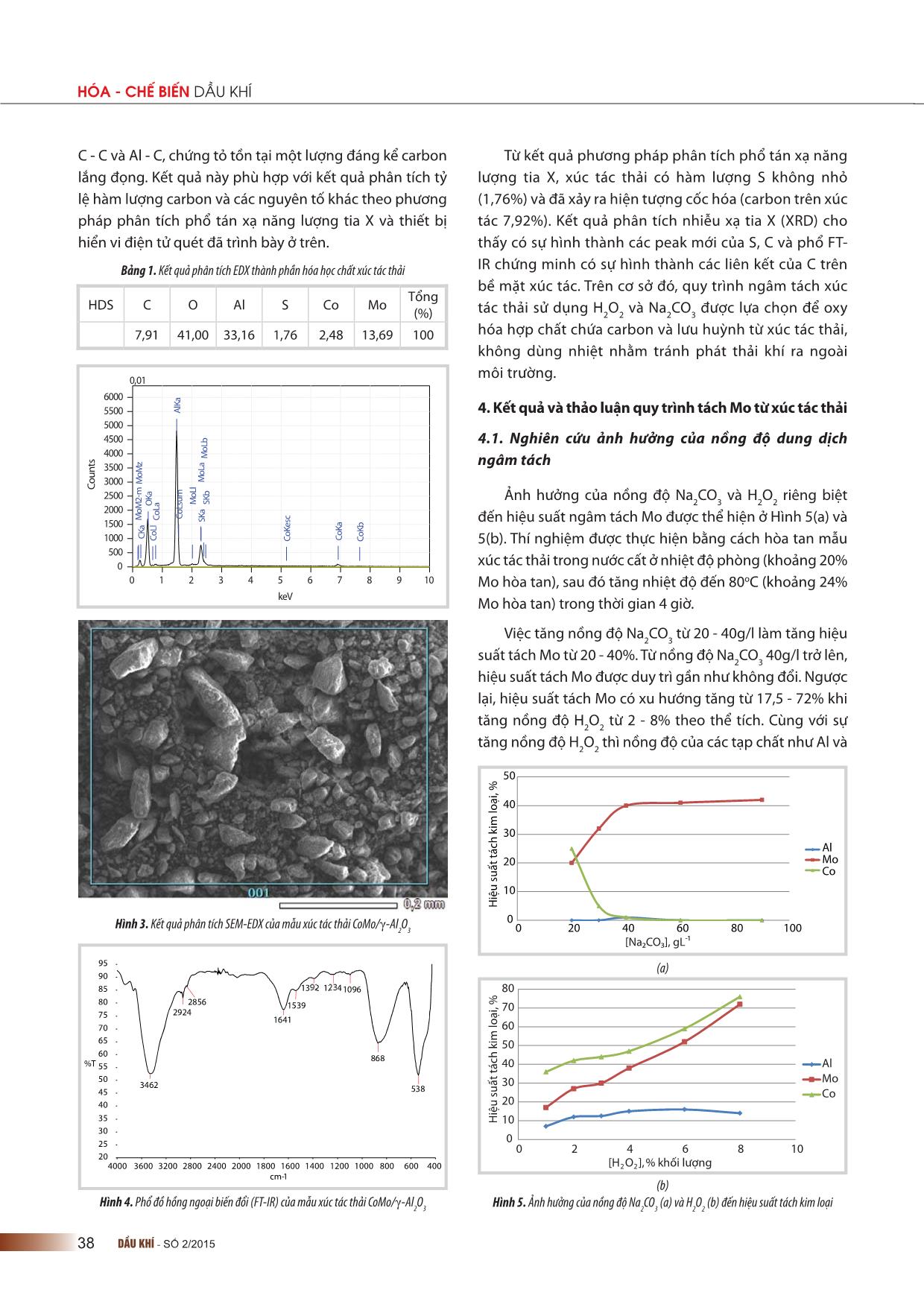
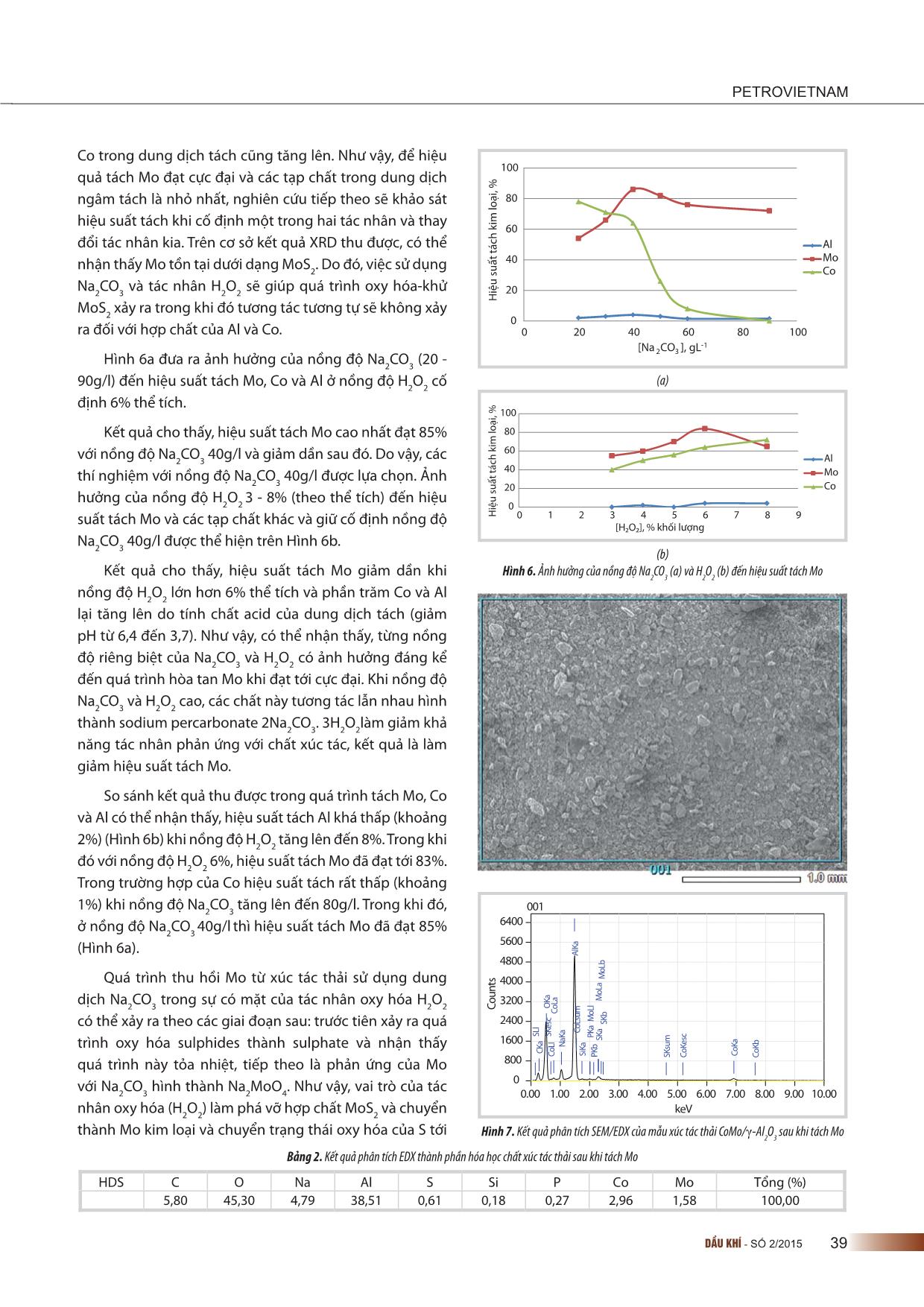
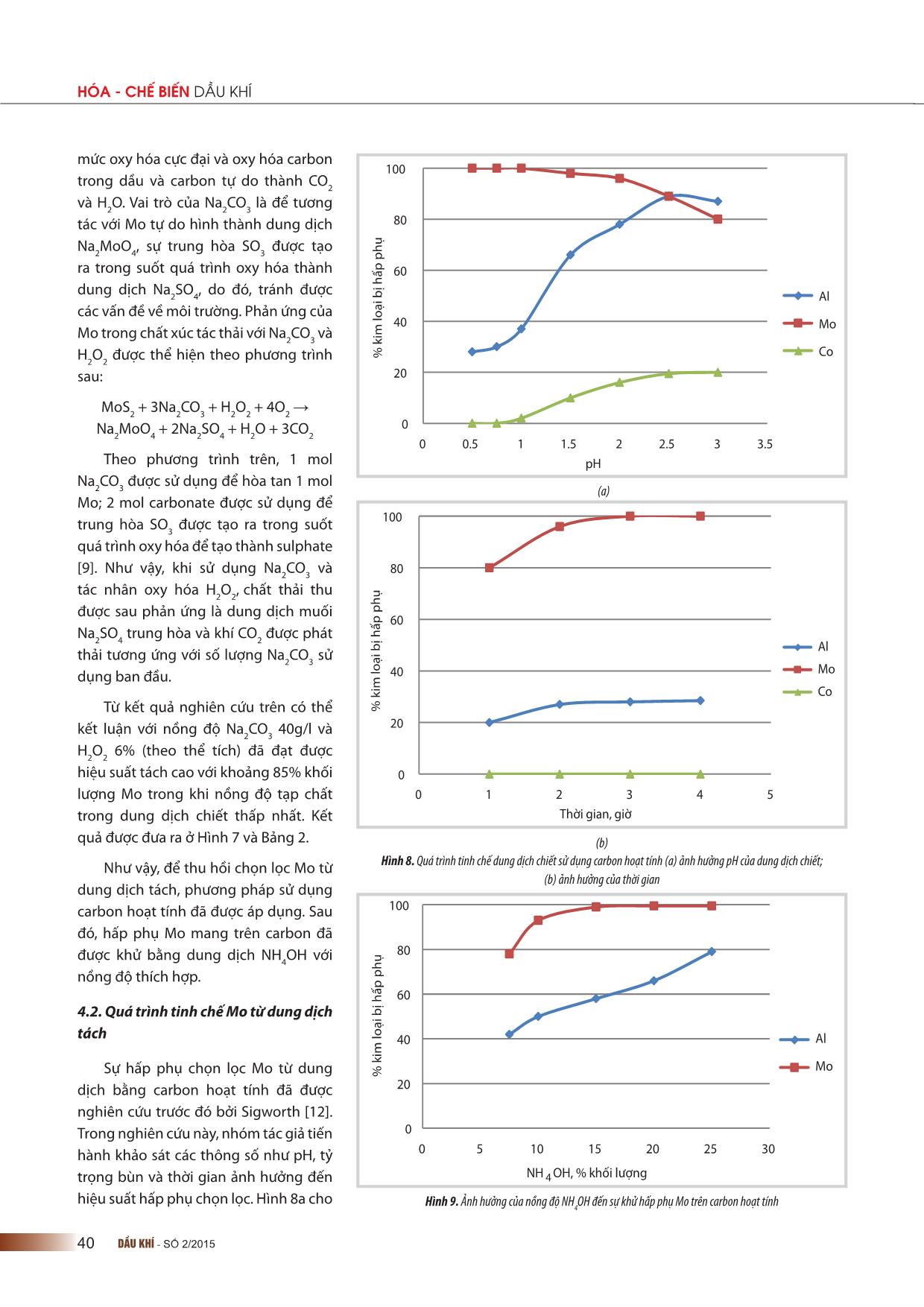
HÓA - CHẾ BIẾN DẦU KHÍ 36 DẦU KHÍ - SỐ 2/2015 1. Mở đầu Xúc tác trong công nghệ lọc dầu chiếm khoảng 1/3 lượng xúc tác tiêu thụ trên toàn thế giới, phần lớn được sử dụng cho quá trình hydro hóa khử lưu huỳnh, hydro đề nitơ và loại bỏ các tạp chất kim loại trong dầu tương ứng với các phân đoạn khác nhau [1]. Sau một chu kỳ hoạt động, một lượng lớn xúc tác này thải ra ngoài môi trường. Xúc tác thải từ quá trình hydroprocessing thường chứa khoảng 4 - 12% Mo, 15 - 30%Al, 1 - 5% Ni, 0 - 4%Co, 5 - 10% S, 1 - 5% Si, 0 - 0,5% V mang lại hiệu quả kinh tế nếu như thu hồi được các kim loại có giá trị [2]. Các nhà máy lọc dầu sử dụng nguồn dầu thô khác nhau thì xúc tác thải có các thành phần khác nhau. Do vậy, các phương pháp thu hồi phải được điều chỉnh để phù hợp với từng trường hợp và điều kiện công nghiệp. Các công trình nghiên cứu liên quan đến lĩnh vực này là các bằng sáng chế trên cơ sở phương pháp tách - nung chảy [3 - 8] và một số nghiên cứu khác, sử dụng phương pháp ngâm tách, oxy hóa để thu hồi Mo [9 - 11]. Các nghiên cứu cho thấy, quá trình tách các kim loại có mặt trong chất xúc tác thải bằng cách ngâm chiết với dung dịch acid đã được nghiên cứu bởi Mulak và cộng sự [12] sử dụng acid oxalic và H2O2 đã thu hồi được 90% Mo, 94% V, 65% Ni và 33% Al theo khối lượng; Marafi và Furimsky [13] dùng acid tartaric thì thu được 93% Mo, 94% V, 83% Ni theo khối lượng, còn sử dụng dung dịch tách acid citric thì thu được 94% Mo, 94% V, 85% Ni. Như vậy, có thể sử dụng nhiều acid vô cơ, hữu cơ khác nhau để ngâm tách thu hồi các kim loại. Wang [14] đã nghiên cứu thu hồi Mo, Co và Al2O3 từ chất xúc tác thải bỏ từ quá trình naphtha hydrotreating (NHT) CoMo/Al2O3 sử dụng kiềm nóng chảy, sau đó bằng NH3 và xử lý ngâm tách bằng acid. Chất xúc tác thải trước tiên được khử cốc, sau đó nung với soda kiềm. Vật liệu sau khi nung được ngâm trong dung dịch NH3 thu được dung dịch chính chứa Mo và chất rắn chủ yếu chứa Al2O3 và cobalt. Sau đó, dung dịch được xử lý bằng HNO3 và NH3 đặc nhằm thu hồi (NH4)2MoO4 với độ tinh khiết cao. Tuy nhiên, các nghiên cứu này cho thấy, quá trình nung tiêu tốn nhiều năng lượng và thải một lượng lớn SOx ra môi trường, Mo bị biến đổi thành molybdates bền với các tạp chất nên cần phải xử lý qua các giai đoạn tiếp theo. Do vậy, cần lựa chọn công nghệ “sạch” để thu hồi kim loại giúp giảm phát thải khí SOx gây ô nhiễm và giảm tiêu tốn năng lượng như sử dụng quy trình ngâm tách thủy luyện sử dụng H2O2 và Na2CO3. Trên cơ sở đó, nhóm tác giả đã nghiên cứu thực hiện quy trình thủy luyện trên cơ sở chất xúc tác thải NHT CoMo/γ-Al2O3 sử dụng tác nhân Na2CO3 và H2O2 nhằm thu hồi MoO3 từ dung dịch chiết, đồng thời khảo sát các thông số tối ưu cho quá trình tách như: thời gian tương tác, nồng độ các tác nhân (Na2CO3/H2O2), pH cân bằng... 2. Thực nghiệm 2.1. Chuẩn bị mẫu Chất xúc tác thải CoMo/γ-Al2O3 sử dụng trong nghiên cứu này thu được từ Phân xưởng Naphtha Hydrotreating (NHT) của Nhà máy Lọc dầu Dung Quất, ký hiệu là S-120 (UOP). Chất mang Al2O3 có dạng viên ép kích cỡ 1/16”, tâm ỨNG DỤNG PHƯƠNG PHÁP NGÂM CHIẾT SODA VÀ TÁC NHÂN OXY HÓA ĐỂ THU HỒI CHỌN LỌC MOLYBDENUM TỪ XÚC TÁC THẢI CỦA QUÁ TRÌNH HYDRODESULPHUR HÓA PGS.TS. Phạm Xuân Núi, KS. Phạm Sơn Tùng Đại học Mỏ - Địa chất Email: [email protected] Tóm tắt Xúc tác thải từ quá trình hydroprocessing chứa khoảng 4 - 12% molybdenum (Mo) (theo khối lượng) sẽ đem lại hiệu quả kinh tế nếu thu hồi được các kim loại có giá trị. Bài báo giới thiệu quy trình thủy luyện đơn giản sử dụng hỗn hợp soda (Na2CO3) kết hợp với H2O2 để thu hồi Mo từ xúc tác thải của quá trình hydrodesulphur hóa. Việc thu hồi Mo phụ thuộc rất nhiều vào nồng độ H2O2 và Na2CO3 trong môi trường phản ứng, việc điều chỉnh pH cho quá trình ngâm tách và sự có mặt của Al, Co. Với điều kiện tách tối ưu theo nồng độ Na2CO3 là 40g/l, H2O2 6% ở nhiệt độ phòng trong khoảng thời gian 2 giờ thì hiệu suất Mo thu được khoảng 85%. Ngâm tách bằng phương pháp hấp phụ sử dụng carbon sẽ thu được MoO3 có độ tinh khiết trên 95%. Từ khóa: Molybdenum, ngâm chiết soda. PETROVIETNAM 37DẦU KHÍ - SỐ 2/2015 kim loại Co, Mo và khối lượng riêng của xúc tác là 850kg/ m3. Xúc tác có hình cầu với kích cỡ hạt 2 x 2mm (Hình 1). Rửa sạch các mẫu bằng nước đã được khử ion, sấy khô ở nhiệt độ 80oC, nghiền và sàng để các hạt có kích cỡ đồng đều. Sau đó, phân tích thành phần hóa học và tiến hành các thí nghiệm ngâm tách. Kết quả phân tích thành phần của mẫu bột xúc tác thải cho thấy có chứa 13,69% khối lượng Mo, 33,18% khối lượng Al, 2,5% khối lượng Co, 1,76% khối lượng S và 7,92% khối lượng C. 2.2. Nghiên cứu phương pháp ngâm tách Cho 200ml hỗn hợp dung dịch (Na2CO3/H2O2) vào bình cầu dung tích 500ml (bịt kín để tránh bay hơi) trong khoảng 1 giờ (các thí nghiệm ban đầu cho thấy cân bằng thu được trong khoảng 1 giờ). Tỷ lệ giữa chất xúc tác với dung dịch chất ngâm tách có tỷ lệ 1 : 5 (theo thể tích). Hỗn hợp được khuấy với tốc độ 300 vòng/phút, sau đó lọc cặn bằng thiết bị lọc chân không, sử dụng giấy lọc màng kích cỡ 0,2μm. Phân tích thành phần Mo, Co và Al bằng phương pháp phân tích phổ tán xạ năng lượng tia X kết hợp với thiết bị hiển vi điện tử quét (SEM-EDX) và phương pháp phổ hấp phụ nguyên tử (AAS) sau khi pha loãng hỗn hợp ở mức độ phù hợp để đánh giá hiệu quả ngâm tách. Mo được thu hồi bằng việc sử dụng carbon hoạt tính và khử hấp phụ bằng dung dịch NH4OH. 2.3. Các phương pháp phân tích Sử dụng phương pháp phổ hấp phụ nguyên tử được sử dụng để xác định hàm lượng kim loại trong dung dịch tách. Các mẫu được đo tại Viện Hóa học, Viện Khoa học và Công nghệ Việt Nam. Phương pháp nhiễu xạ tia X được sử dụng để nghiên cứu cấu trúc xúc tác thải được đo tại Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia Hà Nội trên máy D8-Advance-Bruker với tia phát xạ CuKα có bước sóng = 1,5406Å, công suất 40KV, 40mA. Phương pháp phâ ... ách hòa tan mẫu xúc tác thải trong nước cất ở nhiệt độ phòng (khoảng 20% Mo hòa tan), sau đó tăng nhiệt độ đến 80oC (khoảng 24% Mo hòa tan) trong thời gian 4 giờ. Việc tăng nồng độ Na2CO3 từ 20 - 40g/l làm tăng hiệu suất tách Mo từ 20 - 40%. Từ nồng độ Na2CO3 40g/l trở lên, hiệu suất tách Mo được duy trì gần như không đổi. Ngược lại, hiệu suất tách Mo có xu hướng tăng từ 17,5 - 72% khi tăng nồng độ H2O2 từ 2 - 8% theo thể tích. Cùng với sự tăng nồng độ H2O2 thì nồng độ của các tạp chất như Al và HDS C O Al S Co Mo Tổng (%) 7,91 41,00 33,16 1,76 2,48 13,69 100 Bảng 1. Kết quả phân tích EDX thành phần hóa học chất xúc tác thải 0 1 2 3 4 5 6 7 8 9 10 keV 0,01 0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000 5500 6000 Co un ts CK a O Ka Al Ka SK a SK b Co Ll Co La Co Ls um Co Ke sc Co Ka Co Kb M oM 2- m M oM z M oL l M oL a M oL b 0 10 20 30 40 50 60 70 80 0 2 4 6 8 10 H iệ u su ất tá ch k im lo ại , % [H2O2],% khối lượng Al Mo Co 0 10 20 30 40 50 0 20 40 60 80 100 H iệ u su ất tá ch k im lo ại , % Al Mo Co [Na2CO3], gL-1 4000 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600 400 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 cm-1 %T 3462 2924 2856 1641 1539 1392 1234 1096 868 538 Hình 3. Kết quả phân tích SEM-EDX của mẫu xúc tác thải CoMo/γ-Al2O3 Hình 4. Phổ đồ hồng ngoại biến đổi (FT-IR) của mẫu xúc tác thải CoMo/γ-Al2O3 Hình 5. Ảnh hưởng của nồng độ Na2CO3 (a) và H2O2 (b) đến hiệu suất tách kim loại (b) (a) PETROVIETNAM 39DẦU KHÍ - SỐ 2/2015 0 20 40 60 80 100 0 1 2 3 4 5 6 7 8 9H iệ u su ất tá ch k im lo ại , % [H2O2], % khối lượng Al Mo Co 0 20 40 60 80 100 0 20 40 60 80 100 H iệ u su ất tá ch k im lo ại , % [Na 2CO3 ], gL-1 Al Mo Co 0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00 9.00 10.00 keV 001 0 800 1600 2400 3200 4000 4800 5600 6400 Co un ts CK a O Ka Na Ka Al Ka Si Ka PK a PK b SL l SK es c SK a SK b SK su m Co Ll Co La Co Ls um Co Ke sc Co Ka Co Kb M oL l M oL a M oL b (b) (a) HDS C O Na Al S Si P Co Mo Tổng (%) 5,80 45,30 4,79 38,51 0,61 0,18 0,27 2,96 1,58 100,00 Hình 7. Kết quả phân tích SEM/EDX của mẫu xúc tác thải CoMo/γ-Al2O3 sau khi tách Mo Hình 6. Ảnh hưởng của nồng độ Na2CO3 (a) và H2O2 (b) đến hiệu suất tách Mo Bảng 2. Kết quả phân tích EDX thành phần hóa học chất xúc tác thải sau khi tách Mo Co trong dung dịch tách cũng tăng lên. Như vậy, để hiệu quả tách Mo đạt cực đại và các tạp chất trong dung dịch ngâm tách là nhỏ nhất, nghiên cứu tiếp theo sẽ khảo sát hiệu suất tách khi cố định một trong hai tác nhân và thay đổi tác nhân kia. Trên cơ sở kết quả XRD thu được, có thể nhận thấy Mo tồn tại dưới dạng MoS2. Do đó, việc sử dụng Na2CO3 và tác nhân H2O2 sẽ giúp quá trình oxy hóa-khử MoS2 xảy ra trong khi đó tương tác tương tự sẽ không xảy ra đối với hợp chất của Al và Co. Hình 6a đưa ra ảnh hưởng của nồng độ Na2CO3 (20 - 90g/l) đến hiệu suất tách Mo, Co và Al ở nồng độ H2O2 cố định 6% thể tích. Kết quả cho thấy, hiệu suất tách Mo cao nhất đạt 85% với nồng độ Na2CO3 40g/l và giảm dần sau đó. Do vậy, các thí nghiệm với nồng độ Na2CO3 40g/l được lựa chọn. Ảnh hưởng của nồng độ H2O2 3 - 8% (theo thể tích) đến hiệu suất tách Mo và các tạp chất khác và giữ cố định nồng độ Na2CO3 40g/l được thể hiện trên Hình 6b. Kết quả cho thấy, hiệu suất tách Mo giảm dần khi nồng độ H2O2 lớn hơn 6% thể tích và phần trăm Co và Al lại tăng lên do tính chất acid của dung dịch tách (giảm pH từ 6,4 đến 3,7). Như vậy, có thể nhận thấy, từng nồng độ riêng biệt của Na2CO3 và H2O2 có ảnh hưởng đáng kể đến quá trình hòa tan Mo khi đạt tới cực đại. Khi nồng độ Na2CO3 và H2O2 cao, các chất này tương tác lẫn nhau hình thành sodium percarbonate 2Na2CO3. 3H2O2làm giảm khả năng tác nhân phản ứng với chất xúc tác, kết quả là làm giảm hiệu suất tách Mo. So sánh kết quả thu được trong quá trình tách Mo, Co và Al có thể nhận thấy, hiệu suất tách Al khá thấp (khoảng 2%) (Hình 6b) khi nồng độ H2O2 tăng lên đến 8%. Trong khi đó với nồng độ H2O2 6%, hiệu suất tách Mo đã đạt tới 83%. Trong trường hợp của Co hiệu suất tách rất thấp (khoảng 1%) khi nồng độ Na2CO3 tăng lên đến 80g/l. Trong khi đó, ở nồng độ Na2CO3 40g/l thì hiệu suất tách Mo đã đạt 85% (Hình 6a). Quá trình thu hồi Mo từ xúc tác thải sử dụng dung dịch Na2CO3 trong sự có mặt của tác nhân oxy hóa H2O2 có thể xảy ra theo các giai đoạn sau: trước tiên xảy ra quá trình oxy hóa sulphides thành sulphate và nhận thấy quá trình này tỏa nhiệt, tiếp theo là phản ứng của Mo với Na2CO3 hình thành Na2MoO4. Như vậy, vai trò của tác nhân oxy hóa (H2O2) làm phá vỡ hợp chất MoS2 và chuyển thành Mo kim loại và chuyển trạng thái oxy hóa của S tới HÓA - CHẾ BIẾN DẦU KHÍ 40 DẦU KHÍ - SỐ 2/2015 mức oxy hóa cực đại và oxy hóa carbon trong dầu và carbon tự do thành CO2 và H2O. Vai trò của Na2CO3 là để tương tác với Mo tự do hình thành dung dịch Na2MoO4, sự trung hòa SO3 được tạo ra trong suốt quá trình oxy hóa thành dung dịch Na2SO4, do đó, tránh được các vấn đề về môi trường. Phản ứng của Mo trong chất xúc tác thải với Na2CO3 và H2O2 được thể hiện theo phương trình sau: MoS2 + 3Na2CO3 + H2O2 + 4O2 → Na2MoO4 + 2Na2SO4 + H2O + 3CO2 Theo phương trình trên, 1 mol Na2CO3 được sử dụng để hòa tan 1 mol Mo; 2 mol carbonate được sử dụng để trung hòa SO3 được tạo ra trong suốt quá trình oxy hóa để tạo thành sulphate [9]. Như vậy, khi sử dụng Na2CO3 và tác nhân oxy hóa H2O2, chất thải thu được sau phản ứng là dung dịch muối Na2SO4 trung hòa và khí CO2 được phát thải tương ứng với số lượng Na2CO3 sử dụng ban đầu. Từ kết quả nghiên cứu trên có thể kết luận với nồng độ Na2CO3 40g/l và H2O2 6% (theo thể tích) đã đạt được hiệu suất tách cao với khoảng 85% khối lượng Mo trong khi nồng độ tạp chất trong dung dịch chiết thấp nhất. Kết quả được đưa ra ở Hình 7 và Bảng 2. Như vậy, để thu hồi chọn lọc Mo từ dung dịch tách, phương pháp sử dụng carbon hoạt tính đã được áp dụng. Sau đó, hấp phụ Mo mang trên carbon đã được khử bằng dung dịch NH4OH với nồng độ thích hợp. 4.2. Quá trình tinh chế Mo từ dung dịch tách Sự hấp phụ chọn lọc Mo từ dung dịch bằng carbon hoạt tính đã được nghiên cứu trước đó bởi Sigworth [12]. Trong nghiên cứu này, nhóm tác giả tiến hành khảo sát các thông số như pH, tỷ trọng bùn và thời gian ảnh hưởng đến hiệu suất hấp phụ chọn lọc. Hình 8a cho 0 20 40 60 80 100 0 0.5 1 1.5 2 2.5 3 3.5 % k im lo ại b ị h ấp p hụ pH Al Mo Co 0 20 40 60 80 100 0 1 2 3 4 5 % k im lo ại b ị h ấp p hụ Thời gian, giờ Al Mo Co 0 20 40 60 80 100 0 5 10 15 20 25 30 % k im lo ại b ị h ấp p hụ NH 4 OH, % khối lượng Al Mo (b) (a) Hình 8. Quá trình tinh chế dung dịch chiết sử dụng carbon hoạt tính (a) ảnh hưởng pH của dung dịch chiết; (b) ảnh hưởng của thời gian Hình 9. Ảnh hưởng của nồng độ NH4OH đến sự khử hấp phụ Mo trên carbon hoạt tính PETROVIETNAM 41DẦU KHÍ - SỐ 2/2015 thấy ảnh hưởng pH (từ 0,5 - 3) của dung dịch tách đến quá trình hấp phụ Mo và các tạp chất khác, tỷ trọng bùn duy trì ở mức 40% và trong khoảng thời gian 4 giờ. Quá trình hấp phụ được sử dụng để thu hồi Mo có độ tinh khiết cao khi thực hiện ở pH thấp. Với pH thấp (trong khoảng 0,5 - 1,0), khoảng gần 99% khối lượng Mo được hấp phụ trên carbon hoạt tính trong khi đó chỉ có 27 - 35% khối lượng Al và lượng nhỏ Co được hấp phụ. Do vậy, pH của dung dịch chiết được giữ không đổi ở 0,75 cho các nghiên cứu sau. Hình 8b cho thấy ảnh hưởng của thời gian đến % Mo hấp phụ. Điều này có thể nhận thấy thời gian tiếp xúc 3 giờ đủ cho quá trình hấp phụ ổn định. Vì vậy, tất cả các nghiên cứu đến quá trình hấp phụ được đưa trong khoảng thời gian tiếp xúc là 3 giờ. Sự khử hấp phụ Mo được nghiên cứu với tỷ trọng bùn cố định là 30% khối lượng cùng với các nồng độ NH4OH từ 7,5 - 25% thể tích (Hình 9). Sự khử hấp phụ với lượng Mo thu được cực đại tương ứng với 15% thể tích NH4OH, Al khử hấp phụ khoảng 58%. pH của dung dịch trong khoảng 9,5. Dung dịch này được acid hóa bằng việc sử dụng dung dịch HCl tới pH = 2 và đun nóng đến nhiệt độ 90oC để kết tủa muối (NH4)2MoO4. Với pH này hầu hết toàn bộ ammonium molybdenum được kết tủa ngay sau đó. Kết tủa được lọc, rửa bằng nước khử ion để trung hòa pH. Cuối cùng sản phẩm được nung ở 450oC để đưa về dạng MoO3 và thu được độ tinh khiết của sản phẩm trên 95%. 5. Kết luận Nghiên cứu này cho thấy tính khả thi của việc thu hồi chọn lọc Mo dạng MoO3 từ xúc tác thải của quá trình hydrodesulphur qua việc hình thành (NH4)2MoO4 bằng quá trình hấp phụ chọn lọc carbon từ dung dịch tách soda với chi phí thấp, thân thiện với môi trường. Với quy trình này, S và C trên xúc tác thải được chuyển thành CO2 và Na2SO4 không gây tác hại đến môi trường. Phản ứng của chất xúc tác thải với tác nhân oxy hóa H2O2 là phản ứng tỏa nhiệt, có tốc độ nhanh và tự duy trì. Hiệu suất ngâm tách Mo và các tạp chất khác như Al và Co phụ thuộc vào nồng độ tác nhân oxy hóa và soda trong môi trường phản ứng. Quá trình xử lý sản phẩm thu hồi Mo từ dung dịch chiết qua quá trình hấp phụ carbon hoạt tính và khử hấp phụ với dung dịch NH4OH đã được áp dụng để thu được sản phẩm MoO3 với độ tinh khiết đạt trên 95% và hiệu suất thu hồi Mo tổng thể đạt 85% khối lượng. Việc tái sinh than hoạt tính để dùng lại đã được chứng minh. Tài liệu tham khảo 1. Edward Furimsky. Spent refi nery catalysts: environment, safety and utilization. Catalysis Today. 1996; 30(4): p. 223 - 286. 2. R.E.Siemens, B.W.Jong, J.H.Russell. Potential of spent catalysts as a source of critical metals. Conservation & Recycling. 1986; 9(2): p. 189 - 196. 3. Phạm Xuân Núi, Phạm Sơn Tùng, Nguyễn Thị Ánh. Nghiên cứu thu hồi platinum (Pt) từ xúc tác thải bỏ của phân xưởng reforming trong nhà máy lọc dầu. Tạp chí Xúc tác và Hấp phụ. 2012; 1: trang 162 - 169. 4. Paul J.Marcantonio. Leaching metals from spent hydroprocessing catalysts with ammonium sulfate. United States Patent 4554138 A. 1985. 5. Keiji Toyabe, Kenji Kirishima, Haruo Shibayama, Hideo Hanawa. Process for recovering valuable metal from waste catalyst. United States Patent 5431892 A. 11/7/1995. 6. Jack Thomas Veal, Kevin Arnol Andersen, Ruth Mary Kowaleski. Process to recover metals from spent catalyst. United States Patent 6180072 B1. 2001. 7. Darren Delai Sun, Joo Hwa Tay, Hee Kiat Cheong, Dickson Lai Kwok Leung, Guang Ren Qian. Recovery of heavy metals and stabilization of spent hydrotreating catalyst using a glass-ceramic matrix. Journal of Hazardous Materials. 2001; 87(1 - 3): p. 213 - 223. 8. M.H.Shariat, N.Setoodeh, R.A.Dehghan. Optimizing conditions for hydrometallurgical production of purifi ed molybdenum trioxide from roasted molybdenite of sarcheshmeh. Minerals Engineering. 2001; 14(7): p. 815 - 820. 9. Roger F.Sebenik, Pablo P.Lavalle, John M.Laferty, William A.May. Recovery of metal values from spent hydrodesulfurization catalysts. United States Patent 4495157 A. 1985. 10. Victor J.Ketcham, Enzo L.Coltrinari, Wayne W.Hazen. Pressure oxidation of aqueous slurry of ore to form soluble and insoluble molybdenum oxides, solubilizing the insoluble molybdenum oxides with an alkali, then solvent extraction, crystallization, calcining to recover molybdenum trioxide. United States Patent 6149883 A. 2000. 11. Robert W.Balliett, Wolfgang Kummer, John E.Litz, Lawrence F.McHugh, Harry H.K.Nauta, Paul B.Queneau, Rong Chien Wu. Forming aqueous slurry of low grade molybdenite concentrates; oxidizing; fi ltering discharge; HÓA - CHẾ BIẾN DẦU KHÍ 42 DẦU KHÍ - SỐ 2/2015 leaching solid fi lter cake with an alkaline solution; fi ltering second discharge; recovering the molybdenum value; crystallization. United States Patent 6730279 B2. 2004. 12. Wladyslawa Mulak, Anna Szymczycha, Anna Lesniewicz, Wieslaw Zyrnicki. Preliminary results of metals leaching from a spent hydrodesulphurization (HDS) catalyst. Physicochemical Problems of Mineral Processing. 2006; 40: p. 69 - 76. 13. M.Marafi , E.Furimsky. Selection of organic agents for reclamation of metals from spent hydroprocessing catalysts. Erdoel Erdgas Kohle. 2005; 121(2): p. 93 - 96. 14. MV.Wang. Recovery of vanadium, molybdenum, nickel and cobalt from spent catalysts: a new processing plant in China. Recycling of Metals and Engineered Materials. 2000. 15. E.A.Sigworth. Potentialities of activated carbon in the metallurgical fi eld. American Institute of Mining, Metallurgical and Petroleum Engineers. 1962. Summary The spent catalysts of these processes contain about 4 - 12 wt% molybdenum (Mo) and will bring economic benefi ts if the valuable metals are recovered. In this article, the authors investigate the process of molybdenum recovery from spent hydrodesulphurisation (HDS) catalyst using the mixture of sodium carbonate and hydrogen peroxide mixture. Molybdenum recovery is dependent on the concentration of Na2CO3, H2O2 and pH in the reaction medium. Under the appropriate reaction conditions as 40g/L Na2CO3; 6 vol.% H2O2, room temperature, and reaction time = 2 hours, a molybdenum yield of 85% could be achieved. Carbon was used as asorbent for the recovery of molybdenum from the leach solution. With this method, recovery of molybdenum as MoO3 product of 95% purity was achieved. Key words: Spent HDS catalyst, Molybdenum trioxide, soda leach, H2O2 oxidative. Application of oxidative and soda leach method for selective recovery of molybdenum from spent hydrodesulfurisation catalysts Pham Xuan Nui, Pham Son Tung University of Mining and Geology
File đính kèm:
 ung_dung_phuong_phap_ngam_chiet_soda_va_tac_nhan_oxy_hoa_de.pdf
ung_dung_phuong_phap_ngam_chiet_soda_va_tac_nhan_oxy_hoa_de.pdf

