Sử dụng quặng Perlite làm vật liệu hấp phụ cho quá trình xử lý ô nhiễm Pb2+ trong nước
Perlite là khoáng tự nhiên đã được xử lý ở các nhiệt độ nung khác nhau. Việc khảo sát hình thái, cấu trúc của mẫu vật liệu Perlite được thực hiện bằng các phương pháp nhiễu xạ tia X (XRD)

Trang 1
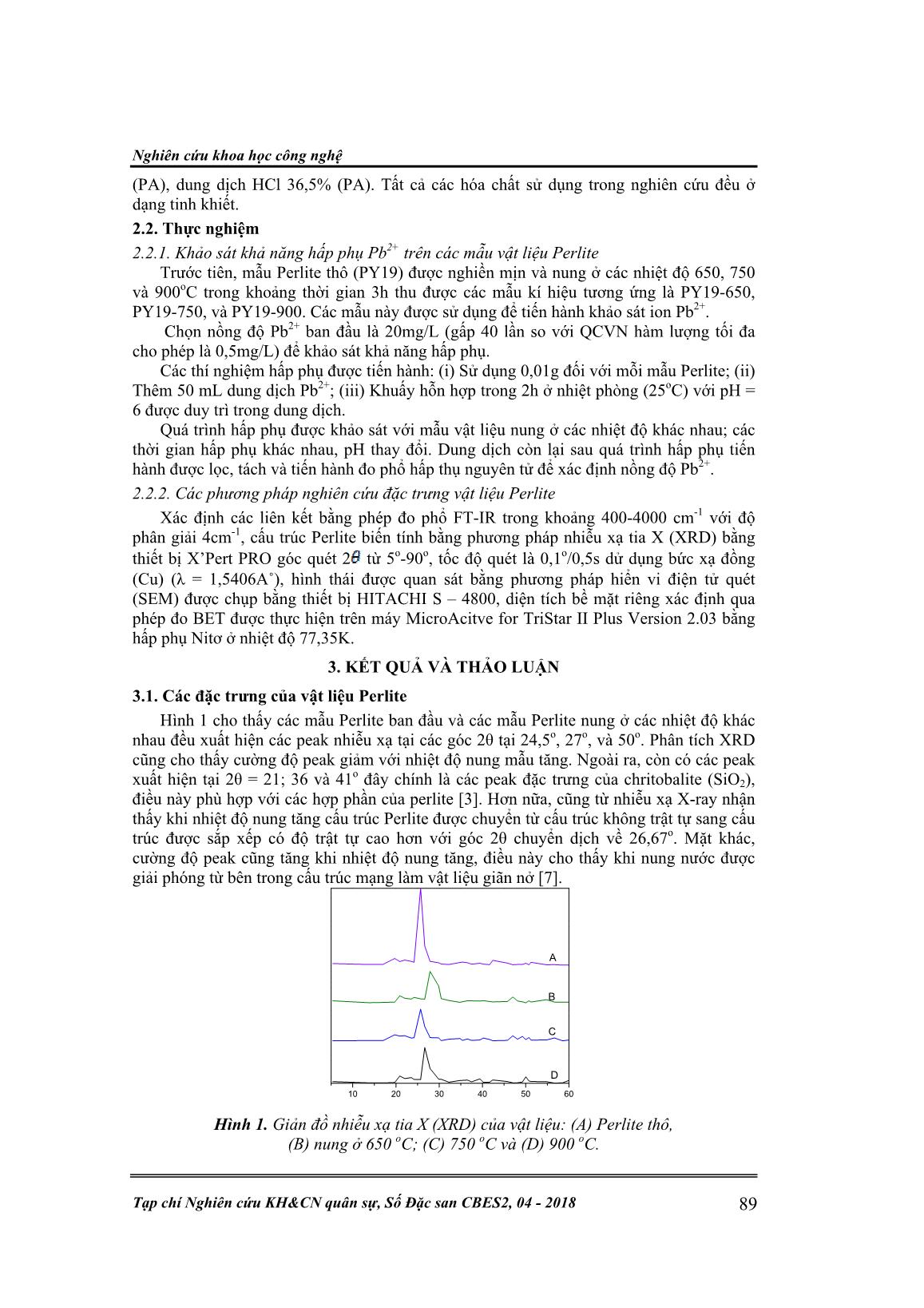
Trang 2

Trang 3
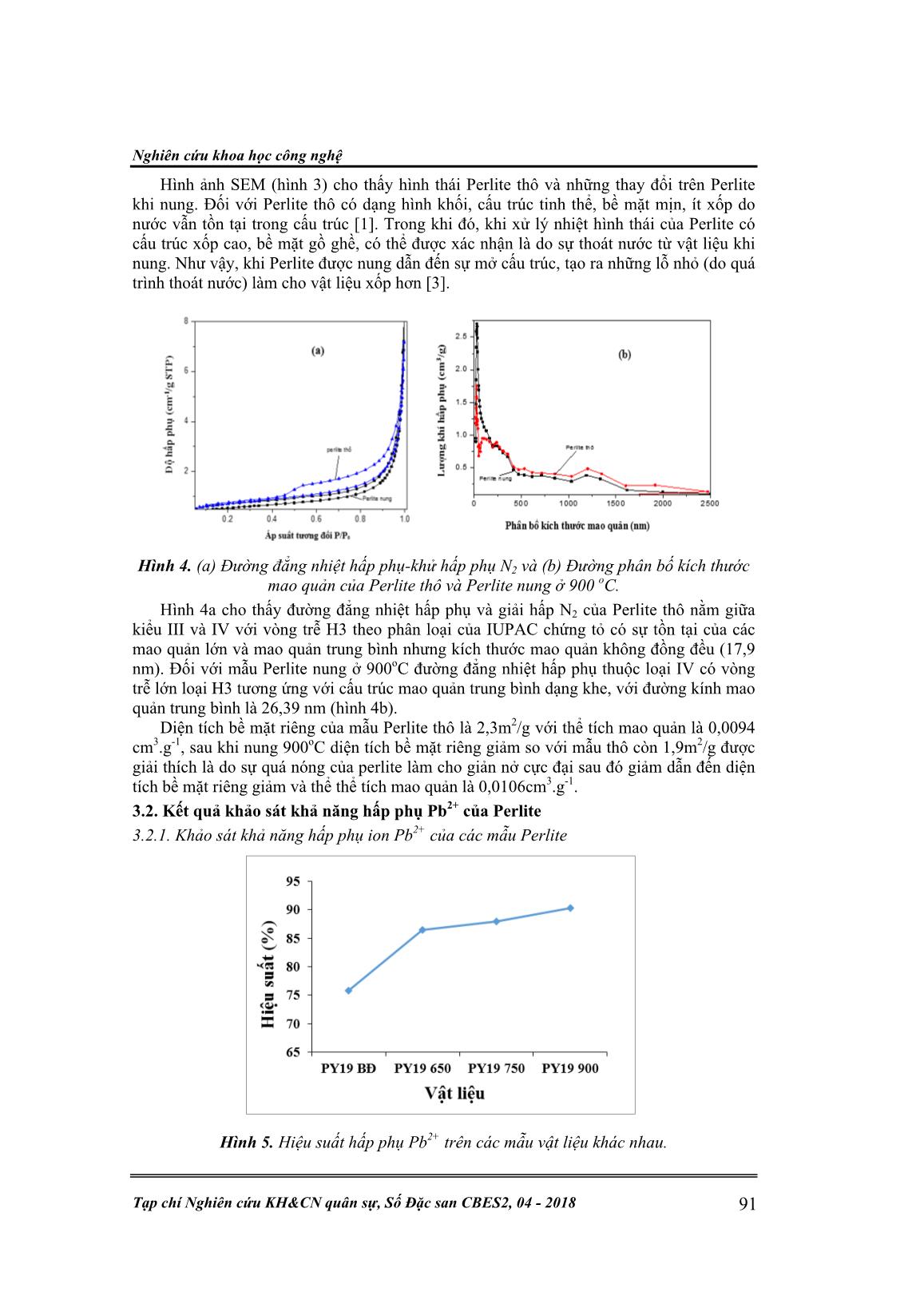
Trang 4
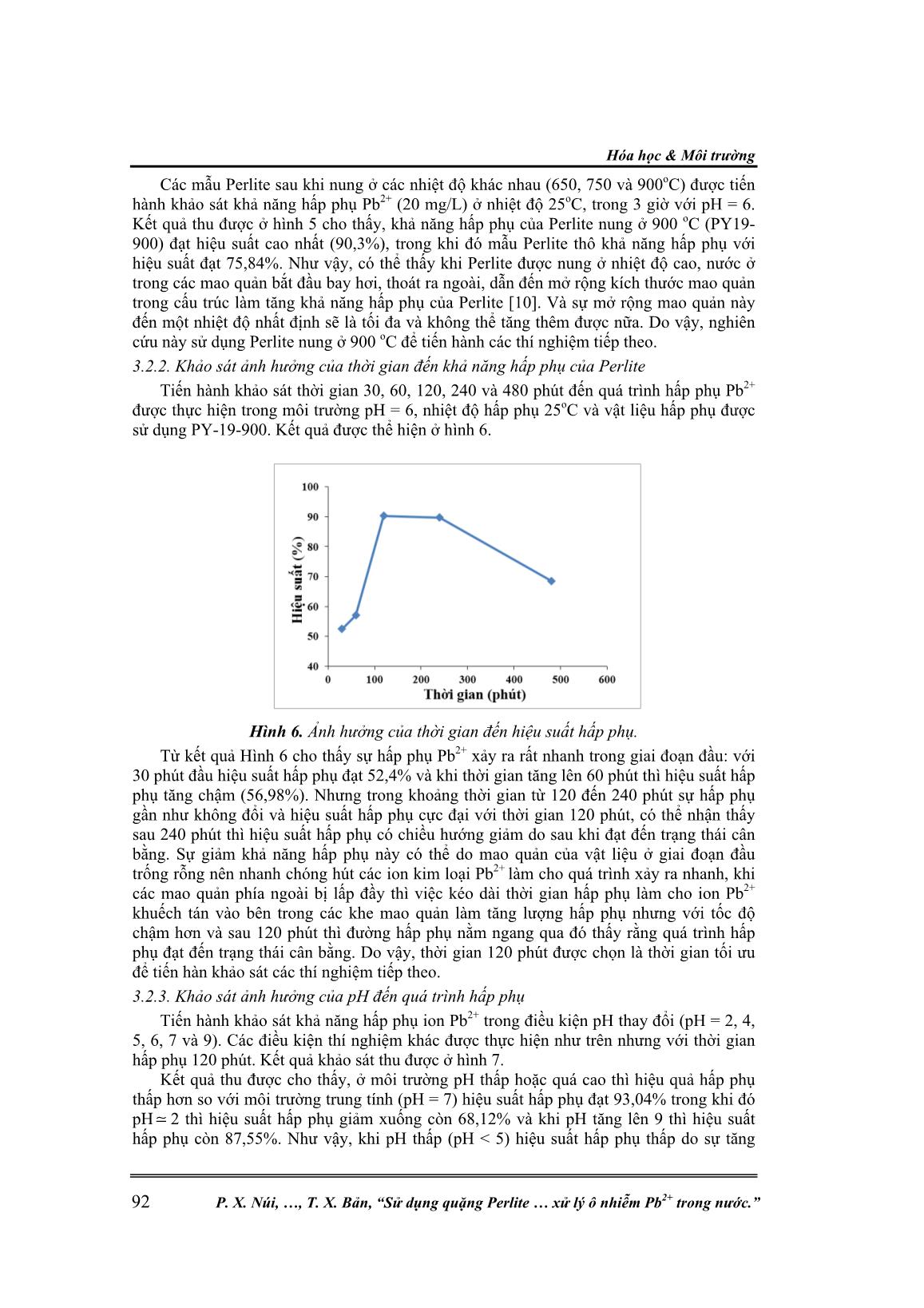
Trang 5
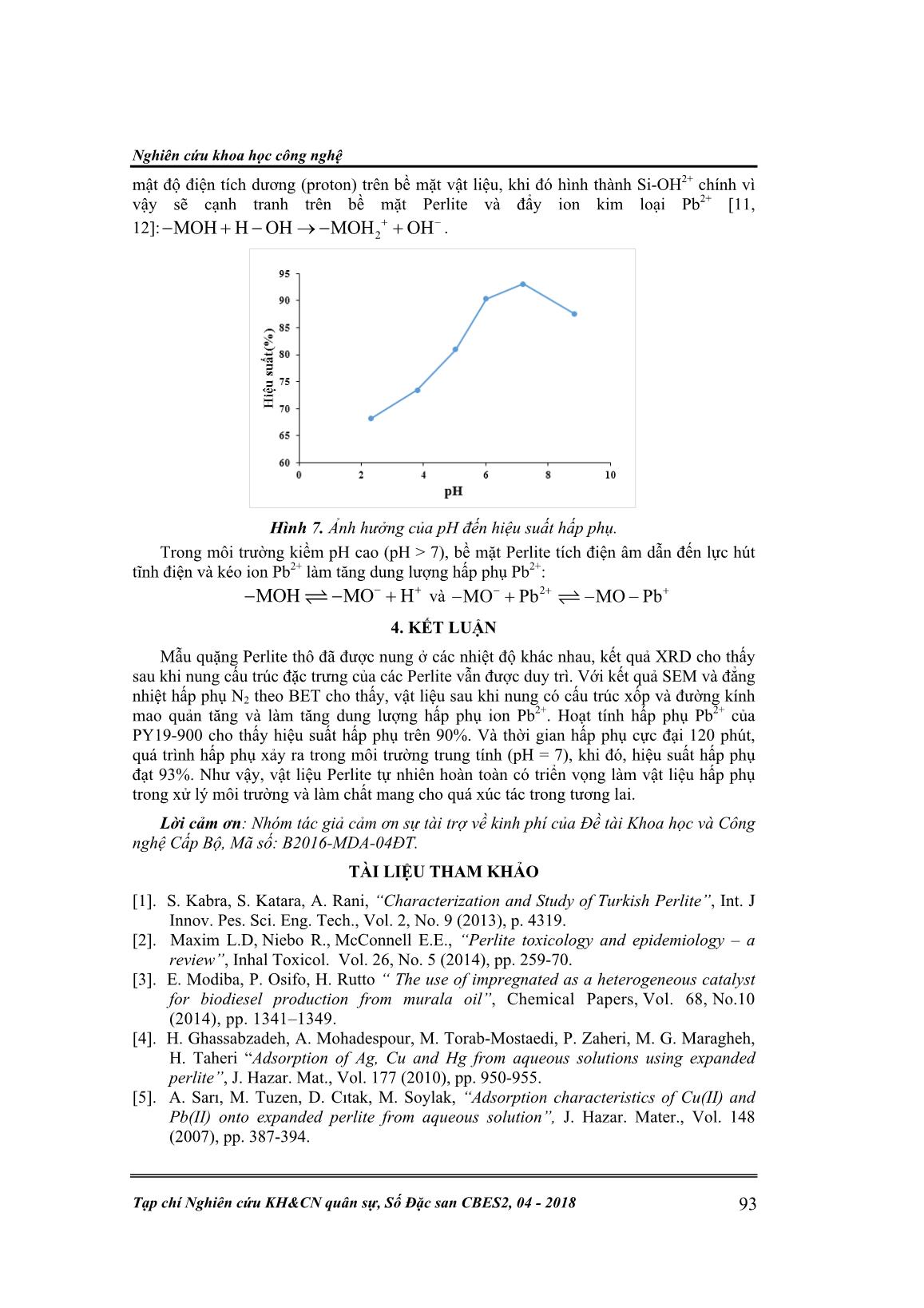
Trang 6

Trang 7
Bạn đang xem tài liệu "Sử dụng quặng Perlite làm vật liệu hấp phụ cho quá trình xử lý ô nhiễm Pb2+ trong nước", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Sử dụng quặng Perlite làm vật liệu hấp phụ cho quá trình xử lý ô nhiễm Pb2+ trong nước

Hóa học & Môi trường P. X. Núi, , T. X. Bản, “Sử dụng quặng Perlite xử lý ô nhiễm Pb2+ trong nước.” 88 SỬ DỤNG QUẶNG PERLITE LÀM VẬT LIỆU HẤP PHỤ CHO QUÁ TRÌNH XỬ LÝ Ô NHIỄM Pb2+ TRONG NƯỚC Phạm Xuân Núi1*, Đinh Xuân Hoàng1, Nguyễn Khắc Giảng2, Phạm Thị Vân Anh2, Tô Xuân Bản2 Tóm tắt: Perlite là khoáng tự nhiên đã được xử lý ở các nhiệt độ nung khác nhau. Việc khảo sát hình thái, cấu trúc của mẫu vật liệu Perlite được thực hiện bằng các phương pháp nhiễu xạ tia X (XRD), phổ hồng ngoại (FT-IR), hiển vi điện tử quét (SEM), và đẳng nhiệt hấp phụ-giải hấp phụ N2 theo BET. Nghiên cứu này bước đầu tiến hành khảo sát quá trình hấp phụ ion Pb2+ trong nước thải công nghiệp trên mẫu vật liệu Perlite. Khả năng hấp phụ Pb2+ được khảo sát với sự thay đổi pH, thời gian và trên các mẫu perlite được nung ở các nhiệt độ khác nhau. Kết quả thu được cho thấy, quá trình hấp phụ tối ưu ở pH = 7, thời gian hấp phụ 120 phút. Nghiên cứu này cho thấy quá trình hấp phụ Pb2+ trên vật liệu Perlite biến tính hoàn toàn có tính khả thi. Từ khóa: Perlite; Ion Pb2+; Perlite dãn nở; Hấp phụ. 1. MỞ ĐẦU Perlite là đá hydrat vô định hình được hydrat hóa, hình thành từ phun trào núi lửa có thành phần chủ yếu là silic oxit (70-75%), nhôm oxit (12-15%) ngoài ra có natri oxit (3- 4%), kali oxit (3-5%), sắt (III) oxit (0,5-2%), magie oxit (0,2-0,7) canxi oxit (0,5-1,5%) và nước (3-5%). Perlite khi được xử lý nhiệt trên 850oC nước sẽ bay hơi bên trong cấu trúc dẫn đến sự giãn nở bất thường của Perlite tăng lên gấp 7-16 lần so với cấu trúc ban đầu tạo ra vật liệu nhẹ, diện tích bề mặt đạt được khoảng 1,22m2/g, mật độ 0,6-2,3g/mL, kích thước hạt khoảng 0,2 - 4mm [1]. Perlite được sử dụng làm chất độn, thiết bị trợ lọc, sản xuất vật liệu xây dựng, trần ngói, thạch cao nhẹ, bê tông vật liệu cách điện, vật liệu hấp phụ, loại bỏ các ion kim loại nặng và các chất ô nhiễm khác từ khí quyển, loại bỏ thuốc nhuộm gây ô nhiễm nguồn nước [2]. Năm 2014, Edward Modiba và các cộng sự [3] đã sử dụng Perlite làm chất xúc tác dị thể để sản xuất Biodiesel từ dầu Marula, nhóm nghiên cứu đã sử dụng Perlite tẩm kali hydroxit (KOH) tạo ra hệ xúc tác dị thể cho phản ứng chuyển hóa Biodiesel thu được hiệu suất chuyển hóa là 91,4%. Xúc tác trên cơ sở Perlite cũng được tái chế đến 3 lần nhưng không có sự thay đổi hoạt tính, các nhiễu xạ tia X và BET cho thấy không có sự thay đổi về cấu trúc của Perlite, dầu sinh học sản xuất ra đáp ứng được tiêu chuẩn nhiên liệu sinh học [3]. Trong lĩnh vực hóa học, Perlite và Perlite biến tính được sử dụng là một chất hấp phụ [4-6]. Perlite có mật độ (tỷ trọng) thấp, diện tích bề mặt lớn, ngoài ra hầu hết các mẫu Pertile đều có hàm lượng silic cao (thường lớn hơn 70%) nên Perlite có đặc tính hấp phụ cao, do các nhóm silanol chi phối được hình thành bởi các nguyên tử silic trên bề mặt [8]. Trên cơ sở đó, trong nghiên cứu này, mẫu perlite tự nhiên thu được từ Phú Yên, Việt Nam được xử lý ở các nhiệt độ nung khác nhau sử dụng làm vật liệu hấp phụ ion Pb(II) trong nước được thực hiện. 2. THỰC NGHIỆM 2.1. Nguyên liệu và hóa chất Quặng Perlite thu được từ mỏ Phú Yên, Việt Nam (PY19) với thành phần SiO2 (68,51%); TiO2 (0,35%); Al2O3 (14,54%); FeO (3,52%); MnO (0,09%); MgO (1,04%); CaO (2,71%); Na2O (3,6%); K2O (4,29%); P2O5 (0,07%) và mất khí nung (LOI: 0,69%). Dung dịch Pb2+ được chuẩn bị từ muối 3 2 2Pd(CH COO) .3H O (PA), NaOH dạng viên Nghiên cứu khoa học công nghệ Tạp chí Nghiên cứu KH&CN quân sự, Số Đặc san CBES2, 04 - 2018 89 (PA), dung dịch HCl 36,5% (PA). Tất cả các hóa chất sử dụng trong nghiên cứu đều ở dạng tinh khiết. 2.2. Thực nghiệm 2.2.1. Khảo sát khả năng hấp phụ Pb2+ trên các mẫu vật liệu Perlite Trước tiên, mẫu Perlite thô (PY19) được nghiền mịn và nung ở các nhiệt độ 650, 750 và 900oC trong khoảng thời gian 3h thu được các mẫu kí hiệu tương ứng là PY19-650, PY19-750, và PY19-900. Các mẫu này được sử dụng để tiến hành khảo sát ion Pb2+. Chọn nồng độ Pb2+ ban đầu là 20mg/L (gấp 40 lần so với QCVN hàm lượng tối đa cho phép là 0,5mg/L) để khảo sát khả năng hấp phụ. Các thí nghiệm hấp phụ được tiến hành: (i) Sử dụng 0,01g đối với mỗi mẫu Perlite; (ii) Thêm 50 mL dung dịch Pb2+; (iii) Khuấy hỗn hợp trong 2h ở nhiệt phòng (25oC) với pH = 6 được duy trì trong dung dịch. Quá trình hấp phụ được khảo sát với mẫu vật liệu nung ở các nhiệt độ khác nhau; các thời gian hấp phụ khác nhau, pH thay đổi. Dung dịch còn lại sau quá trình hấp phụ tiến hành được lọc, tách và tiến hành đo phổ hấp thụ nguyên tử để xác định nồng độ Pb2+. 2.2.2. Các phương pháp nghiên cứu đặc trưng vật liệu Perlite Xác định các liên kết bằng phép đo phổ FT-IR trong khoảng 400-4000 cm-1 với độ phân giải 4cm-1, cấu trúc Perlite biến tính bằng phương pháp nhiễu xạ tia X (XRD) bằng thiết bị X’Pert PRO góc quét 2 từ 5o-90o, tốc độ quét là 0,1o/0,5s dử dụng bức xạ đồng (Cu) (λ = 1,5406A˚), hình thái được quan sát bằng phương pháp hiển vi điện tử quét (SEM) được chụp bằng thiết bị HITACHI S – 4800, diện tích bề mặt riêng xác định qua phép đo BET được thực hiện trên máy MicroAcitve for TriStar II Plus Version 2.03 bằng hấp phụ Nitơ ở nhiệt độ 77,35K. 3. KẾT QUẢ VÀ THẢO LUẬN 3.1. Các đặc trưng của vật liệu Perlite Hình 1 cho thấy các mẫu Perlite ban đầu và các mẫu Perlite nung ở các nhiệt độ khác nhau đều xuất hiện các peak nhiễu xạ tại các góc 2θ tại 24,5o, 27o, và 50o. Phân tích XRD cũng cho thấy cường độ peak giảm với nhiệt độ nung mẫu tăng. Ngoài ra, còn có các peak xuất hiện tại 2θ = 21; 36 và 41o đây chính là các peak đặc trưng của chritobalite (SiO2), điều này phù hợp với các hợp phần của perlite [3]. Hơn nữa, cũng từ nhiễu xạ X-ray nhận thấy khi nhiệt độ nung tăng cấu trúc Perlite được chuyển từ cấu trúc không trật tự sang cấu trúc được sắp xếp có độ trật tự cao hơn với góc 2θ chuyển dịch về 26,67o. Mặt khác, cường độ peak cũng tăng khi nhiệt độ nung tăng, điều này cho thấy khi nung nước được
File đính kèm:
 su_dung_quang_perlite_lam_vat_lieu_hap_phu_cho_qua_trinh_xu.pdf
su_dung_quang_perlite_lam_vat_lieu_hap_phu_cho_qua_trinh_xu.pdf

