Phương pháp tổng quát tổng hợp chấm lượng tử Carbon pha tạp kim loại
Chấm lượng tử carbon (CQDs) là họ vật liệu nano carbon mới, có tiềm năng ứng dụng lớn trong nhiều lĩnh vực quan trọng do chúng không độc hại, tan trong nước, tương thích sinh học, có thể phát xạ ánh sáng trong vùng nhìn thấy và dễ tổng hợp.

Trang 1

Trang 2

Trang 3
Trang 4

Trang 5
Trang 6

Trang 7

Trang 8
Bạn đang xem tài liệu "Phương pháp tổng quát tổng hợp chấm lượng tử Carbon pha tạp kim loại", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Phương pháp tổng quát tổng hợp chấm lượng tử Carbon pha tạp kim loại

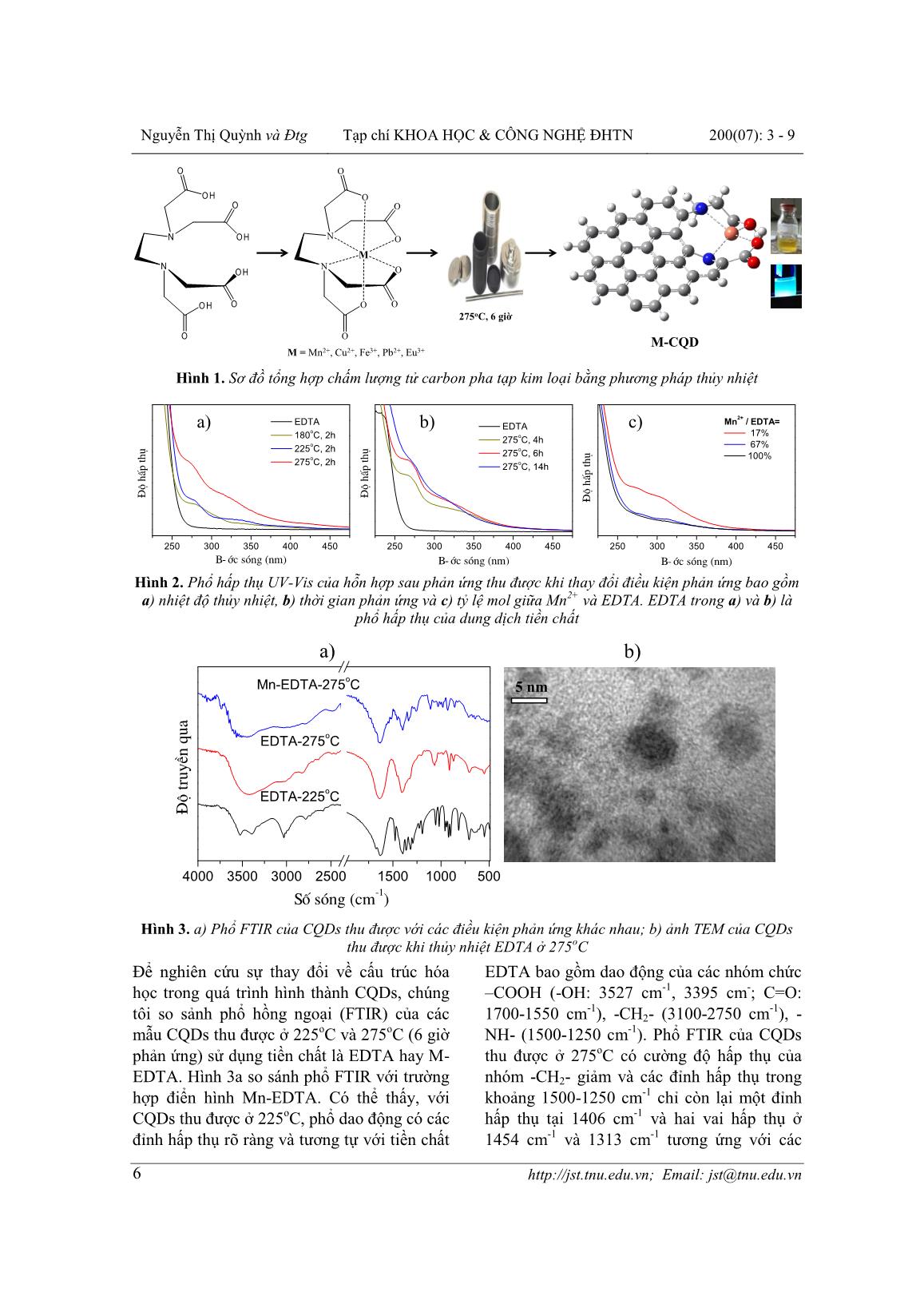
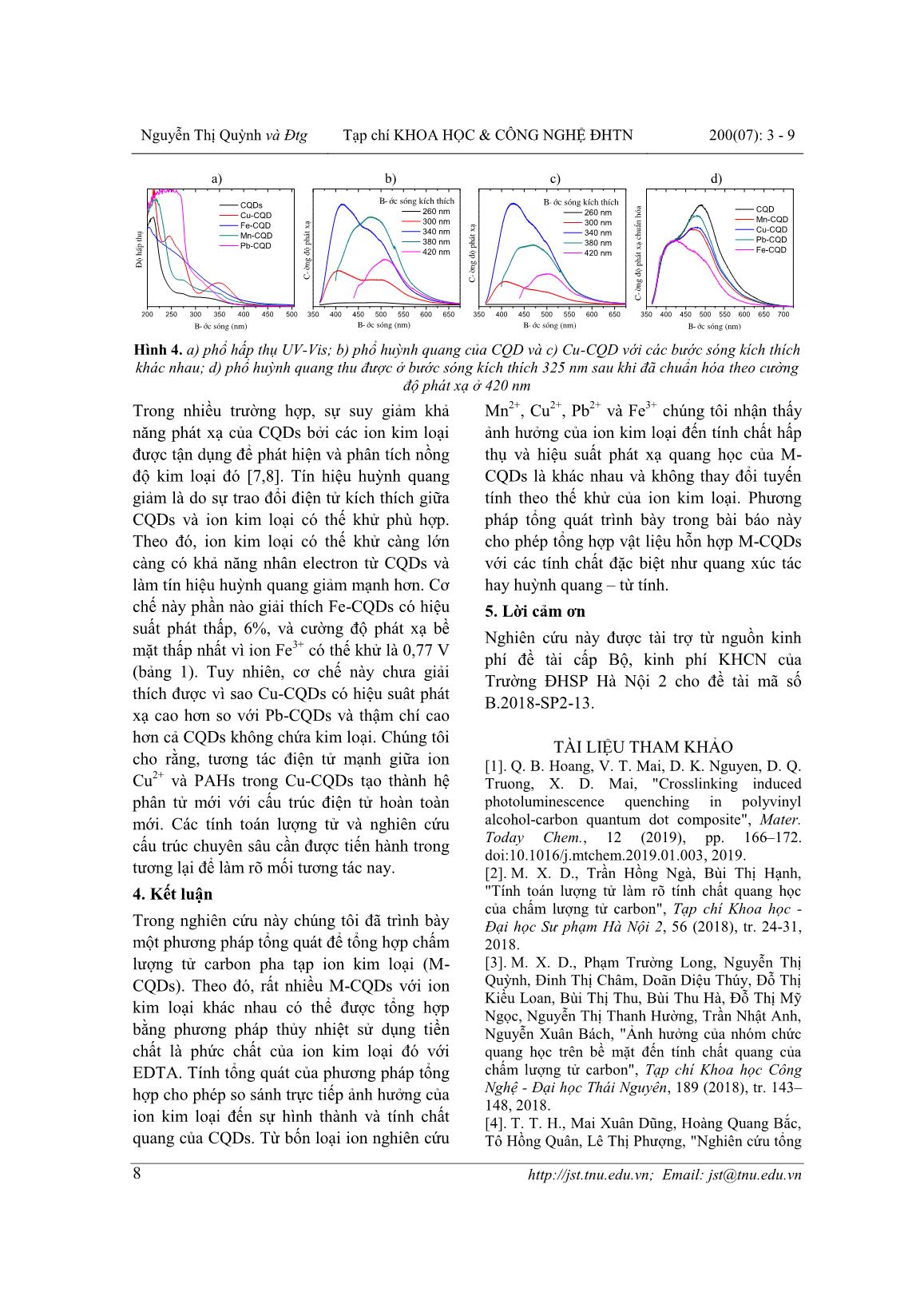
ISSN: 1859-2171 TNU Journal of Science and Technology 200(07): 3 - 9 Email: jst@tnu.edu.vn 3 PHƯƠNG PHÁP TỔNG QUÁT TỔNG HỢP CHẤM LƯỢNG TỬ CARBON PHA TẠP KIM LOẠI Nguyễn Thi Quỳnh1,2, Nguyễn Thị Tuyến1, Phạm Thi Mai1, Nguyễn Thị Lan Anh1, Lê Thi Phương1, Nguyễn Thị Phượng1, Nguyễn Thị Kiều Trinh1, Vũ Anh Đức1, Phạm Trường Long3, Mai Xuân Dũng*1 1Trường Đại học Sư phạm Hà Nội 2, 2Trường Đại học Khoa học Tự nhiên - Đại học Quốc gia Hà Nội, 3Đại học Cần Thơ TÓM TẮT Chấm lượng tử carbon (CQDs) là họ vật liệu nano carbon mới, có tiềm năng ứng dụng lớn trong nhiều lĩnh vực quan trọng do chúng không độc hại, tan trong nước, tương thích sinh học, có thể phát xạ ánh sáng trong vùng nhìn thấy và dễ tổng hợp. Pha tạp CQDs với ion kim loại được kỳ vọng có thể đưa thêm các tính năng như xúc tác hay từ tính cho CQDS định hướng ứng dụng trong các lĩnh vực như quang xúc tác, đánh dấu và phân tích sinh học. Trong nghiên cứu này, chúng tôi nghiên cứu tổng hợp CQDs pha tạp kim loại sử dụng phức chất ethylenediaminetetraacetic acid (EDTA) với kim loại (Cu, Fe, Mn, Pb) bằng phương pháp thủy nhiệt. Phân tích kim loại bằng phổ hấp thụ nguyên tử cho thấy M-CQDs chứa từ 3% đến 13% khối lượng kim loại. So sánh phổ hấp thụ và phổ phát xạ của các M-CQDs với nhau và với CQDs cho thấy bản chất ion kim loại ảnh hưởng đến tính chất hấp thụ trong vùng tử ngoại và hiệu suất phát xạ huỳnh quang của CQDs. Phương pháp tổng hợp trình bày trong bài báo này mang tính tổng quát và cho phép tổng hợp nhiều M-CQDs để so sánh trực tiếp ảnh hưởng của ion kim loại đến tính chất của CQDs. Từ khóa: chấm lượng tử carbon, pha tạp kim loại, thủy nhiệt, huỳnh quang, tương tác điện tử. Ngày nhận bài: 16/3/2019; Ngày hoàn thiện: 02/4/2019;Ngày duyệt đăng: 04 /5/2019 UNIVERSAL METHOD FOR PREPARATION OF METAL-DOPED CARBON QUANTUM DOTS Nguyen Thi Quynh 1,2 , Nguyen Thi Tuyen 1 , Pham Thi Mai 1 , Nguyen Thi Lan Anh 1 , Le Thi Phuong 1 , Nguyen Thi Phuong 1 , Nguyen Thi Kieu Trinh 1 , Vu Anh Duc 1 , Pham Truong Long 3 , Mai Xuan Dung *1 1Hanoi Pedagogical University 2, 2VNU University of Science, 3Can Tho University ABSTRACT Carbon quantum dots (CQDs) have been drawn much attention for diverse application due to their low toxicity, excellent biocompatibility, visible photoluminescence and easy synthesis. Doping CQDs with metal ions has been demonstrated to add functionalities such as catalytic and magnetic properties for photocatalysis, bio-imaging and bioanalytic applications. Herein, we repot a universal method for preparation of metal doped CQDs (M-CQDs, M= Cu 2+ , Fe 3+ , Mn 2+ and Pb 2+ ). The universary is enabled by using complexes of the metal ions with ethylenediaminetetraacetic acid (EDTA) as single precursor. The mass fraction of metal varied from 3 to 13% as determined by atomic absoption spectroscopy. Optical properties of CQDs and M-CQDs were studied by UV- Vis absorption and photoluminescence spectroscopy. Metal ions such as Fe 3+ , Pb 2+ and Cu +2 change the absorption profile in the UV region and while the emission quantum yield of QDs varied from 6 to 27%. The method is of importance for preparation of a series of M-CQDs from which the effects of metal ions on the properties of CQDs can be revealed. Keywords: carbon quantum dots, metal doping, hydrothermal, photoluminescence, electronic interactions. Received: 16/3/2019; Revised: 02/4/2019;Approved: 04/5/2019 * Corresponding author: Email: xdmai@hpu2.edu.vn Nguyễn Thị Quỳnh và Đtg Tạp chí KHOA HỌC & CÔNG NGHỆ ĐHTN 200(07): 3 - 9 Email: jst@tnu.edu.vn 4 1. Giới thiệu Chấm lượng tử carbon (CQDs) là nhóm vật liệu carbon có kích thước cỡ nanomet (nm), có cấu trúc khá phức tạp gồm ba hợp phần chính: hệ đa vòng liên hợp PAHs (polyaromatic hydrocarbons), nhóm chức quang hoạt F (fluorophore) và các nhóm chức hữu cơ đơn giản như mạch hydrocarbon no, - OH, -COOH, -CONH- hay -NH- [1]. Trong khi các nhóm chức phân cực đơn giản quyết định đến tính tan của CQDs, kích thước của PAHs, cấu trúc của F và tương tác giữa PAHs và F quyết định đến tính chất hấp thụ và phát xạ quang học của CQDs [2–4]. Mặc dù cấu trúc của CQDs chưa được làm sáng tỏ như đối với CdSe, PhS, InP hay Si QDs [5], CQDs đang thu hút được sự quan tâm nghiên cứu vì các tính chất nổi bật như không độc hại, tan trong nước, tương thích sinh học, phát xạ huỳnh quang trong giải ánh sáng nhìn thấy và tương đối dễ tổng hợp [4,6]. Cho đến nay, CQDs đã được nghiên cứu ứng dụng trong nhiều lĩnh vực khác nhau như vật liệu chuyển đổi quang học trong đèn chiếu sáng diode (LEDs), đầu dò huỳnh quang trong phân tính tế bào và đánh dấu sinh học, xúc tác quang hóa, vật liệu hấp thụ và chuyển hóa quang - điện trong pin mặt trời, vật liệu huỳnh huỳnh quang phân tích ion kim loại nặng [7], [8] và nhiều ứng dụng khác [9]. Để khai thác các tính chất quang và ưu điểm tương thích sinh học của CQDs, người ta kết hợp CQDs với các ion kim loại có từ tính (Gd, Fe), có hoạt tính xúc tác (Fe, Cu, Ni, ), hay có tính chất huỳnh quang (Eu) để tạo thành vật liệu lai đa chức năng [10–13]. CQDs pha tạp kim loại (M-CQDs) ngoài những tính chất vốn có của CQDs và ion kim loại còn xuất hiện thêm nhiều tính chất hóa lý quan trọng khác như độ hấp thụ vùng khả kiến tăng hay chuyển dịch phổ phát xạ sang vùng bước sóng lớn hơn. Các tính chất này xuất phát từ tương tác điện tử giữa hệ liên hợp trong CQDs và ion kim loại. Để tổng hợp M-CQDs, một số phương pháp đã được nghiên cứu như thủy nhiệt, nhiệt vi sóng, nhiệt phân, hay phương pháp đính ion kim loại [10]. Trong các phương pháp này, phương pháp thủy nhiệt hỗn hợp của muối ion kim loại với tiền chất carbon như citric acid, ascorbic acid, hay các polymer được sử dụng phổ biến vì thân thiện với môi trường và dễ thực hiện. Mặc dù vậy, với mỗi ion kim loại khác nhau cần lựa chọn tiền chất ... cho các thí nghiệp tiếp theo. Khi tăng thời gian thủy nhiệt từ 2h lên 14 giờ, hình 2b cho thấy độ hấp thụ ở 350 nm tăng dần chứng tỏ nồng độ CQDs tăng theo thời gian phản ứng. Tuy nhiên, ở thời gian phản ứng dài, ví dụ 14h, chúng tôi thu được lượng đáng kể cặn carbon không tan trong nước. Do vậy, chúng tôi lựa chọn điều kiện phản ứng tối ưu là 275oC và 6h. Để khảo sát ảnh hưởng của ion kim loại đến sự hình thành CQDs từ EDTA, chúng tôi thủy nhiệt hỗn hợp Mn2+ - EDTA (275oC, 6h) với tỷ lệ mole Mn2+/EDTA khác nhau. Phổ hấp thụ trên hình 2c cho thấy, độ hấp thụ ở 350 nm giảm dần khi tỷ lệ Mn2+/EDTA tăng dần. Điều này chứng tỏ sự tạo phức giữa Mn2+ và EDTA làm cho quá trình chuyển hóa EDTA thành CQDs khó hơn và nhóm liên kết bền Mn- EDTA có thể được duy trì ở CQDs cuối cùng. Nguyễn Thị Quỳnh và Đtg Tạp chí KHOA HỌC & CÔNG NGHỆ ĐHTN 200(07): 3 - 9 Email: jst@tnu.edu.vn 6 OH N OH O N OH O OH O O ON O O N O O O O O M M = Mn2+, Cu2+, Fe3+, Pb2+, Eu3+ 275oC, 6 giờ M-CQD Hình 1. Sơ đồ tổng hợp chấm lượng tử carbon pha tạp kim loại bằng phương pháp thủy nhiệt 250 300 350 400 450 § é h Êp t h ô B-íc sãng (nm) EDTA 180 o C, 2h 225 o C, 2h 275 o C, 2h 250 300 350 400 450 § é h Êp t h ô B-íc sãng (nm) EDTA 275 o C, 4h 275 o C, 6h 275 o C, 14h 250 300 350 400 450 § é h Êp t h ô B-íc sãng (nm) Mn 2+ / EDTA= 17% 67% 100% a) b) c) Hình 2. Phổ hấp thụ UV-Vis của hỗn hợp sau phản ứng thu được khi thay đổi điều kiện phản ứng bao gồm a) nhiệt độ thủy nhiệt, b) thời gian phản ứng và c) tỷ lệ mol giữa Mn2+ và EDTA. EDTA trong a) và b) là phổ hấp thụ của dung dịch tiền chất 4000 3500 3000 2500 1500 1000 500 Mn-EDTA-275 o C EDTA-275 o C § é t ru y Òn q u a Sè sãng (cm -1 ) EDTA-225 o C 5 nm a) b) Hình 3. a) Phổ FTIR của CQDs thu được với các điều kiện phản ứng khác nhau; b) ảnh TEM của CQDs thu được khi thủy nhiệt EDTA ở 275oC Để nghiên cứu sự thay đổi về cấu trúc hóa học trong quá trình hình thành CQDs, chúng tôi so sảnh phổ hồng ngoại (FTIR) của các mẫu CQDs thu được ở 225oC và 275oC (6 giờ phản ứng) sử dụng tiền chất là EDTA hay M- EDTA. Hình 3a so sánh phổ FTIR với trường hợp điển hình Mn-EDTA. Có thể thấy, với CQDs thu được ở 225oC, phổ dao động có các đỉnh hấp thụ rõ ràng và tương tự với tiền chất EDTA bao gồm dao động của các nhóm chức –COOH (-OH: 3527 cm-1, 3395 cm-; C=O: 1700-1550 cm -1 ), -CH2- (3100-2750 cm -1 ), - NH- (1500-1250 cm -1). Phổ FTIR của CQDs thu được ở 275oC có cường độ hấp thụ của nhóm -CH2- giảm và các đỉnh hấp thụ trong khoảng 1500-1250 cm-1 chỉ còn lại một đỉnh hấp thụ tại 1406 cm-1 và hai vai hấp thụ ở 1454 cm -1 và 1313 cm -1 tương ứng với các Nguyễn Thị Quỳnh và Đtg Tạp chí KHOA HỌC & CÔNG NGHỆ ĐHTN 200(07): 3 - 9 Email: jst@tnu.edu.vn 7 hấp thụ dao động của nhóm alkyl nối với vòng thơm. Như vậy, khi tăng nhiệt độ thủy nhiệt, các nhóm –N-H, C-H, -C=O, -OH tham gia vào quá trình đề hydrat hóa để tạo thành cấu trúc PAHs. Ảnh TEM chụp mẫu CQDs thu được khi thủy nhiệt ở 275oC, hình 3b, cho thấy CQDs thu được có kích thước thay đổi trong khoảng 2-8 nm. Để xác định hàm lượng kim loại có trong M- CQDs, chúng tôi sử dụng phương pháp phân tích khối lượng kết hợp với phổ hấp thụ nguyên tử, kết quả được tóm tắt trong bảng 1. Phần trăm khối lượng kim loại trong M- CQDs thay đổi trong khoảng từ 3 đến 12,8%. Phổ hấp thụ và phổ phát xạ huỳnh quang của CQDs và M-CQDs được trình bày trong hình 4. So sanh phổ hấp thụ UV-Vis của các loại CQDs khác nhau trên hình 4a cho thấy Mn- CQDs và CQDs có phổ hấp thụ tương tự nhau trong khi các ion Fe 3+ , Cu 2+ và Pb 2+ làm thay đổi đang kể dải hấp thụ trong khoảng 250 – 400 nm. Đặc biệt, trên phổ hấp thụ của Cu- CQDs xuất hiện một vùng hấp thụ đặc trưng khá rộng ở khoảng 350 nm. Chúng tôi lưu ý rằng, trong bài báo này M-CQDs thu được bằng cách thủy nhiệt phức chất M-EDTA tương ứng; không trùng lặp với các phương pháp tổng M-CQDs đã công bố. Do đó, cấu trúc chi tiết và phổ hấp thụ của M-CQDs thu được từ M-EDTA khác so với M-CQDs công bố bởi các nhóm tác giả khác [11–13]. Ví dụ, Cu-CQDs tổng hợp từ hỗn hợp của Cu2+ và 1- (2-pyridylazo)-2-naphthol có một đỉnh hấp thụ rộng ở 550 nm và hai vai hấp thụ ở 330 nm và 270 nm [13]. Mn-CQDs thu được khi thủy nhiệt hỗn hợp của citric acid và Mn2+ có một đỉnh hấp thụ rộng ở khoảng 350 nm [12]. Sự thay đổi trong phổ hấp của M-CQDs (M=Cu, Fe, Pb) so với CQDs và chứng tỏ có sự tương tác điện tử giữa ion kim loại trung tâm và cấu trúc PAHs bên trong CQDs. Có lẽ tính toán lý thuyết trên phức chất của PAHs với các ion kim loại khác nhau sẽ giải thích tốt hơn phổ hấp thụ của M-CQDs trên hình 4a. Chúng tôi hy vọng có thể trình bày kết quả này trong một bài báo riêng biệt sắp tới. CQDs và M-CQDs đều có phổ phát dạ dạng đám với vùng phát xạ từ 365 nm đến 625 nm và cực đại phát xạ ở khoảng 450±50 nm, hình 4d. Cấu trúc của phổ phát xạ phụ thuộc vào bước sóng ánh sáng kích thích. Trên hình 4b và 4c là phổ phát xạ của CQDs và Cu-CQDs thu được ở các bước sóng kích thích khác nhau. Các CQDs có hai tâm phát xạ chủ yếu ở bước sóng 420 nm và 482 nm tương ứng với sự phát xạ từ lõi PAHs và sự phát xạ có tham gia của các nhóm chức bề mặt trên CQDs. Trong [13], Tan và cộng sự cho rằng, tâm phát xạ ở khoảng 482 nm xuất phát từ cấu trúc phức của ion Cu2+ trong khi phát xạ ở khoảng 420 nm xuất phát từ các PAHs. Để thấy rõ hơn ảnh hưởng của ion kim loại đến phổ phát xạ của CQDs, chúng tôi chuẩn hóa phổ phát xạ theo cường độ phát xạ của PAHs ở 420 nm như hình 4d. Có thể thấy, so với CQDs, M-CQDs có cường độ phát xạ bề mặt giảm và giảm dần theo thứ tự Pb2+, Cu2+, Mn 2+ , Fe 3+ . Để tính hiệu suất phát xạ của CQDs và M- CQDs, chúng tôi so sánh phổ phát xạ của mẫu nghiên cứu với dung dịch quinine sulfate, chất chuẩn có hiệu suất phát xạ là 55%; kết quả được tóm tắt trong bảng 1. Hiệu suất phát xạ của M-CQDs thay đổi trong khoảng 6 đến 27 % tùy thuộc vào ion kim loại. Khi so với CQDs, Mn 2+ và Cu 2+ loại tăng hiệu suất phát xạ của CQDs trong khi Fe3+ và Pb2+ làm giảm khả năng phát xạ. Bảng 1. Hàm lượng kim loại (%) và hiệu suất phát xạ lượng tử (QY) của CQDs CQDs Mn- Pb- Cu- Fe- * % - 3,0 12,8 4,4 4,0 E (V) - -1,04 -0,13 0,35 0,77 ** QY (%) 18 25 9 27 6 * phần trăm khối lượng xác định bằng AAS ** xác định bằng cách so sánh với quinine sulfate ở bước sóng kích thích 350 nm Nguyễn Thị Quỳnh và Đtg Tạp chí KHOA HỌC & CÔNG NGHỆ ĐHTN 200(07): 3 - 9 Email: jst@tnu.edu.vn 8 350 400 450 500 550 600 650 C - ê n g ® é p h ¸ t x ¹ B-íc sãng (nm) B-íc sãng kÝch thÝch 260 nm 300 nm 340 nm 380 nm 420 nm 200 250 300 350 400 450 500 § é h Ê p t h ô B-íc sãng (nm) CQDs Cu-CQD Fe-CQD Mn-CQD Pb-CQD 350 400 450 500 550 600 650 C - ê n g ® é p h ¸ t x ¹ B-íc sãng (nm) B-íc sãng kÝch thÝch 260 nm 300 nm 340 nm 380 nm 420 nm a) b) c) d) 350 400 450 500 550 600 650 700 C - ê n g ® é p h ¸ t x ¹ c h u È n h ã a B-íc sãng (nm) CQD Mn-CQD Cu-CQD Pb-CQD Fe-CQD Hình 4. a) phổ hấp thụ UV-Vis; b) phổ huỳnh quang của CQD và c) Cu-CQD với các bước sóng kích thích khác nhau; d) phổ huỳnh quang thu được ở bước sóng kích thích 325 nm sau khi đã chuẩn hóa theo cường độ phát xạ ở 420 nm Trong nhiều trường hợp, sự suy giảm khả năng phát xạ của CQDs bởi các ion kim loại được tận dụng để phát hiện và phân tích nồng độ kim loại đó [7,8]. Tín hiệu huỳnh quang giảm là do sự trao đổi điện tử kích thích giữa CQDs và ion kim loại có thế khử phù hợp. Theo đó, ion kim loại có thế khử càng lớn càng có khả năng nhân electron từ CQDs và làm tín hiệu huỳnh quang giảm mạnh hơn. Cơ chế này phần nào giải thích Fe-CQDs có hiệu suất phát thấp, 6%, và cường độ phát xạ bề mặt thấp nhất vì ion Fe3+ có thế khử là 0,77 V (bảng 1). Tuy nhiên, cơ chế này chưa giải thích được vì sao Cu-CQDs có hiệu suât phát xạ cao hơn so với Pb-CQDs và thậm chí cao hơn cả CQDs không chứa kim loại. Chúng tôi cho rằng, tương tác điện tử mạnh giữa ion Cu 2+ và PAHs trong Cu-CQDs tạo thành hệ phân tử mới với cấu trúc điện tử hoàn toàn mới. Các tính toán lượng tử và nghiên cứu cấu trúc chuyên sâu cần được tiến hành trong tương lại để làm rõ mối tương tác nay. 4. Kết luận Trong nghiên cứu này chúng tôi đã trình bày một phương pháp tổng quát để tổng hợp chấm lượng tử carbon pha tạp ion kim loại (M- CQDs). Theo đó, rất nhiều M-CQDs với ion kim loại khác nhau có thể được tổng hợp bằng phương pháp thủy nhiệt sử dụng tiền chất là phức chất của ion kim loại đó với EDTA. Tính tổng quát của phương pháp tổng hợp cho phép so sánh trực tiếp ảnh hưởng của ion kim loại đến sự hình thành và tính chất quang của CQDs. Từ bốn loại ion nghiên cứu Mn 2+ , Cu 2+ , Pb 2+ và Fe 3+ chúng tôi nhận thấy ảnh hưởng của ion kim loại đến tính chất hấp thụ và hiệu suất phát xạ quang học của M- CQDs là khác nhau và không thay đổi tuyến tính theo thế khử của ion kim loại. Phương pháp tổng quát trình bày trong bài báo này cho phép tổng hợp vật liệu hỗn hợp M-CQDs với các tính chất đặc biệt như quang xúc tác hay huỳnh quang – từ tính. 5. Lời cảm ơn Nghiên cứu này được tài trợ từ nguồn kinh phí đề tài cấp Bộ, kinh phí KHCN của Trường ĐHSP Hà Nội 2 cho đề tài mã số B.2018-SP2-13. TÀI LIỆU THAM KHẢO [1]. Q. B. Hoang, V. T. Mai, D. K. Nguyen, D. Q. Truong, X. D. Mai, "Crosslinking induced photoluminescence quenching in polyvinyl alcohol-carbon quantum dot composite", Mater. Today Chem., 12 (2019), pp. 166–172. doi:10.1016/j.mtchem.2019.01.003, 2019. [2]. M. X. D., Trần Hồng Ngà, Bùi Thị Hạnh, "Tính toán lượng tử làm rõ tính chất quang học của chấm lượng tử carbon", Tạp chí Khoa học - Đại học Sư phạm Hà Nội 2, 56 (2018), tr. 24-31, 2018. [3]. M. X. D., Phạm Trường Long, Nguyễn Thị Quỳnh, Đinh Thị Châm, Doãn Diệu Thúy, Đỗ Thị Kiều Loan, Bùi Thị Thu, Bùi Thu Hà, Đỗ Thị Mỹ Ngọc, Nguyễn Thị Thanh Hường, Trần Nhật Anh, Nguyễn Xuân Bách, "Ảnh hưởng của nhóm chức quang học trên bề mặt đến tính chất quang của chấm lượng tử carbon", Tạp chí Khoa học Công Nghệ - Đại học Thái Nguyên, 189 (2018), tr. 143– 148, 2018. [4]. T. T. H., Mai Xuân Dũng, Hoàng Quang Bắc, Tô Hồng Quân, Lê Thị Phượng, "Nghiên cứu tổng Nguyễn Thị Quỳnh và Đtg Tạp chí KHOA HỌC & CÔNG NGHỆ ĐHTN 200(07): 3 - 9 Email: jst@tnu.edu.vn 9 hợp chấm lượng tử carbon với hiệu suất lượng tử cao", Tạp chí Khoa học - Đại học Sư phạm Hà Nội 2, 47 (2017), tr. 20-25, 2017. [5]. V. T. Mai, N. H. Duong, X. D. Mai, "Surface polarity controls the optical properties of one-pot synthesized silicon quantum dots", Chem. Phys., 518 (2019), pp. 107-111. doi:10.1016/j.chemphys.2018.11.012, 2019. [6]. M. V. T., Hoàng Quang Bắc, Trần Thu Hương, Đinh Thị Châm, Nguyễn Thị Loan, Nguyễn Thị Quỳnh, Bùi Thị Huệ, Lê Thị Thùy Hương, Mai Xuân Dũng, "Nghiên cứu tổng hợp hạt nano huỳnh quang từ một số rau củ quả", Tạp chí Hóa học ứng dụng, 4 (2017), tr. 70-73, 2017. [7]. M. X. D., Đăng Thị Thu Huyền, Nguyễn Thị Quỳnh, Lê Thị Hằng, Lê Quang Trung, Đỗ Thị Thu Hòa, Phạm Thị Hải Yến, "Tổng hợp polymer nano carbon từ thực phẩm và ứng dụng của nó trong phát hiện ion Pb (II)", Tạp chí Khoa học Công nghệ - Đại học Thái Nguyên, 189 (2018) tr. 45-51, 2018. [8]. M. X. D., Đăng Thị Thu Huyền, Lê Thị Thùy Hương, Lê Quang Trung, Đỗ Thị Kiều Loan, Bùi Thị THu, Đỗ Thị Mỹ Ngọc, Nguyễn Thị Thanh Mai, Mai Văn Tuấn, "Nghiên cứu chế tạo màng mỏng chấm lượng tử cacbon pha tạp nitơ ứng dụng phát hiện kim loại nặng", Tạp chí Hóa học, 56 (2019), tr. 68-71, 2019. [9]. M. H. Chan, R. S. Liu, "Carbon nitride quantum dots and their applications, Phosphors, Up Convers. Nano Part." Quantum Dots Their Appl., 2 (2016), pp. 485-502. doi:10.1007/978- 981-10-1590-8_17, 2016. [10]. L. Lin, Y. Luo, P. Tsai, J. Wang, X. Chen, "Metal ions doped carbon quantum dots: Synthesis, physicochemical properties, and their applications", TrAC - Trends Anal. Chem., 103 (2018), pp. 87-101. doi:10.1016/j.trac.2018.03.015, 2018. [11]. S. A. Rub Pakkath, S. S. Chetty, P. Selvarasu, A. Vadivel Murugan, Y. Kumar, L. Periyasamy, M. Santhakumar, S. R. Sadras, K. Santhakumar, "Transition Metal Ion (Mn2+, Fe2+, Co2+, and Ni2+)-Doped Carbon Dots Synthesized via Microwave-Assisted Pyrolysis: A Potential Nanoprobe for Magneto-fluorescent Dual- Modality Bioimaging", ACS Biomater. Sci. Eng., 4 (2018), pp. 2581-2596. doi:10.1021/acsbiomaterials.7b00943, 2018. [12]. Z. Xia, L. Dai, N. Li, R. Su, Q. Xu, X. Zheng, C. Xu, W. Li, Y. Chen, H. Pan, J. Zhu, S. Theruvakkattil Sreenivasan, "Metal Charge Transfer Doped Carbon Dots with Reversibly Switchable, Ultra-High Quantum Yield Photoluminescence", ACS Appl. Nano Mater., 1 (2018), pp. 1886-1893. doi:10.1021/acsanm.8b00277, 2018. [13]. P. P. Zhu, Z. Cheng, L. L. Du, Q. Chen, K. J. Tan, "Synthesis of the Cu-Doped Dual-Emission Fluorescent Carbon Dots and Its Analytical Application", Langmuir, 34 (2018), pp. 9982- 9989. doi:10.1021/acs.langmuir.8b01230, 2018. [14]. Y. Song, S. Zhu, S. Zhang, Y. Fu, L. Wang, X. Zhao, B. Yang, "Investigation from chemical structure to photoluminescent mechanism: A type of carbon dots from the pyrolysis of citric acid and an amine", J. Mater. Chem. C., 3 (2015), pp. 5976–5984. doi:10.1039/c5tc00813a, 2015. [15]. G. Malloci, G. Mulas, C. Joblin, "Electronic absorption spectra of PAHs up to vacuum UV Towards a detailed model of interstellar PAH photophysics", Astron. Astrophys., 426 (2004), pp. 105-117. doi:10.1051/0004-6361:20040541, 2004. Email: jst@tnu.edu.vn 10
File đính kèm:
 phuong_phap_tong_quat_tong_hop_cham_luong_tu_carbon_pha_tap.pdf
phuong_phap_tong_quat_tong_hop_cham_luong_tu_carbon_pha_tap.pdf

