Hướng dẫn ôn tập kiểm tra cuối kỳ 2 môn Hóa học 10 - Năm học 2020-2021
2. Các yếu tố ảnh hưởng đến tốc độ phản ứng
- Ảnh hưởng của nồng độ: Tốc độ phản ứng tỉ lệ thuận với nồng độ các chất tham gia phản ứng .
- Ảnh hưởng của áp suất: (Đối với phản ứng có chất khí tham gia ) : Khi áp suất tăng , tốc độ phản ứng tăng (hoặc ngược lại )
- Ảnh hưởng của nhiệt độ : khi nhiệt độ tăng , tốc độ phản ứng tăng (hoặc ngược lại ) .
- Ảnh hưởng của diện tích bề mặt : (Đối với phản ứng có chất rắn tham gia ) : Khi diện tích bề mặt tăng , tốc độ phản ứng tăng .
- Ảnh hưởng của chất xúc tác: Chất xúc tác là chất làm tăng tốc độ phản ứng , nhưng không bị tiêu hao trong phản ứng.
Trang 1

Trang 2

Trang 3

Trang 4

Trang 5

Trang 6

Trang 7

Trang 8

Trang 9

Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Hướng dẫn ôn tập kiểm tra cuối kỳ 2 môn Hóa học 10 - Năm học 2020-2021", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Hướng dẫn ôn tập kiểm tra cuối kỳ 2 môn Hóa học 10 - Năm học 2020-2021
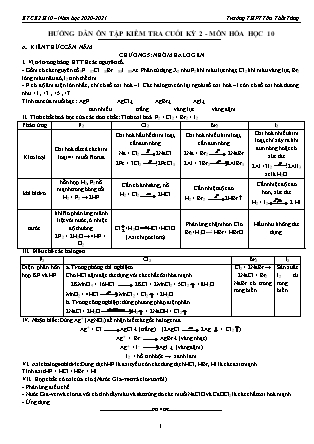
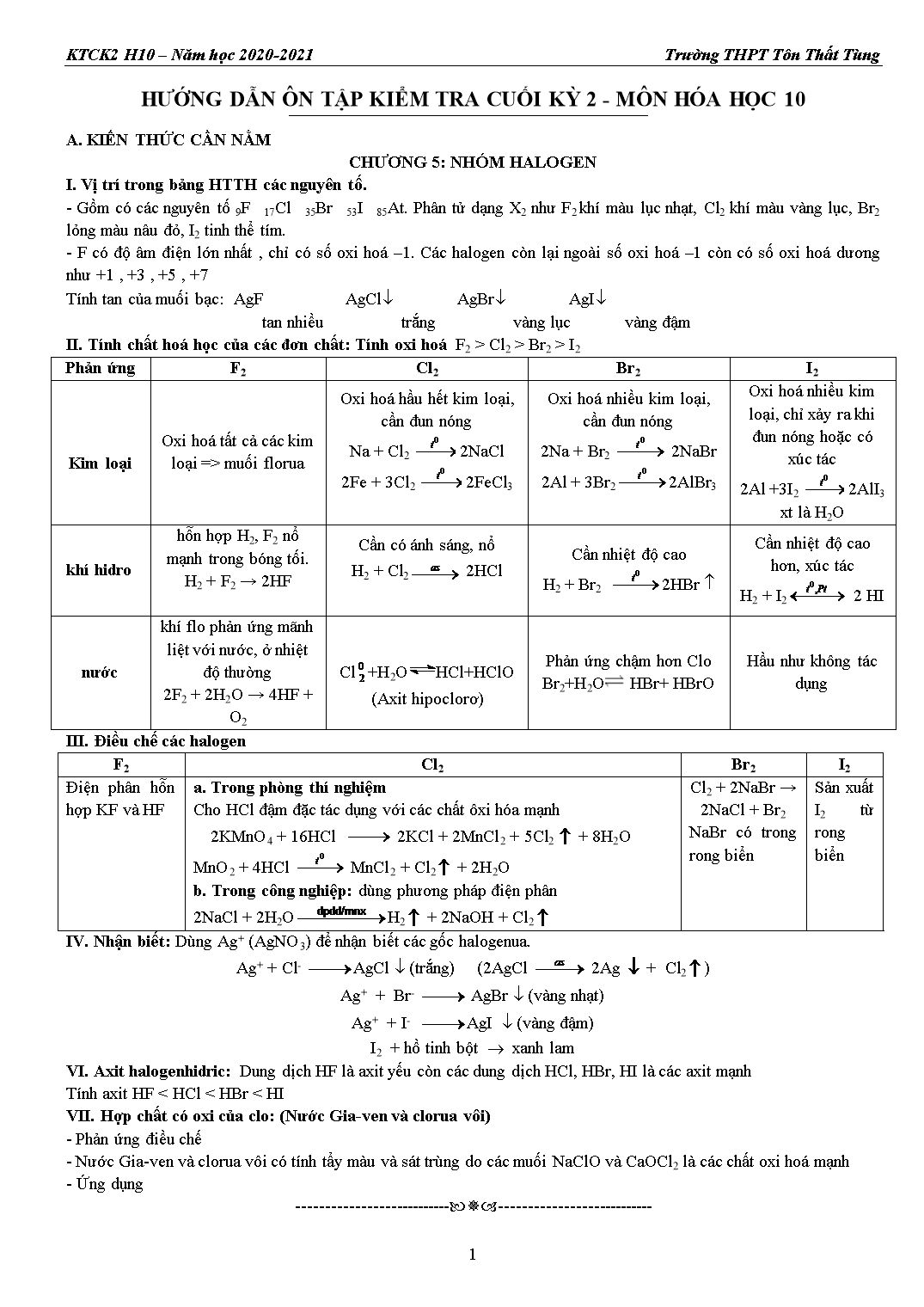
HƯỚNG DẪN ÔN TẬP KIỂM TRA CUỐI KỲ 2 - MÔN HÓA HỌC 10 A. KIẾN THỨC CẦN NẰM CHƯƠNG 5: NHÓM HALOGEN I. Vị trí trong bảng HTTH các nguyên tố. - Gồm có các nguyên tố 9F 17Cl 35Br 53I 85At. Phân tử dạng X2 như F2 khí màu lục nhạt, Cl2 khí màu vàng lục, Br2 lỏng màu nâu đỏ, I2 tinh thể tím. - F có độ âm điện lớn nhất , chỉ có số oxi hoá –1. Các halogen còn lại ngoài số oxi hoá –1 còn có số oxi hoá dương như +1 , +3 , +5 , +7 Tính tan của muối bạc: AgF AgCl¯ AgBr¯ AgI¯ tan nhiều trắng vàng lục vàng đậm II. Tính chất hoá học của các đơn chất: Tính oxi hoá F2 > Cl2 > Br2 > I2 Phản ứng F2 Cl2 Br2 I2 Kim loại Oxi hoá tất cả các kim loại => muối florua Oxi hoá hầu hết kim loại, cần đun nóng Na + Cl2 2NaCl 2Fe + 3Cl2 2FeCl3 Oxi hoá nhiều kim loại, cần đun nóng 2Na + Br2 2NaBr 2Al + 3Br22AlBr3 Oxi hoá nhiều kim loại, chỉ xảy ra khi đun nóng hoặc có xúc tác 2Al +3I2 2AlI3 xt là H2O khí hidro hỗn hợp H2, F2 nổ mạnh trong bóng tối. H2 + F2 → 2HF Cần có ánh sáng, nổ H2 + Cl2 2HCl Cần nhiệt độ cao H2 + Br2 2HBr Cần nhiệt độ cao hơn, xúc tác H2 + I2 2 HI nước khí flo phản ứng mãnh liệt với nước, ở nhiệt độ thường 2F2 + 2H2O → 4HF + O2 Cl+H2OHCl+HClO (Axit hipoclorơ) Phản ứng chậm hơn Clo Br2+H2O HBr+ HBrO Hầu như không tác dụng III. Điều chế các halogen F2 Cl2 Br2 I2 Điện phân hỗn hợp KF và HF a. Trong phòng thí nghiệm Cho HCl đậm đặc tác dụng với các chất ôxi hóa mạnh 2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 + 8H2O MnO2 + 4HCl MnCl2 + Cl2 + 2H2O b. Trong công nghiệp: dùng phương pháp điện phân 2NaCl + 2H2OH2 + 2NaOH + Cl2 Cl2 + 2NaBr → 2NaCl + Br2 NaBr có trong rong biển Sản xuất I2 từ rong biển IV. Nhận biết: Dùng Ag+ (AgNO3) để nhận biết các gốc halogenua. Ag+ + Cl- AgCl ¯ (trắng) (2AgCl 2Ag + Cl2) Ag+ + Br- AgBr ¯ (vàng nhạt) Ag+ + I- AgI ¯ (vàng đậm) I2 + hồ tinh bột ® xanh lam VI. Axit halogenhidric: Dung dịch HF là axit yếu còn các dung dịch HCl, HBr, HI là các axit mạnh Tính axit HF < HCl < HBr < HI VII. Hợp chất có oxi của clo: (Nước Gia-ven và clorua vôi) - Phản ứng điều chế - Nước Gia-ven và clorua vôi có tính tẩy màu và sát trùng do các muối NaClO và CaOCl2 là các chất oxi hoá mạnh - Ứng dụng ---------------------------¯--------------------------- CHƯƠNG 6: OXI – LƯU HUỲNH I. OXI. Oxi là một phi kim hoạt động và là một chất oxi hóa mạnh 1. Tác dụng hầu hết với kim loại, phi kim (trừ halogen): cần có t0 tạo ôxit 2Mg + O2 2MgO S + O2 SO2 C + O2 CO2 2. Tác dụng với các hợp chất. CH4 + 2O2 CO2 + 2H2O C2H5OH + 3O2 → 2CO2 + 3H2O 3. Điều chế oxi a. PTN: Nhiệt phân KMnO4 rắn, KClO3 rắn: 2KMnO4 K2MnO2 + MnO2 + O2 b. CN: Chưng cất phân đoạn không khí lỏng hoặc điện phân nước II. OZON là dạng thù hình của oxi và có tính ôxi hóa mạnh hơn O2 rất nhiều 2Ag + O3 Ag2O + O2 (ở điều kiện thường oxi không có phản ứng) III. LƯU HUỲNH là chất ôxi hóa nhưng yếu hơn O2, ngoài ra S còn đóng vai trò là chất khử khi tác dụng với oxi 1. S là chất oxi hóa khi tác dụng với kim loại và H2 tạo sunfua chứa S2- Tác dụng với nhiều kim loại (có t0,tạo sản phẩm ứng số oxy hoá thấp của kim loại) Fe + S0 FeS-2 (sắt II sunfua) Hg + S HgS-2 (thủy ngân sunfua, phản ứng xảy ra ở t0 thường) Tác dụng với H2: tạo hidro sunfua mùi trứng ung (trứng thối ) H2 + S H2S-2 (hidrosunfua) 2. S là chất khử khi tác dụng với chất ôxi hóa tạo hợp chất với số oxi hoá dương (+4, +6) Tác dụng với một số phi kim S + O2 SO2 (khí sunfurơ, lưu huỳnh điôxit, lưu huỳnh (IV) ôxit.) S + 3F2 → SF6 IV. HIDRO SUNFUA (H2S) là chất khử mạnh 1. Tác dụng với oxi có thể tạo S hoặc SO2 tùy lượng ôxi và cách tiến hành phản ứng. 2H2S + 3O22H2O + 2SO2 (dư ôxi, đốt cháy) 2H2S + O22H2O + 2S 2. Dung dịch H2S có tính axit yếu : Khi tác dụng dung dịch kiềm có thể tạo muối axit hoặc muối trung hoà H2S + NaOH NaHS + H2O H2S + 2NaOH Na2S + 2H2O 3. Điều chế khí H2S: PTN từ phản ứng FeS + 2HCl ® FeCl2 + H2S . Công nghiệp không sản xuất V. LƯU HUỲNH ĐIOXIT công thức hóa học SO2, ngoài ra có các tên gọi khác là lưu huỳnh dioxit hay khí sunfurơ, hoặc anhidrit sunfurơ. 1. Tính chất hoá học: a. SO2 là một oxit axit: tác dụng với nước tạo axit sunfurơ H2SO3 SO2 + NaOH NaHSO3 hoặc SO2 + 2 NaOH Na2SO3 + H2O b. SO2 vừa là chất khử, vừa là chất oxi hoá 2 + Br2 + 2H2O → 2HBr + H24 (SO2đóng vai trò là chất khử) 2 + 2H2S ® 2H2O + 3(SO2đóng vai trò là chất oxi hoá) 2. Điều chế a. Phòng thí nghiệm: Na2SO3 + H2SO4 Na2SO4 + H2O + SO2 b. Công nghiệp: 4FeS2 + 11O2 2Fe2O3 + 8SO2 VI. LƯU HUỲNH (VI) OXIT công thức hóa học SO3, ngoài ra còn tên gọi khác lưu huỳnh tri oxit, anhidrit sunfuric. Là một ôxit axit Tác dụng với H2O tạo axit sunfuric: SO3 + H2O ® H2SO4 + Q Tác dụng với oxit bazơ và bazơ tạo muối sunfat: SO3 + 2NaOH ® Na2SO4 + H2O VII. AXIT SUNFURIC H2SO4 ở trạng thái loãng là một axit mạnh, ở trạng thái đặc là một chất ôxi hóa mạnh. 1. Tính chất của axit sunfuric loãng là axít mạnh làm đỏ quì tím, tác dụng kim loại(trước H2) giải phóng H2, tác dụng bazơ, oxit bazơ và nhiều muối. 2. Tính chất của axit sunfuric đặc là một chất ôxihóa mạnh và có tính háo nước a. Tính oxi hoá mạnh: axit sunfuric đặc nóng oxi hoá hầu hết các kim loại (trừ Au và Pt), nhiều phi kim (C, S, P...) và nhiều hợp chất: 2Fe + 6 H2SO4 Fe2(SO4)3+ 3SO2+ 6H2O Cu + 2 H2SO4 CuSO4 + SO2 + 2H2O Lưu ý: Al, Fe, Cr không tác dụng với H2SO4 đặc nguội, vì kim loại bị thụ động hóa. 2H2SO4(đ) + C CO2 + 2SO2 + 2H2O 2H2SO4(đ) + S 3SO2 + 2H2O FeO + H2SO4 (đ) Fe2(SO4)3 + SO2 + 4H2O b. Tính háo nước: hấp thụ nước của một số chất hữu cơ. Ví dụ: nhỏ H2SO4(đ) vào đường saccarozơ C12H22O11 + H2SO4(đ) → 12C + H2SO4.11H2O 2H2SO4(đ) + C CO2 + 2SO2 + 2H2O 3. Điều chế axit sunfuric - Sản xuất SO2 từ FeS2 hoặc S: 4FeS2 + 11O2 2Fe2O 3 + 8SO2 hoặc S + O2 SO2 - Oxi hoá SO2 2SO2 + O2 2SO3 - Hấp thụ SO3 bằng H2SO4: SO3 + H2SO4 H2SO4.nSO3 (ôleum) H2SO4.nSO3 + n H2O ® (n+1) H2SO4 4. Nhận biết ion sunfat: Nhận biết gốc SO42- (sunfat) dùng dung dịch muối bari như BaCl2 hoặc Ba(OH)2. Tạo kết tủa t ... Câu 27: Cho cân bằng hóa học: N2 (k) + 3H2(k) 2NH3 (k) ΔH < 0 . Cân bằng trên chuyển dịch theo chiều thuận khi A. giảm áp suất của hệ phản ứng. B. tăng áp suất của hệ phản ứng. C. tăng nhiệt độ của hệ phản ứng. D. thêm chất xúc tác vào hệ phản ứng. Câu 28: Xét cân bằng: N2O4 (k) ⇄ 2NO2 (k) ở 25oC. Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2 A. tăng 9 lần. B. giảm 3 lần. C. tăng 4,5 lần. D. tăng 3 lần. PHẦN TỰ LUẬN: (3,0 điểm) Câu 29: (1 điểm) Viết phương trình hóa học của các phản ứng theo sơ đồ sau: SO3 ® H2SO4 ® Na2SO4 ® NaCl ® HCl Câu 30: (1 điểm) Trong những trường hợp dưới đây, yếu tố nào đã ảnh hưởng đến tốc độ phản ứng? a. Tốc độ của phản ứng giữa natri và clo tăng lên khi đun nóng. b. Sự cháy diễn ra mạnh và nhanh hơn khi đưa lưu huỳnh đang cháy ngoài không khí vào lọ đựng khí oxi. c. Bột nhôm tác dụng với dung dịch axit clohidric nhanh hơn so với nhôm dây. d. Phản ứng oxi hóa SO2 tạo thành SO3 diễn ra nhanh hơn khi có mặt V2O5. Câu 31: (0,5 điểm) Cho phản ứng nung vôi xảy ra trong bình kín: CaCO3(r) CaO(r) + CO2(k) ∆H=178 kJ Cân bằng sẽ thay đổi như thế nào nếu thay đổi các điều kiện sau: a. Thêm vào cân bằng khí CO2. b. Giảm nhiệt độ phản ứng. Câu 32: Chia m gam hỗn hợp (X) gồm Fe và FeO thành hai phần bằng nhau: - Phần 1: Hòa tan hoàn toàn phần 1 trong H2SO4 loãng, dư thì thu được 0,2 mol khí. - Phần 2: Hoà tan hết trong H2SO4 đặc, dư thì thu được 0,35 mol khí SO2 (duy nhất). a. Tính giá trị của m. b. Tính số mol NaOH tối thiểu cần để hấp thụ hết lượng khí SO2 trên. ---------------------------¯--------------------------- TRƯỜNG TRUNG HỌC PHỔ THÔNG TÔN THẤT TÙNG TỔ HÓA HỌC KIỂM TRA CUỐI HỌC KÌ 2 NĂM HỌC 2020 - 2021 Môn: Hóa học - Lớp 10 Thời gian làm bài: 45 phút (không tính thời gian phát đề) ĐỀ THAM KHẢO SỐ 4 PHẦN TRẮC NGHIỆM (7 điểm) Câu 1: Ở điều kiện thường, brom là chất A. rắn màu vàng. B. khí không màu. C. lỏng màu nâu đỏ. D. rắn màu đen tím. Câu 2: Trong phòng thí nghiệm, người ta điều chế oxi bằng cách nào sau đây? A. Điện phân nước. B. Nhiệt phân Cu(NO3)2. C. Nhiệt phân KClO3 có xúc tác MnO2. D. Chưng cất phân đoạn không khí lỏng. Câu 3: Nguyên tố lưu huỳnh thuộc nhóm nhóm VIA có cấu hình electron ở lớp ngoài cùng là A. ns2. B. ns2np4. C. np4. D. nd6. Câu 4: Tính chất vật lí nào sau đây của hidrosunfua là không đúng? A. Chất khí. B. Tan nhiều trong nước. C. Mùi trứng thối. D. Nhẹ hơn không khí. Câu 5: Phương pháp điều chế SO2 trong công nghiệp là A. đốt cháy S. B. đốt cháy H2S. C. cho Na2SO3 tác dụng với dung dịch H2SO4. D. nhiệt phân CaSO3. Câu 6: Lưu huỳnh trioxit thuộc loại oxit nào sau đây? A. Oxit axit. B. Oxit bazơ. C. Oxit trung tính. D. Oxit lưỡng tính. Câu 7: Công thức chung của oleum là A. H2SO4.nSO3. B. H2SO4.nSO2. C. H2SO3.nSO2. D. H2SO3.nSO3. Câu 8: Dùng dung dịch nào sau đây để phân biệt hai dung dịch Na2SO4 và NaCl? A. NaCl. B. BaCl2. C. K2CO3. D. NaOH. Câu 9: Nguyên tắc pha loãng dung dịch axit H2SO4 đặc cần tiến hành như thế nào để an toàn? A. Rót từ từ axit vào nước. B. Rót từ từ nước vào axit. C. Rót nước thật nhanh vào axit. D. Rót nhanh axit vào nước. Câu 10: Sục khí SO2 dư vào bình đựng dung dịch Br2. Hiện tượng quan sát được là A. dung dịch Br2 không đổi màu. B. dung dịch Br2 bị mất màu. C. có kết tủa xuất hiện. D. vừa có kết tủa vừa mất màu dung dịch Br2. Câu 11: Để đánh giá mức độ xảy ra nhanh, chậm của các phản ứng hóa học, người ta đưa ra khái niệm A. tốc độ phản ứng. B. cân bằng hóa học. C. nồng độ. D. chất xúc tác. Câu 12: Tốc độ phản ứng không phụ thuộc vào yếu tố nào sau đây? A. Nhiệt độ. B. Nồng độ. C. Chất xúc tác. D. Thể tích dung dịch. Câu 13: Tốc độ phản ứng được xác định bằng độ biến thiên nồng độ của A. một trong các chất phản ứng trong một đơn vị thời gian. B. một trong các sản phẩm trong một đơn vị thời gian. C. một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian. D. các chất có trong phản ứng trong một đơn vị thời gian. Câu 14: Một phản ứng thuận nghịch ở trạng thái cân bằng khi nào? A. Phản ứng thuận đã kết thúc. B. Tốc độ phản ứng thuận và nghịch bằng nhau. C. Phản ứng nghịch đã kết thúc. D. Nồng độ chất tham gia và sản phẩm như nhau. Câu 15: Dùng không khí nén thổi vào lò cao để đốt cháy than cốc (trong sản xuất gang), yếu tố nào ảnh hưởng đến tốc độ phản ứng? A. Nồng độ. B. Xúc tác. C. Tăng diện tích. D. Nhiệt độ, áp suất. Câu 16: Hai nhóm học sinh làm thí nghiệm: - Nhóm thứ nhất: thả miếng Zn 1 gam vào cốc đựng 200ml dung dịch axit HCl 2M. - Nhóm thứ hai: thả 1 gam bột Zn vào cốc đựng 300ml dung dịch axit HCl 2M Kết quả là bột khí thoát ra ở thí nghiệm của nhóm thứ hai nhanh hơn. Nguyên nhân là A. thể tích axit nhiều hơn. B. diện tích bề mặt bột Zn lớn hơn. C. nồng độ Zn bột lớn hơn. D. nồng độ miếng Zn lớn hơn. Câu 17: Phản ứng nào sau đây là không đúng? A. H2 + F2 2HF. B. H2 + Cl2 2HCl. C. H2 + Br22HBr. D. H2 + I2 2HI. Câu 18 : Cho 6 gam một kim loại R có hóa trị II khi tác dụng với oxi tạo ra 10 gam oxit. Kim loại R là A. Zn. B. Fe. C. Mg. D. Ca. Câu 19: Cho các phản ứng hóa học sau: (1) S + O2 SO2. (2) S + Mg MgS. (3) S + F2SF6. Phản ứng hóa học nào trong đó đơn chất lưu huỳnh thể hiện tính oxi hóa? A. (1), (2). B. (1), (3). C. (2), (3). D. (2). Câu 20: Cho phản ứng: H2S + Cl2 + H2O → H2SO4 + HCl.Chất khử và chất oxi hóa lần lượt trong phản ứng trên là A. H2S và Cl2. B. Cl2 và H2S. C. H2S và H2O. D. H2O và H2S. Câu 21: Hấp thụ hoàn toàn V lít khí SO2 (đktc) vào 100ml dung dịch KOH 1M, sau phản ứng chỉ thu được muối axit. Giá trị của V là A. 2,24. B. 3,36. C. 4,48. D. 5,60. Câu 22: Dung dịch H2SO4 loãng tác dụng với tất cả các chất trong dãy nào sau đây? A. BaCl2, NaCl, Al, Cu(OH)2. B. Fe(OH)2, Na2CO3, CuCl2, NH3. C. Zn(OH)2, CaCO3, CuO, Al. D. CaCO3, Cu, Al(OH)3, MgO. Câu 23: Kim loại nào sau đây phản ứng với H2SO4 loãng và H2SO4 đặc, nóng cho hai muối khác nhau? A. Al. B. Fe. C. Mg. D. Zn. Câu 24: Cho 5,4 gam Al hòa tan hoàn toàn với dung dịch H2SO4 loãng dư, thu được V lít khí SO2 (đktc). Gía trị của V là A. 4,48. B. 6,72. C. 8,96. D. 11,2. Câu 25: Tiến hành thí nghiệm: Cho kim loại Cu vào ống nghiệm chứa dung dịch H2SO4 đặc, đun nhẹ, thấy kim loại Cu tan, có khí thoát ra và dung dịch thu được A. có màu xanh. B. có màu vàng. C. không màu . D. có màu da cam. Câu 26: Yếu tố nào dưới đây được sử dụng để làm tăng tốc độ phản ứng khi rắc men vào tinh bột đã được nấu chín để ủ rượu? A. Chất xúc tác. B. Áp suất. C. Nồng độ. D. Nhiệt độ. Câu 27: Hệ cân bằng xảy ra trong bình kín I2 (k) + H2 (k) 2HI (k) ∆H > 0. Khi giữ nguyên các điều kiện khác, nếu thêm I2 vào bình phản ứng thì cân bằng sẽ A. chuyển dịch theo chiều thuận. B. chuyển dịch theo chiều nghịch. C. chuyển dịch theo chiều tăng nồng độ H2. D. không chuyển dịch. Câu 28: Cho ba mẫu đã vôi có cùng khối lượng: mẫu (1) dạng khối, mẫu (2) dạng viên nhỏ, mẫu (3) dạng bột mịn vào ba cốc đựng cùng thể tích dung dịch HCl 1M(dư). Thời gian để đá vôi tan hết tương ứng trong ba cốc là t1, t2, t3 (giây). Biểu thức nào sau đây đúng? A. t1 = t2 = t3. B. t1 < t2 < t3. C. t3 < t2 < t1. D. t2 < t1 < t3. PHẦN TỰ LUẬN (3 điểm) Câu 29 (1 điểm) Viết các phương trình hoá học thực hiện chuỗi phản ứng sau (ghi rõ điều kiện phản ứng nếu có) FeS2 1 SO2 2 S 3 H2S 4 H2SO4 Câu 30 (1 điểm) Cho 6 gam kẽm hạt vào cốc đựng dung dịch H2SO4 4M (dư) ở nhiệt độ thường. Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau đây thì tốc độ phản ứng biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)? Giải thích. a. Thay dung dịch H2SO4 4M bằng dung dịch H2SO4 2M. b. Dùng thể tích dung dịch H2SO4 4M gấp đôi ban đầu. Câu 31 (0,5 điểm) Cho cân bằng: CO (k) + H2O (k) CO2 (k) + H2 (k) ∆H = -41 kJ. Cân bằng hóa học của hệ sẽ chuyển dịch như thế nào nếu thay đổi một trong các yếu tố sau: a. Tăng nhiệt độ của hệ. b. Thêm một lượng hơi nước vào hệ. Câu 32 (0,5 điểm) Hòa tan hoàn toàn 17,1 gam hỗn hợp X gồm Mg, Al và Cu vào dung dịch H2SO4 đặc, vừa đủ. Kết thúc phản ứng thu được dung dịch Y và 0,5 mol khí SO2 (sản phẩm khử duy nhất). Cô cạn Y thu được m gam hỗn hợp muối. Tính giá trị của m. ---------------------------¯--------------------------- TRƯỜNG TRUNG HỌC PHỔ THÔNG TÔN THẤT TÙNG TỔ HÓA HỌC KIỂM TRA CUỐI HỌC KÌ 2 NĂM HỌC 2020 - 2021 Môn: Hóa học - Lớp 10 Thời gian làm bài: 45 phút (không tính thời gian phát đề) ĐỀ THAM KHẢO SỐ 5 PHẦN TRẮC NGHIỆM (7 điểm) Câu 1: Ở điều kiện thường, clo là chất A. rắn màu vàng. B. khí không màu. C. khí màu vàng lục. D. rắn màu lục nhạt. Câu 2: Công thức của muối natri clorua là A. NaCl. B. KCl. C. NaClO. D. CaOCl2. Câu 3: Trong bảng tuần hoàn, lưu huỳnh thuộc nhóm VIA. Số electron lớp ngoài cùng của nguyên tử lưu huỳnh là A. 4. B. 5. C. 6. D. 7. Câu 4: Lưu huỳnh đioxit có công thức là A. H2S. B. SO3. C. SO2. D. H2SO4. Câu 5: Số nguyên tử oxi trong phân tử lưu huỳnh trioxit là A. 1. B. 2. C. 3. D. 4. Câu 6: Ở điều kiện thường, hiđro sunfua là chất A. khí, mùi trứng thối. B. khí, không mùi. C. lỏng, mùi trứng thối. D. lỏng, không màu. Câu 7: Chất nào sau đây nhận biết được ion sunfat ? A. BaCl2. B. HCl. C. KNO3. D. HNO3. Câu 8: Muốn pha loãng H2SO4 đặc, phải rót A. từ từ axit vào nước và khuấy nhẹ. B. từ từ nước vào axit và khuấy nhẹ. C. nhanh axit vào nước và khuấy nhẹ. D. nhanh nước vào axit và khuấy nhẹ. Câu 9: Hấp thụ SO3 bằng H2SO4 đặc (98%), thu được oleum có công thức dạng A. H2SO4.nH2O. B. H2SO4.nSO3. C. H2SO4.nSO2. D. H2SO4. Câu 10: Dẫn khí X vào nước brom, thấy nước brom mất màu. Khí X là A. SO2. B. CO2. C. O2. D. N2. Câu 11: Để đánh giá mức độ xảy ra nhanh, chậm của các phản ứng hóa học, người ta đưa ra khái niệm A. tốc độ phản ứng. B. cân bằng hóa học. C. nồng độ. D. chất xúc tác. Câu 12: Khi cho MnO2 vào dung dịch H2O2 thì H2O2 bị phân hủy nhanh hơn, khi đó yếu tố nào đã làm tăng tốc độ phản ứng phân hủy H2O2? A. Áp suất. B. Nhiệt độ. C. Nồng độ. D. Chất xúc tác. Câu 13: Nếu giữ nguyên các điều kiện khác mà chỉ thay đổi một yếu tố thì yếu tố nào sau đây sẽ làm tăng tốc độ ban đầu của phản ứng? A. Giảm nhiệt độ của phản ứng. B. Giảm áp suất hệ phản ứng. C. Tăng nhiệt độ của phản ứng. D. Giảm nồng độ chất phản ứng. Câu 14: Yếu tố nào sau đây không thể làm chuyển dịch cân bằng hóa học? A. Nhiệt độ. B. Áp suất. C. Chất xúc tác. D. Nồng độ. Câu 15: Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi A. tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. B. tốc độ phản ứng thuận lớn hơn tốc độ phản ứng nghịch. C. tốc độ phản ứng thuận nhỏ hơn tốc độ phản ứng nghịch. D. các phản ứng thuận và phản ứng nghịch đã kết thúc. Câu 16: Cho một hạt Zn vào dung dịch H2SO4 loãng, sau đó đun nóng thì A. bọt khí thoát ra nhanh hơn. B. bọt khí thoát ra chậm hơn. C. tốc độ thoát khí không đổi. D. kẽm tan chậm hơn. Câu 17: Trong phản ứng: 3Cl2 + 2Fe 2FeCl3, clo thể hiện A. tính khử mạnh. B. tính khử yếu. C. tính oxi hóa mạnh. D. cả tính oxi hóa và tính khử. Câu 18: Khi cho Cl2 tác dụng với dung dịch NaOH ở nhiệt độ thường, thu được dung dịch chứa hai muối nào sau đây? A. KCl và KClO3. B. NaCl và NaClO. C. NaCl và NaClO3. D. KCl và KClO3. Câu 19: Muốn thu hồi thủy ngân bị rơi vãi người ta dùng chất nào sau đây? A. S. B. O2. C. Cl2. D. N2. Câu 20: Hấp thụ hết 0,1 mol SO2 vào dung dịch NaOH dư. Số mol NaOH đã phản ứng là A. 0,10. B. 0,20. C. 0,15. D. 0,05. Câu 21: Khi dẫn khí SO2 vào dung dịch H2S thì trong dung dịch xuất hiện A. kết tủa màu đen. C. kết tủa màu vàng. B. kết tủa màu trắng. D. kết tủa màu đỏ. Câu 22: Hoà tan hoàn toàn 5,6 gam Fe cần vừa đủ dung dịch chứa x mol H2SO4 loãng. Giá trị của x là A. 0,10. B. 0,15. C. 0,05 D. 0,20. Câu 23: Cho 0,1 mol FeSO4 tác dụng hết với dung dịch BaCl2 dư, thu được m gam kết tủa . Giá trị của m là A. 23,30. B. 11,65. C. 46,60. D. 34,95. Câu 24: Trong phản ứng: Cu + 2H2SO4 (đặc, nóng) CuSO4 + SO2 + 2H2O, axit H2SO4 thể hiện tính A. oxi hóa mạnh. B. khử mạnh. C. axit mạnh. D. háo nước. Câu 25: Tiến hành thí nghiệm: Cho kim loại Cu vào ống nghiệm chứa dung dịch H2SO4 (đặc), đun nhẹ, thấy kim loại Cu tan, có khí thoát ra và dung dịch thu được A. có màu xanh. B. có màu vàng. C. không màu . D. có màu da cam. Câu 26: Người ta đã lợi dụng yếu tố nào để tăng tốc độ phản ứng khi dùng không khí nén, nóng thổi vào lò cao để đốt cháy than cốc trong sản xuất gang? A. Nhiệt độ và diện tích tiếp xúc. C. Nhiệt độ và áp suất. B. Áp suất và diện tích tiếp xúc. D. Nồng độ và diện tích tiếp xúc. Câu 27: Hệ cân bằng xảy ra trong bình kín: ∆H > 0. Khi giữ nguyên các điều kiện khác, nếu thêm H2 vào bình phản ứng thì cân bằng sẽ A. chuyển dịch theo chiều thuận. B. chuyển dịch theo chiều nghịch. C. chuyển dịch theo chiều tăng nồng độ H2. D. không chuyển dịch. Câu 28: Tiến hành thí nghiệm: Cho một hạt kẽm vào ống nghiệm chứa 3 ml dung dịch HCl 10%. Nếu giữ nguyên các điều kiện khác thì tốc độ phản ứng trong thí nghiệm sẽ tăng khi thay dung dịch HCl 10% bằng dung dịch HCl có nồng độ nào sau đây? A. 6%. B. 8%. C. 5%. D. 15%. PHẦN TỰ LUẬN (3 điểm) Câu 29 (1 điểm): Cho cân bằng: Cần tác động các yếu tố (nhiệt độ, nồng độ, áp suất) như thế nào để cân bằng trên chuyển dịch theo chiều thuận? Giải thích. Câu 30 (1 điểm): Nung nóng 14,4 gam hỗn hợp X gồm Fe và S (trong điều kiện không có oxi), thu được hỗn hợp Y. Hòa tan Y trong dung dịch HCl dư, thu được 4,48 lít hỗn hợp khí. Biết các phản ứng xảy ra hoàn toàn. a. Viết phương trình phản ứng xảy ra. b. Tính phần trăm khối lượng các chất trong X. Câu 31 (0,5 điểm): Khi làm thí nghiệm điều chế các khí H2S và khí Cl2. Một học sinh đề xuất dùng H2SO4 đặc để làm khô hai khí này. Hãy cho biết quan điểm của em về đề xuất trên. Giải thích và viết phương trình phản ứng (nếu có). Câu 32 (0,5 điểm): Đốt cháy hoàn toàn m gam FeS2 trong O2 thu được Fe2O3 và SO2.. Hấp thụ hết SO2 vào dung dịch chứa 0,015 mol Ba(OH)2, sau khi phản ứng xảy ra hoàn toàn thu được 2,17 gam kết tủa. Tính m.
File đính kèm:
 huong_dan_on_tap_kiem_tra_cuoi_ky_2_mon_hoa_hoc_10_nam_hoc_2.docx
huong_dan_on_tap_kiem_tra_cuoi_ky_2_mon_hoa_hoc_10_nam_hoc_2.docx

